Clear Sky Science · pl
Historia i funkcja kolistego RNA
Jak małe pętle RNA pomagają zestresowanym mózgom radzić sobie
Kiedy cierpimy na brak snu, ulegamy urazowi lub jesteśmy emocjonalnie przeciążeni, komórki mózgu muszą szybko dostosować swoją aktywność, by przetrwać i utrzymać funkcjonowanie obwodów. Artykuł opisuje niezwykłą cząsteczkę w mózgu — kolistą formę RNA zwaną Cdr1as — i pokazuje, jak współdziała z innymi małymi RNA, by precyzyjnie regulować komunikację nerwową w warunkach stresu. Zrozumienie tego ukrytego systemu kontroli może otworzyć nowe drogi leczenia udaru, depresji i innych zaburzeń mózgu — a także doprowadzić do testów krwi, które z daleka informowałyby o stanie mózgu.
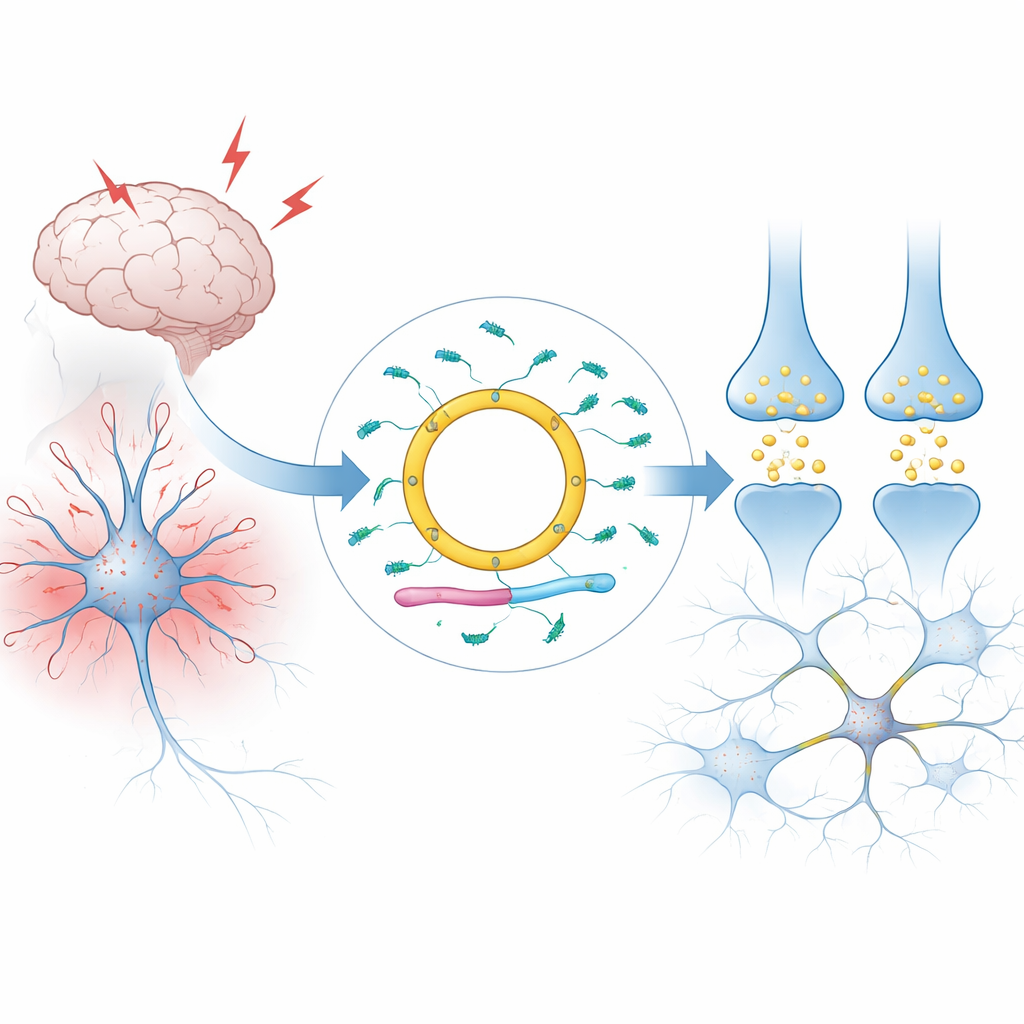
Kolista wiadomość w komórkach mózgu
Większość RNA w naszych komórkach jest liniowa: ma dwa końce i jest szybko rozkładana. Cdr1as jest inny. Tworzy zamkniętą pętlę, co czyni go wyjątkowo stabilnym i pozwala mu gromadzić się w bardzo wysokich stężeniach w mózgach ssaków, zwłaszcza w określonych typach neuronów. Autorzy wyjaśniają, jak Cdr1as powstaje z większej jednostki RNA na chromosomie X przez proces składania końców razem. U ludzi i myszy niemal cały RNA z tego locus jest przekształcany w formę kolistą, z niemal żadną pozostałością wersji liniowej. Obszerne badania tkanek i pojedynczych komórek pokazują, że Cdr1as jest, w praktyce, molekułą specyficzną dla neuronów — rzadko występującą w innych narządach i w komórkach wspierających mózg, takich jak glej.
Gęsta sieć drobnych regulatorów
Znaczenie Cdr1as wynika z towarzystwa, w jakim występuje. Jego kolista sekwencja niesie wyjątkowo dużą liczbę miejsc dokujących dla małego regulatorowego RNA zwanego miR-7 — około siedemdziesięciu u ludzi i około 130 u myszy. miR-7 należy do cenionej rodziny mikroRNA, niedawno uhonorowanej Nagrodą Nobla, które jednocześnie wyciszają wiele informacyjnych wiadomości kodujących białka. W neuronach miR-7 celuje w przekazy związane z reakcjami na stres i uwalnianiem przekaźnika glutaminianu. Cdr1as wiąże miR-7 w żywej tkance mózgowej, wpływając na to, jak długo miR-7 przetrwa, gdzie jest zlokalizowany wewnątrz neuronu i jak silnie może oddziaływać na swoje liczne cele. Drugie małe RNA, miR-671, potrafi przeciąć i zniszczyć Cdr1as, podczas gdy długie RNA zwane Cyrano powoduje aktywny rozkład samego miR-7. Te trzy niefunkcjonalne RNA i dwa mikroRNA tworzą ściśle powiązany obwód.
Utrzymywanie równowagi aktywności nerwowej pod presją
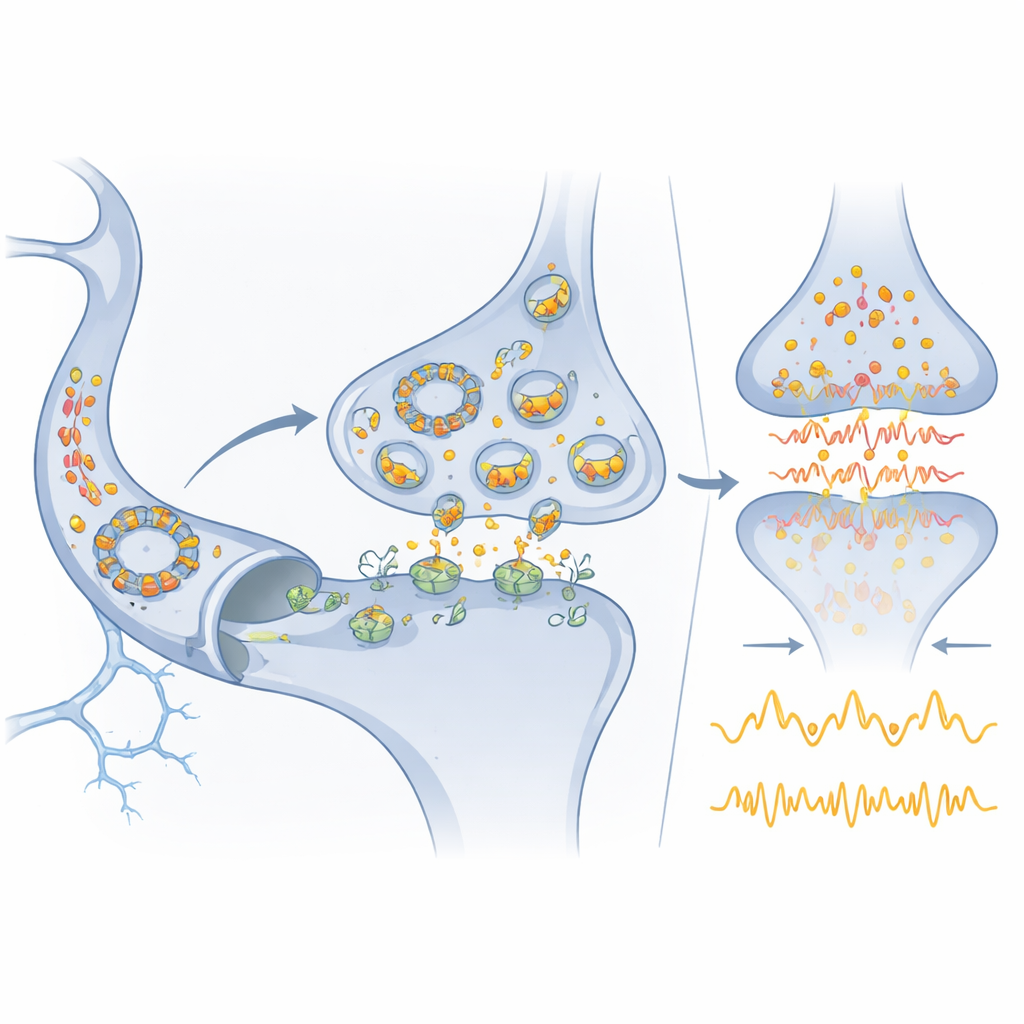
Wykorzystując modele myszy pozbawione poszczególnych elementów tego obwodu, autorzy podsumowują dekadę badań pokazujących, jak kształtuje on funkcjonowanie mózgu. Usunięcie Cdr1as obniża poziomy dojrzałego miR-7 i zaburza ekspresję „genów natychmiast wczesnych”, które normalnie reagują na aktywność i stres. Neurony pozbawione Cdr1as wykazują bardziej nieregularne, nadmiernie pobudliwe wyładowania, a myszy prezentują zmienione reakcje na bodźce sensoryczne. W przeciwieństwie do tego, usunięcie Cyrano prowadzi do silnego nagromadzenia miR-7, co z kolei uniemożliwia akumulację Cdr1as, ujawniając pętlę sprzężenia zwrotnego. Eksperymenty na hodowlach neuronów i na żywych mysich modelach imitujące warunki podobne do udaru pokazują, że poziomy Cdr1as, miR-7 i Cyrano zmieniają się w skoordynowany, zależny od czasu sposób. Te zmiany modyfikują uwalnianie glutaminianu w synapsach, wpływając na przeżywalność neuronów i to, jak sieci neuronalne regenerują się po urazie.
Dodatkowa warstwa ewolucyjna dla precyzyjnej kontroli
Przegląd umieszcza także ten obwód w kontekście ewolucyjnym. miR-7 jest starożytny — pojawił się wraz z pierwszymi zwierzętami rozwijającymi scentralizowane układy nerwowe — i jest głęboko zachowany, ponieważ pomaga kontrolować wczesne decyzje rozwojowe, takie jak te prowadzone przez główny regulator PAX6. Dla odmiany Cyrano pojawiło się później u kręgowców, miR-671 jeszcze później u ssaków z prymitywnymi łożyskami, a Cdr1as dopiero u ssaków łożyskowych. Autorzy twierdzą, że te nowsze RNA stopniowo nałożono na starszy system miR-7, by udoskonalić sposób, w jaki wydzielanie i odpowiedzi na stres są regulowane w wyspecjalizowanych komórkach mózgu i komórkach wydzielających hormony. Proponują, że Cdr1as może działać jak transporter, przenosząc miR-7 do zakończeń nerwowych, gdzie kontrolowana jest miejscowa synteza białek i uwalnianie przekaźnika.
Od obwodu molekularnego do medycyny
Ponieważ Cdr1as jest tak bogato reprezentowany w mózgu, a jednocześnie na tyle stabilny, że można go wykryć we krwi, może służyć jako wygodny marker stanu mózgu w chorobach neurologicznych i psychiatrycznych. miR-7, już wykrywany w różnych płynach ustrojowych, może podobnie pomóc śledzić lub modyfikować procesy chorobowe. Autorzy przedstawiają, jak leki lub terapie oparte na RNA skierowane przeciwko miR-7, Cdr1as lub miR-671 mogłyby kiedyś złagodzić szkodliwe nagromadzenia glutaminianu w udarze lub przywrócić równowagę w sieciach nieprawidłowo wyładowujących się w zaburzeniach nastroju i rozwojowych. Jednocześnie ostrzegają, że większość proponowanych regulatorów RNA kolistego prawdopodobnie nie ma wyjątkowej obfitości i zdolności wiązania charakterystycznej dla Cdr1as. W efekcie ten system staje się punktem odniesienia: pokazuje, że obwody złożone wyłącznie z RNA mogą dorównywać sieciom białkowym pod względem precyzji i odporności, ale też że prawdziwe regulatory o dużej sile wśród RNA kolistych są prawdopodobnie rzadkie i muszą być identyfikowane za pomocą rygorystycznych, ilościowych testów.
Cytowanie: Cerda-Jara, C.A., Scoyni, F., Zolotarov, G. et al. The history and function of a circular RNA. Nat Commun 17, 3862 (2026). https://doi.org/10.1038/s41467-026-71822-0
Słowa kluczowe: RNA koliste, microRNA-7, stres neuronalny, sygnalizacja glutaminergiczna, biomarkery RNA