Clear Sky Science · fr
L’histoire et la fonction d’un ARN circulaire
Comment de petites boucles d’ARN aident le cerveau stressé à faire face
Lorsque nous manquons de sommeil, sommes blessés ou submergés émotionnellement, les cellules cérébrales doivent ajuster rapidement leur activité pour survivre et maintenir le fonctionnement des circuits. Cet article décrit une molécule inhabituelle du cerveau, un fragment d’ARN circulaire appelé Cdr1as, et montre comment elle coopère avec d’autres petits ARN pour affiner la communication entre neurones en situation de stress. Comprendre ce système de contrôle caché pourrait ouvrir de nouvelles voies pour traiter l’accident vasculaire cérébral, la dépression et d’autres troubles cérébraux — et peut‑être même conduire à des tests sanguins renseignant à distance sur l’état du cerveau.
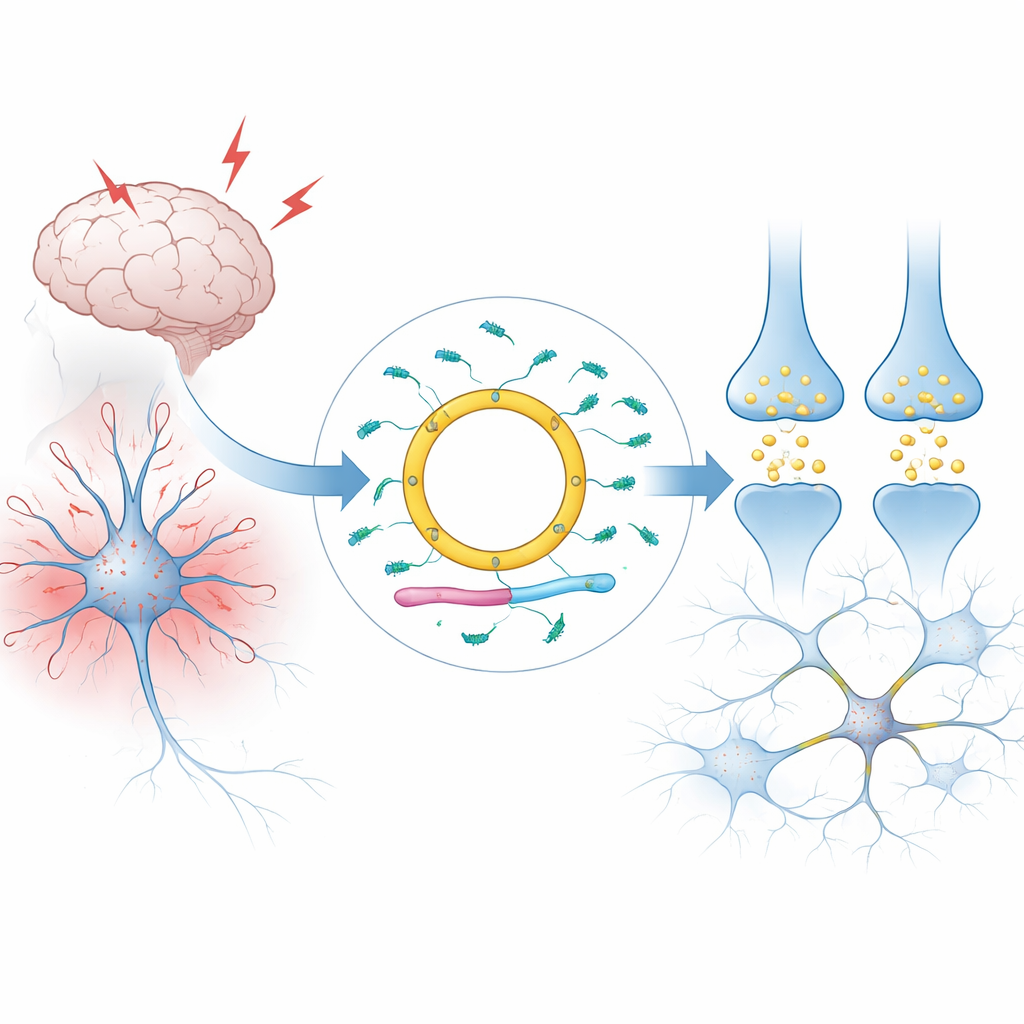
Un message circulaire dans les cellules cérébrales
La plupart des ARN dans nos cellules sont linéaires : ils ont deux extrémités et sont rapidement dégradés. Cdr1as est différent. Il forme une boucle fermée, ce qui le rend exceptionnellement stable et lui permet de s’accumuler à des niveaux très élevés dans les cerveaux des mammifères, en particulier dans certains types de neurones. Les auteurs expliquent comment Cdr1as est produit à partir d’une unité d’ARN plus grande sur le chromosome X par un processus qui assemble ses extrémités. Chez l’homme et la souris, presque tout l’ARN issu de ce locus est converti en forme circulaire, laissant à peine de version linéaire. De larges enquêtes de tissus et d’unicellules montrent que Cdr1as est, à des fins pratiques, une molécule spécifique aux neurones, rare dans d’autres organes et dans les cellules de soutien du cerveau comme les cellules gliales.
Une toile dense de petits régulateurs
Cdr1as tire son importance de la compagnie qu’il garde. Sa séquence circulaire porte un nombre exceptionnel de sites d’ancrage pour un petit ARN régulateur appelé miR‑7 — environ soixante‑dix chez l’homme et environ 130 chez la souris. miR‑7 appartient à la célèbre famille des microARNs, des molécules récemment reconnues par un prix Nobel qui silencient simultanément de nombreux messages codant pour des protéines. Chez les neurones, miR‑7 vise des messages impliqués dans les réponses au stress et la libération du neurotransmetteur glutamate. Cdr1as se lie à miR‑7 dans le tissu cérébral vivant, affectant la durée de vie de miR‑7, son emplacement à l’intérieur du neurone et la force avec laquelle il agit sur ses nombreuses cibles. Un second petit ARN, miR‑671, peut couper et détruire Cdr1as, tandis qu’un long ARN appelé Cyrano provoque la dégradation active de miR‑7 lui‑même. Ensemble, ces trois ARN non codants et ces deux microARNs forment un circuit étroitement connecté.
Maintenir l’équilibre de l’activité nerveuse sous pression
En utilisant des modèles murins dépourvus d’éléments individuels de ce circuit, les auteurs résument une décennie de travaux montrant comment il façonne la fonction cérébrale. La suppression de Cdr1as réduit les niveaux de miR‑7 mature et perturbe l’expression des gènes « précoces immédiats » qui répondent normalement à l’activité et au stress. Les neurones privés de Cdr1as tirent de manière plus erratique, avec une excitabilité excessive, et les souris présentent des réactions altérées aux stimuli sensoriels. À l’inverse, la suppression de Cyrano entraîne une forte accumulation de miR‑7, qui empêche à son tour l’accumulation de Cdr1as, révélant une boucle de rétroaction. Des expériences qui imitent des conditions proches d’un AVC dans des cultures de neurones et chez des souris vivantes démontrent que les niveaux de Cdr1as, miR‑7 et Cyrano évoluent de manière coordonnée et dépendante du temps. Ces modifications altèrent la libération de glutamate aux synapses, influençant la survie des neurones et la capacité des réseaux à récupérer après une lésion.
Un ajout évolutif pour un contrôle fin
La revue situe aussi ce circuit dans son contexte évolutif. miR‑7 est ancien, apparu avec les premiers animaux ayant développé des systèmes nerveux centralisés, et est profondément conservé parce qu’il aide à contrôler des décisions développementales précoces, telles que celles guidées par le régulateur maître PAX6. En revanche, Cyrano est apparu plus tard chez les vertébrés, miR‑671 encore plus tard chez les mammifères à placenta primitif, et Cdr1as seulement chez les mammifères placentaires. Les auteurs soutiennent que ces ARN plus récents se sont superposés progressivement au système miR‑7 plus ancien pour affiner la façon dont la sécrétion et les réponses au stress sont réglées dans des cellules cérébrales spécialisées et des cellules sécrétrices d’hormones. Ils proposent que Cdr1as puisse agir comme un transporteur, emmenant miR‑7 dans les terminaisons nerveuses où la synthèse protéique locale et la libération de neurotransmetteur sont contrôlées.
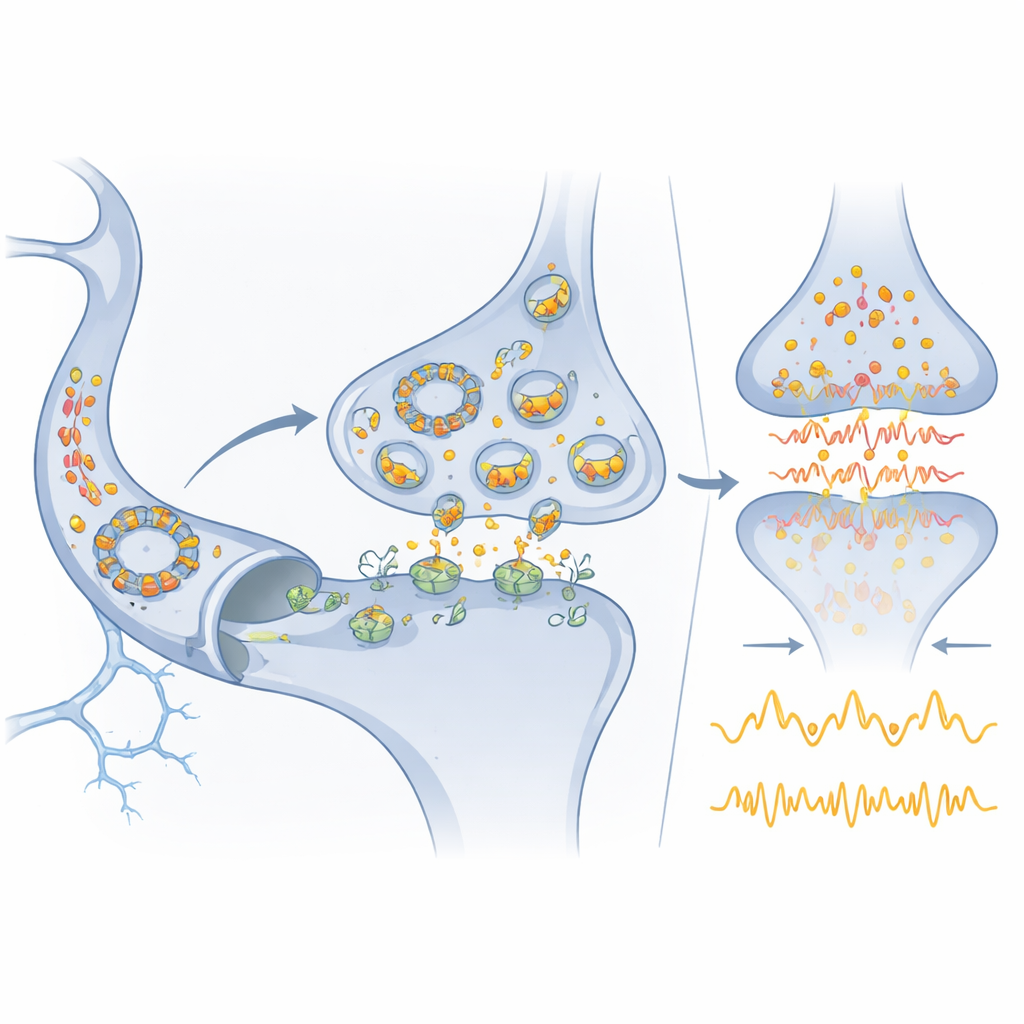
Du circuit moléculaire à la médecine
Parce que Cdr1as est si enrichi dans le cerveau tout en étant assez stable pour être détecté dans le sang, il pourrait servir de marqueur pratique de l’état cérébral dans les maladies neurologiques et psychiatriques. miR‑7, déjà détecté dans divers fluides corporels, pourrait de même aider à suivre ou à modifier des processus pathologiques. Les auteurs décrivent comment des médicaments ou des thérapies à base d’ARN ciblant miR‑7, Cdr1as ou miR‑671 pourraient un jour atténuer les pointes dommageables de glutamate lors d’un AVC ou rééquilibrer des réseaux mal synchronisés dans les troubles de l’humeur et du développement. Ils soulignent toutefois que la plupart des ARN circulaires proposés comme régulateurs manquent probablement de l’abondance exceptionnelle et de la capacité de liaison de Cdr1as. En conséquence, ce système devient une référence : il montre que des circuits composés uniquement d’ARN peuvent rivaliser avec les réseaux protéiques en précision et robustesse, mais aussi que de véritables régulateurs majeurs parmi les ARN circulaires sont probablement rares et doivent être identifiés par des tests rigoureux et quantitatifs.
Citation: Cerda-Jara, C.A., Scoyni, F., Zolotarov, G. et al. The history and function of a circular RNA. Nat Commun 17, 3862 (2026). https://doi.org/10.1038/s41467-026-71822-0
Mots-clés: ARN circulaire, microARN-7, stress neuronal, signalisation glutamatergique, biomarqueurs ARN