Clear Sky Science · tr
Dairesel bir RNA’nın tarihçesi ve işlevi
Ufak RNA halkaları stres altındaki beyinlere nasıl yardımcı oluyor
Uykusuz, yaralı veya duygusal olarak bunalmış olduğumuzda, beyin hücreleri hayatta kalmak ve devrelerin işlevini sürdürmek için etkinliklerini hızla ayarlamak zorundadır. Bu makale, beyindeki alışılmadık bir molekül olan Cdr1as adlı dairesel bir RNA parçasını tanımlıyor ve bunun diğer küçük RNA’larla birlikte stres altında sinir hücresi iletişimini nasıl ince ayarladığı gösteriliyor. Bu gizli kontrol sisteminin anlaşılması, inme, depresyon ve diğer beyin bozukluklarının tedavisi için yeni yollar açabilir — hatta uzaktan beyin sağlığını bildiren kan testleri geliştirebilir.
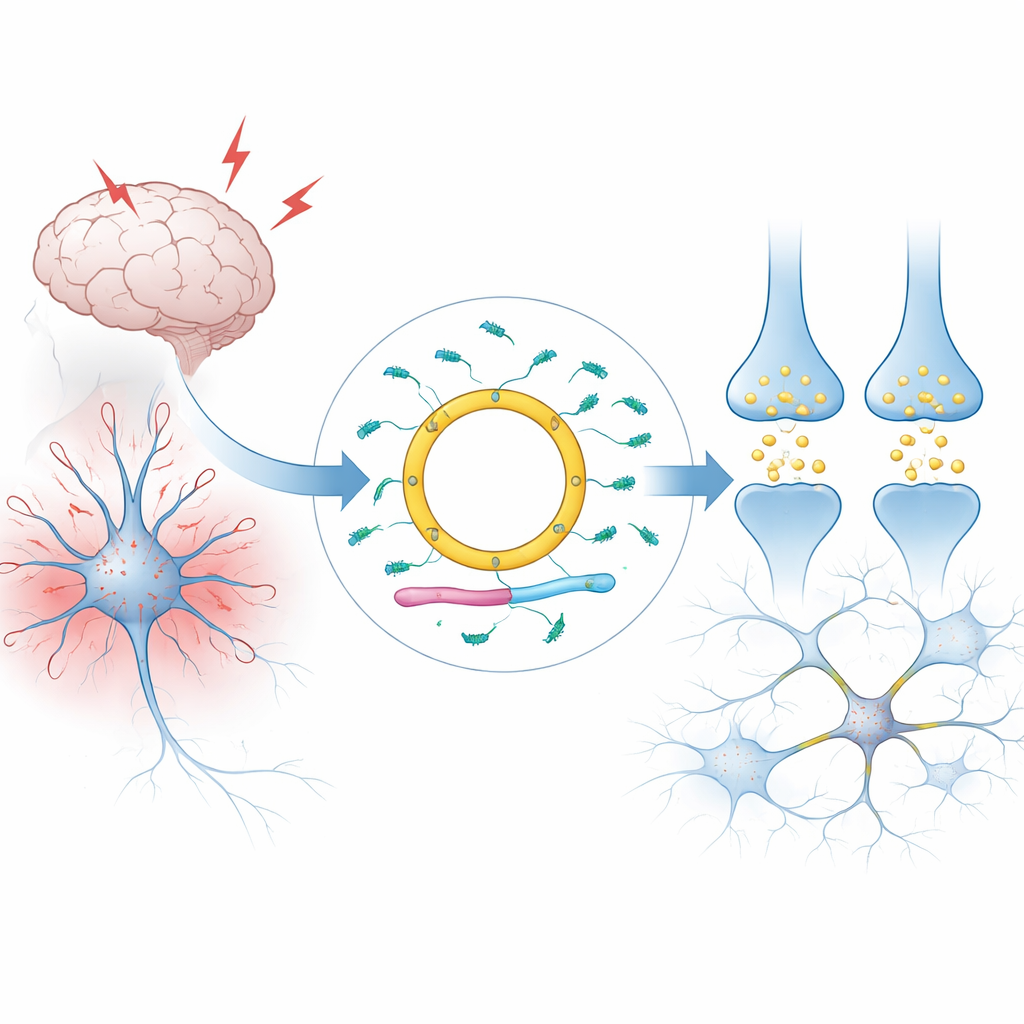
Beyin hücrelerinde dairesel bir mesaj
Hücrelerimizdeki RNA’ların çoğu lineerdir: iki ucu vardır ve hızla parçalanırlar. Cdr1as farklıdır. Kapalı bir döngü oluşturur, bu da onu alışılmadık derecede kararlı kılar ve memelilerin beyinlerinde, özellikle belirli nöron türlerinde çok yüksek düzeylerde birikmesine izin verir. Yazarlar, Cdr1as’ın X kromozomundaki daha büyük bir RNA biriminden uçlarının birbirine eklenmesiyle nasıl üretildiğini açıklar. İnsanlarda ve farelerde bu lokustan elde edilen neredeyse tüm RNA dairesel forma dönüştürülür; geriye neredeyse hiç lineer versiyon kalmaz. Doku ve tek hücreli geniş taramalar, pratik açıdan Cdr1as’ın diğer organlarda ve glia gibi destekleyici beyin hücrelerinde nadir olan, nöronlara özgü bir molekül olduğunu gösterir.
Yoğun bir küçük düzenleyiciler ağı
Cdr1as önemini beraberinde tuttuğu ortaklardan alır. Dairesel dizisi, miR‑7 adı verilen küçük düzenleyici bir RNA için olağanüstü sayıda bağlanma bölgesi taşır — insanlarda yaklaşık yetmiş, farelerde ise yaklaşık 130. miR‑7, birçok protein kodlayan mesajı aynı anda susturan ve Nobel ile tanınan microRNA ailesine aittir. Nöronlarda miR‑7, stres tepkileri ve kimyasal iletici glutamatın salınımıyla ilgili mesajları hedef alır. Cdr1as canlı beyin dokusunda miR‑7’ye bağlanır; bu durum miR‑7’nin ne kadar süre yaşadığına, nöron içinde nerede bulunduğuna ve birçok hedefi üzerinde ne kadar güçlü etki edebileceğine etki eder. İkinci bir küçük RNA olan miR‑671, Cdr1as’ı kesip yok edebilirken, Cyrano adlı uzun bir RNA aktif olarak miR‑7’nin parçalanmasını sağlar. Birlikte, bu üç kodlamayan RNA ve iki microRNA sıkı bağlantılı bir devre oluşturur.
Basınç altında sinir etkinliğini dengede tutmak
Yazarlar, bu devrenin bireysel parçalarından yoksun fare modellerini kullanarak, on yıllık çalışmayı özetleyip bunun beyin işlevini nasıl şekillendirdiğini gösterir. Cdr1as’ın kaldırılması, olgun miR‑7 düzeylerini azaltır ve normalde etkinlik ve strese yanıt veren “hemen erken” genlerin ifadesini bozar. Cdr1as’sız nöronlar daha düzensiz, aşırı uyarılabilir şekilde ateşlenir ve fareler duyusal uyaranlara farklı tepkiler gösterir. Buna karşılık Cyrano’nun kaldırılması miR‑7’de güçlü bir birikime yol açar; bu da Cdr1as’ın birikmesini engelleyerek bir geri besleme döngüsünü ortaya koyar. Nöron kültürlerinde ve canlı farelerde inme benzeri koşulları taklit eden deneyler, Cdr1as, miR‑7 ve Cyrano düzeylerinin zaman içinde koordineli bir şekilde değiştiğini gösterir. Bu değişimler sinapslardaki glutamat salınımını değiştirir; bu da nöronların ne kadar iyi hayatta kaldığını ve ağların yaralanma sonrası nasıl toparlandığını etkiler.
İnce kontrol için evrimsel bir ek
Derleme aynı zamanda bu devreyi evrimsel bağlama yerleştirir. miR‑7, merkezi sinir sistemleri gelişmiş ilk hayvanlarla birlikte ortaya çıkan eski bir moleküldür ve PAX6 gibi ana düzenleyicilerin yönlendirdiği erken gelişim kararlarını kontrol etmeye yardımcı olduğu için derinlemesine korunmuştur. Buna karşın Cyrano daha sonra omurgalılarda, miR‑671 ise ilkel plasentası olan memelilerde daha sonra ortaya çıkmış; Cdr1as ise yalnızca plasentalı memelilerde görülür. Yazarlar, bu daha yeni RNA’ların, salgı ve stres tepkilerinin uzmanlaşmış beyin ve hormon salgılayan hücrelerde nasıl ayarlandığını iyileştirmek için eski miR‑7 sisteminin üzerine kademeli olarak eklendiğini savunur. Cdr1as’ın, miR‑7’yi yerel protein sentezi ve iletici salınımının kontrol edildiği sinir uçlarına taşıyan bir taşıyıcı olarak görev yapabileceğini öne sürerler.
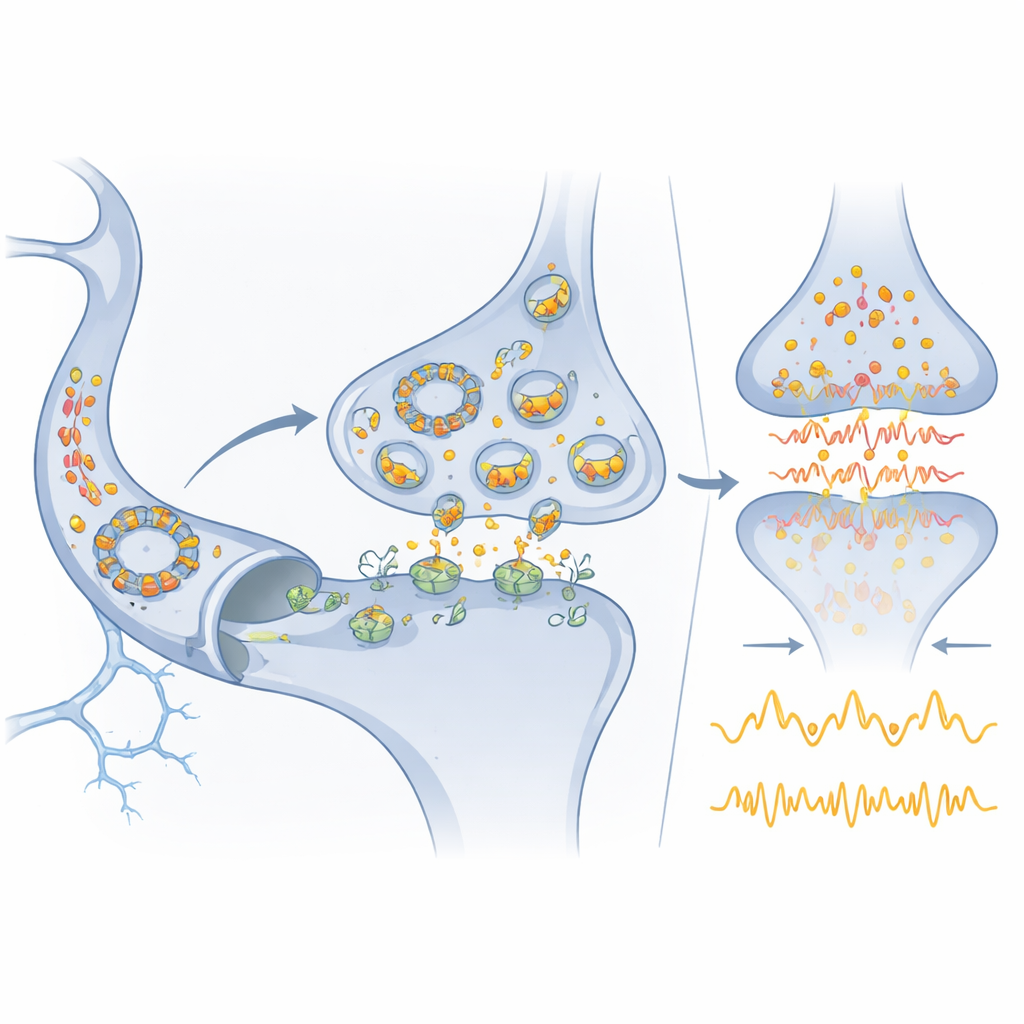
Moleküler devreden tıbba
Cdr1as beyin açısından çok zengin olmasına rağmen kandaki varlığı tespit edilebilecek kadar kararlı olduğu için, nörolojik ve psikiyatrik hastalıklarda beyin durumunun uygun bir göstergesi olarak kullanılabilir. Çeşitli vücut sıvılarında zaten bulunan miR‑7 benzer şekilde hastalık süreçlerini izlemeye veya değiştirmeye yardımcı olabilir. Yazarlar, miR‑7, Cdr1as veya miR‑671’ye yönelik ilaçlar veya RNA‑temelli terapilerin bir gün inmelerde zararlı glutamat patlamalarını hafifletebileceğini veya duygu ve gelişimsel bozukluklardaki yanlış ateşlenen ağları dengeleyebileceğini özetler. Aynı zamanda, önerilen dairesel RNA düzenleyicilerinin çoğunun muhtemelen Cdr1as’ın sahip olduğu istisnai bolluk ve bağlanma kapasitesinden yoksun olacağı konusunda uyarırlar. Sonuç olarak bu sistem bir kıstas görevi görür: RNA‑yalnız devrelerin protein ağlarıyla hassasiyet ve dayanıklılık bakımından yarışabileceğini gösterir, ancak dairesel RNA’lar arasında gerçek düzenleyici ağır topların muhtemelen nadir olduğunu ve titiz, nicel testlerle tanımlanmaları gerektiğini de belirtir.
Atıf: Cerda-Jara, C.A., Scoyni, F., Zolotarov, G. et al. The history and function of a circular RNA. Nat Commun 17, 3862 (2026). https://doi.org/10.1038/s41467-026-71822-0
Anahtar kelimeler: dairesel RNA, microRNA-7, nöronal stres, glutamaterjik sinyalizasyon, RNA biyobelirteçleri