Clear Sky Science · pt
A história e a função de um RNA circular
Como pequenos laços de RNA ajudam cérebros estressados a lidar com a situação
Quando estamos privados de sono, lesionados ou emocionalmente sobrecarregados, as células cerebrais precisam ajustar rapidamente sua atividade para sobreviver e manter os circuitos funcionando. Este artigo descreve uma molécula incomum no cérebro, um pedaço circular de RNA chamado Cdr1as, e mostra como ela atua em conjunto com outros pequenos RNAs para ajustar finamente a comunicação entre neurônios sob estresse. Entender esse sistema de controle oculto pode abrir novos caminhos para tratar AVC, depressão e outros distúrbios cerebrais — e pode até gerar exames de sangue que informem sobre a saúde do cérebro à distância.
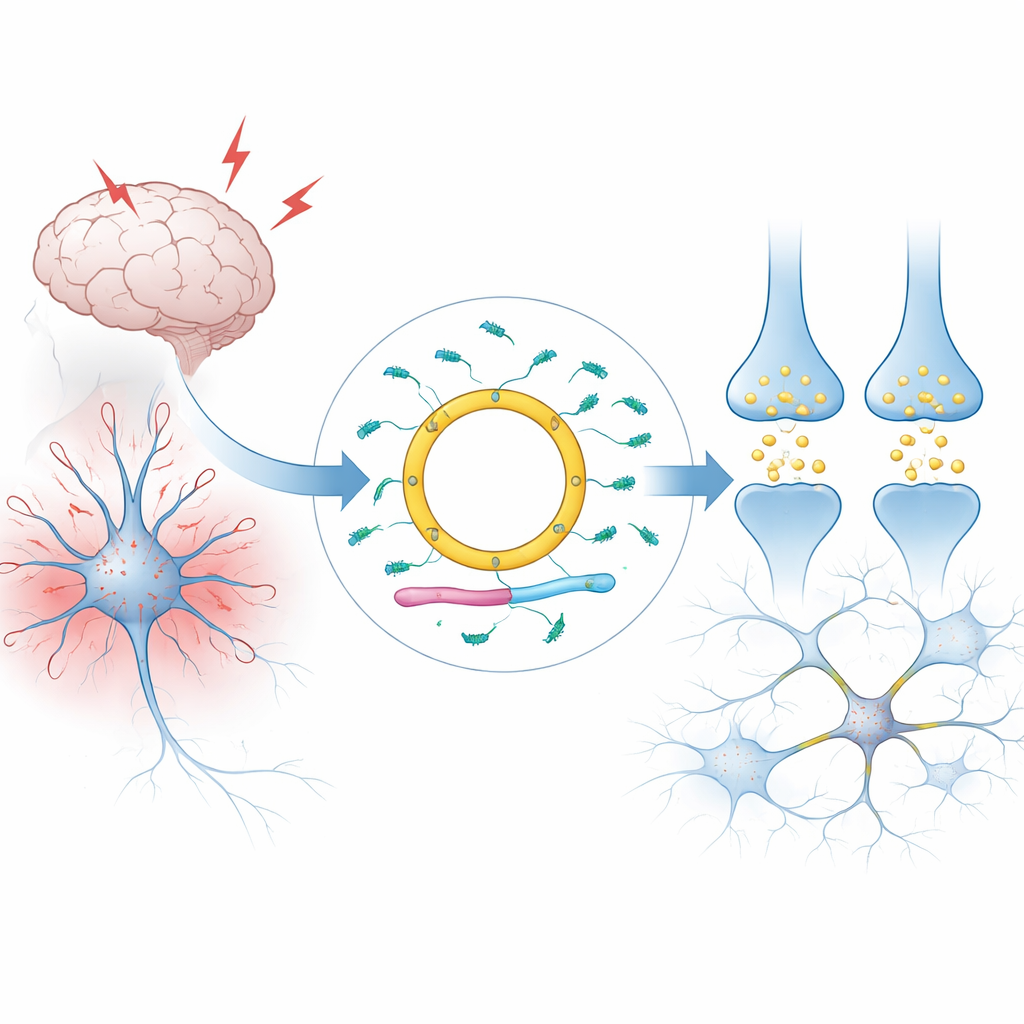
Uma mensagem circular nas células do cérebro
A maioria dos RNAs em nossas células é linear: têm duas extremidades e são rapidamente degradados. Cdr1as é diferente. Ele forma um laço fechado, tornando‑se incomumente estável e permitindo que se acumule em níveis muito altos em cérebros de mamíferos, especialmente em tipos específicos de neurônios. Os autores explicam como Cdr1as é produzido a partir de uma unidade de RNA maior no cromossomo X por um processo que emenda suas extremidades. Em humanos e camundongos, quase todo o RNA desse locus é convertido na forma circular, com muito pouco restante na versão linear. Grandes levantamentos de tecidos e de células individuais mostram que Cdr1as é, na prática, uma molécula específica de neurônios, rara em outros órgãos e em células de suporte do cérebro, como a glia.
Uma teia densa de pequenos reguladores
Cdr1as ganha importância pela companhia que mantém. Sua sequência circular carrega um número excepcional de sítios de ancoragem para um pequeno RNA regulador chamado miR‑7 — cerca de setenta em humanos e cerca de 130 em camundongos. miR‑7 pertence à célebre família dos microRNAs, moléculas recentemente reconhecidas com o Nobel que silenciam muitas mensagens codificadoras de proteínas de uma só vez. Em neurônios, miR‑7 tem como alvos mensagens envolvidas em respostas ao estresse e na liberação do neurotransmissor glutamato. Cdr1as se liga a miR‑7 em tecido cerebral vivo, afetando quanto tempo miR‑7 sobrevive, onde ele se localiza dentro do neurônio e com que intensidade pode agir sobre seus muitos alvos. Um segundo pequeno RNA, miR‑671, pode cortar e destruir Cdr1as, enquanto um RNA longo chamado Cyrano provoca a degradação ativa do próprio miR‑7. Juntos, esses três RNAs não codificadores e dois microRNAs formam um circuito fortemente conectado.
Manter o equilíbrio da atividade nervosa sob pressão
Usando modelos de camundongo que carecem de peças individuais desse circuito, os autores resumem uma década de trabalho mostrando como ele molda a função cerebral. Remover Cdr1as reduz os níveis de miR‑7 maduro e perturba a expressão de genes “imediatos‑iniciais” que normalmente respondem à atividade e ao estresse. Neurônios sem Cdr1as disparam de forma mais errática, excessivamente excitável, e os camundongos apresentam reações alteradas a sinais sensoriais. Em contraste, remover Cyrano leva a um forte acúmulo de miR‑7, que por sua vez impede o acúmulo de Cdr1as, revelando um loop de retroalimentação. Experimentos que mimetizam condições semelhantes a AVC em culturas de neurônios e em camundongos vivos demonstram que os níveis de Cdr1as, miR‑7 e Cyrano mudam de forma coordenada e dependente do tempo. Essas mudanças alteram a liberação de glutamato nas sinapses, influenciando quão bem os neurônios sobrevivem e como as redes se recuperam após lesão.
Um acréscimo evolutivo para controle fino
A revisão também coloca esse circuito no contexto evolutivo. miR‑7 é antigo, aparecendo com os primeiros animais que desenvolveram sistemas nervosos centralizados, e é profundamente conservado porque ajuda a controlar decisões iniciais do desenvolvimento, como aquelas guiadas pelo regulador mestre PAX6. Em contraste, Cyrano surgiu mais tarde nos vertebrados, miR‑671 ainda mais tarde em mamíferos com placentas primitivas, e Cdr1as apenas em mamíferos placentários. Os autores argumentam que esses RNAs mais novos foram gradualmente empilhados sobre o sistema mais antigo de miR‑7 para refinar como a secreção e as respostas ao estresse são ajustadas em células cerebrais especializadas e em células secretoras de hormônios. Eles propõem que Cdr1as pode agir como um transportador, levando miR‑7 para as terminações nervosas onde a síntese protéica local e a liberação de neurotransmissor são controladas.
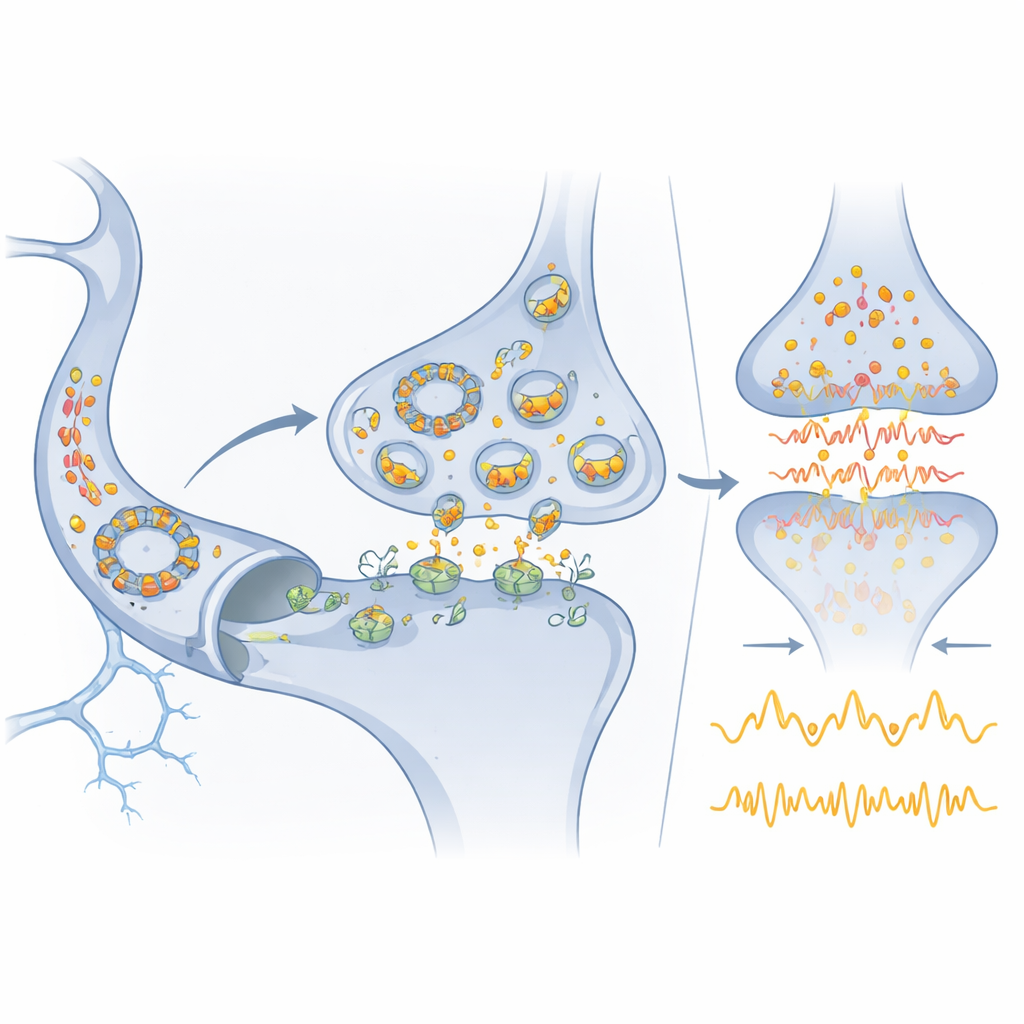
Do circuito molecular à medicina
Porque Cdr1as é tão enriquecido no cérebro e ainda estável o bastante para ser detectado no sangue, ele poderia servir como um marcador conveniente do estado cerebral em doenças neurológicas e psiquiátricas. miR‑7, já encontrado em vários fluidos corporais, pode igualmente ajudar a rastrear ou modificar processos da doença. Os autores delineiam como drogas ou terapias baseadas em RNA direcionadas a miR‑7, Cdr1as ou miR‑671 podem um dia atenuar surtos prejudiciais de glutamato em AVC ou reequilibrar redes com disparos erráticos em transtornos de humor e do desenvolvimento. Ao mesmo tempo, alertam que a maioria dos reguladores propostos entre os RNAs circulares provavelmente não tem a abundância excepcional e a capacidade de ligação de Cdr1as. Como resultado, esse sistema torna‑se um ponto de referência: mostra que circuitos formados apenas por RNA podem rivalizar com redes de proteínas em precisão e robustez, mas também que verdadeiros pesos‑pesados regulatórios entre os RNAs circulares são provavelmente raros e devem ser identificados com testes rigorosos e quantitativos.
Citação: Cerda-Jara, C.A., Scoyni, F., Zolotarov, G. et al. The history and function of a circular RNA. Nat Commun 17, 3862 (2026). https://doi.org/10.1038/s41467-026-71822-0
Palavras-chave: RNA circular, microRNA-7, estresse neuronal, sinalização glutamatérgica, biomarcadores de RNA