Clear Sky Science · it
La storia e la funzione di un RNA circolare
Come piccoli anelli di RNA aiutano i cervelli sotto stress
Quando siamo privati del sonno, feriti o emotivamente sopraffatti, le cellule cerebrali devono regolare rapidamente la loro attività per sopravvivere e mantenere il funzionamento dei circuiti. Questo articolo descrive una molecola insolita nel cervello, un frammento circolare di RNA chiamato Cdr1as, e mostra come lavori insieme ad altri piccoli RNA per modulare finemente la comunicazione neuronale sotto stress. Comprendere questo sistema di controllo nascosto potrebbe aprire nuove strade per trattare ictus, depressione e altri disturbi cerebrali — e potrebbe perfino portare a esami del sangue in grado di informare sullo stato del cervello a distanza.
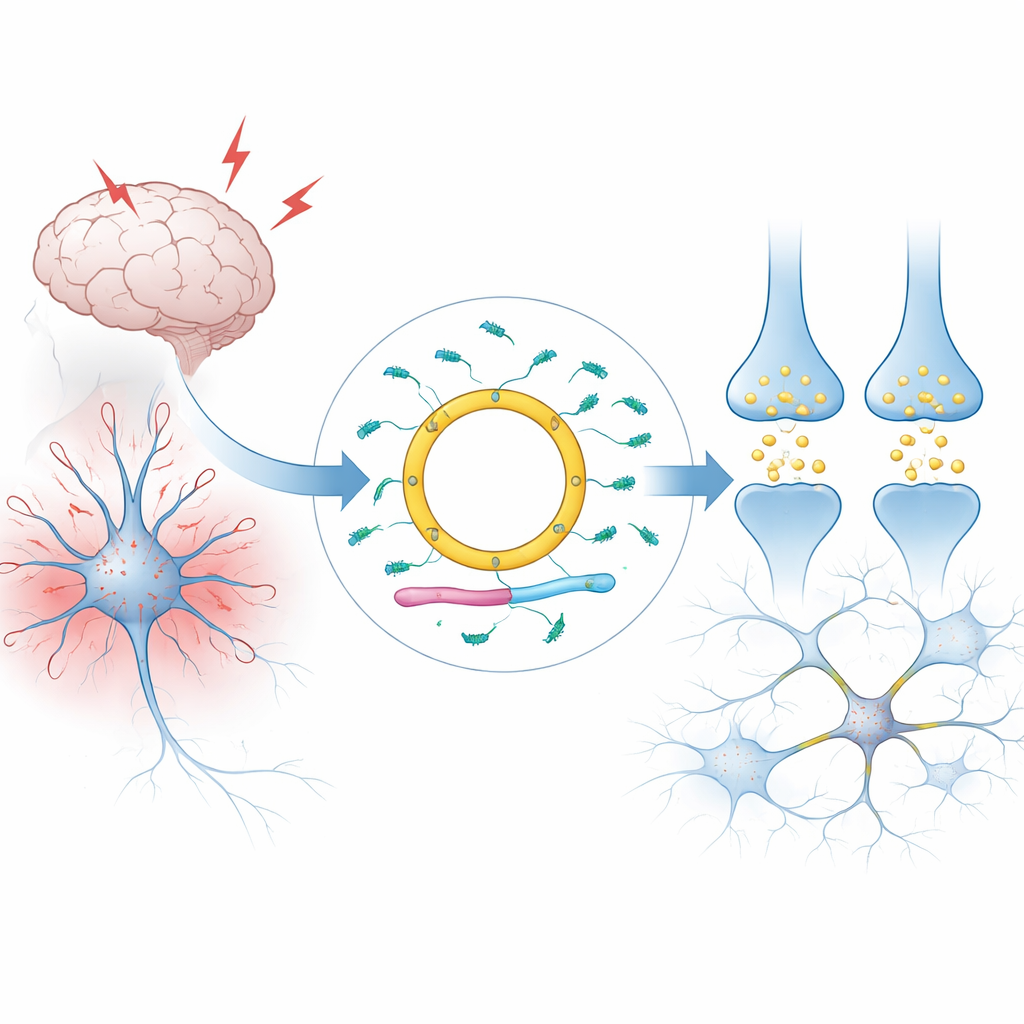
Un messaggio circolare nelle cellule cerebrali
La maggior parte degli RNA nelle nostre cellule è lineare: ha due estremità ed è rapidamente degradata. Cdr1as è diverso. Forma un anello chiuso, che lo rende insolitamente stabile e gli consente di accumularsi a livelli molto elevati nei cervelli dei mammiferi, specialmente in tipi neuronali specifici. Gli autori spiegano come Cdr1as venga prodotto da un’unità di RNA più grande sul cromosoma X tramite un processo che unisce le sue estremità. Nell’uomo e nel topo, quasi tutto l’RNA proveniente da questo locus viene convertito nella forma circolare, con pochissima versione lineare residua. Ampie analisi di tessuti e cellule singole mostrano che Cdr1as è, a tutti gli effetti, una molecola specifica dei neuroni, scarsa in altri organi e nelle cellule di supporto cerebrale come la glia.
Una fitta rete di minuscoli regolatori
L’importanza di Cdr1as deriva dalla compagnia che tiene. La sua sequenza circolare porta un numero eccezionale di siti di ancoraggio per un piccolo RNA regolatorio chiamato miR‑7 — circa settanta nell’uomo e circa 130 nel topo. miR‑7 appartiene alla nota famiglia dei microRNA, molecole di recente riconoscimento Nobel che silenziano contemporaneamente molti messaggi codificanti proteine. Nei neuroni, miR‑7 prende di mira messaggi coinvolti nelle risposte allo stress e nel rilascio del neurotrasmettitore glutammato. Cdr1as lega miR‑7 nei tessuti cerebrali vivi, influenzando la durata di vita di miR‑7, la sua localizzazione all’interno del neurone e la forza con cui può agire sui suoi numerosi bersagli. Un secondo piccolo RNA, miR‑671, può tagliare e distruggere Cdr1as, mentre un RNA lungo chiamato Cyrano provoca la degradazione attiva dello stesso miR‑7. Insieme, questi tre RNA non codificanti e due microRNA formano un circuito strettamente connesso.
Mantenere l’equilibrio dell’attività nervosa sotto pressione
Utilizzando modelli murini privi di singoli elementi di questo circuito, gli autori riassumono un decennio di lavori che mostrano come esso modelli la funzione cerebrale. Rimuovere Cdr1as riduce i livelli di miR‑7 maturo e altera l’espressione di geni “immediati” che normalmente rispondono all’attività e allo stress. I neuroni privi di Cdr1as scaricano in modo più erratico e iper‑eccitabile, e i topi mostrano reazioni alterate a stimoli sensoriali. Al contrario, eliminare Cyrano porta a un forte accumulo di miR‑7, che a sua volta impedisce l’accumulo di Cdr1as, rivelando un circuito di retroazione. Esperimenti che imitano condizioni simili all’ictus in piastre di neuroni e in topi vivi dimostrano che i livelli di Cdr1as, miR‑7 e Cyrano cambiano in modo coordinato e dipendente dal tempo. Questi cambiamenti modificano il rilascio di glutammato alle sinapsi, influenzando la sopravvivenza neuronale e la capacità delle reti di recuperare dopo il danno.
Un’aggiunta evolutiva per un controllo fine
La review colloca inoltre questo circuito nel contesto evolutivo. miR‑7 è antico, appare con i primi animali che svilupparono sistemi nervosi centralizzati, ed è profondamente conservato perché aiuta a controllare decisioni di sviluppo precoci, come quelle guidate dal regolatore maestro PAX6. Per contro, Cyrano è comparso più tardi nei vertebrati, miR‑671 ancora più tardi nei mammiferi con placente più evolute, e Cdr1as solo nei mammiferi placentati. Gli autori sostengono che questi RNA più recenti siano stati gradualmente sovrapposti al sistema più antico di miR‑7 per affinare come la secrezione e le risposte allo stress vengono regolate in cellule nervose specializzate e in cellule secernenti ormoni. Propongono che Cdr1as possa agire come un trasportatore, portando miR‑7 nelle terminazioni nervose dove la sintesi proteica locale e il rilascio di neurotrasmettitori sono controllati.
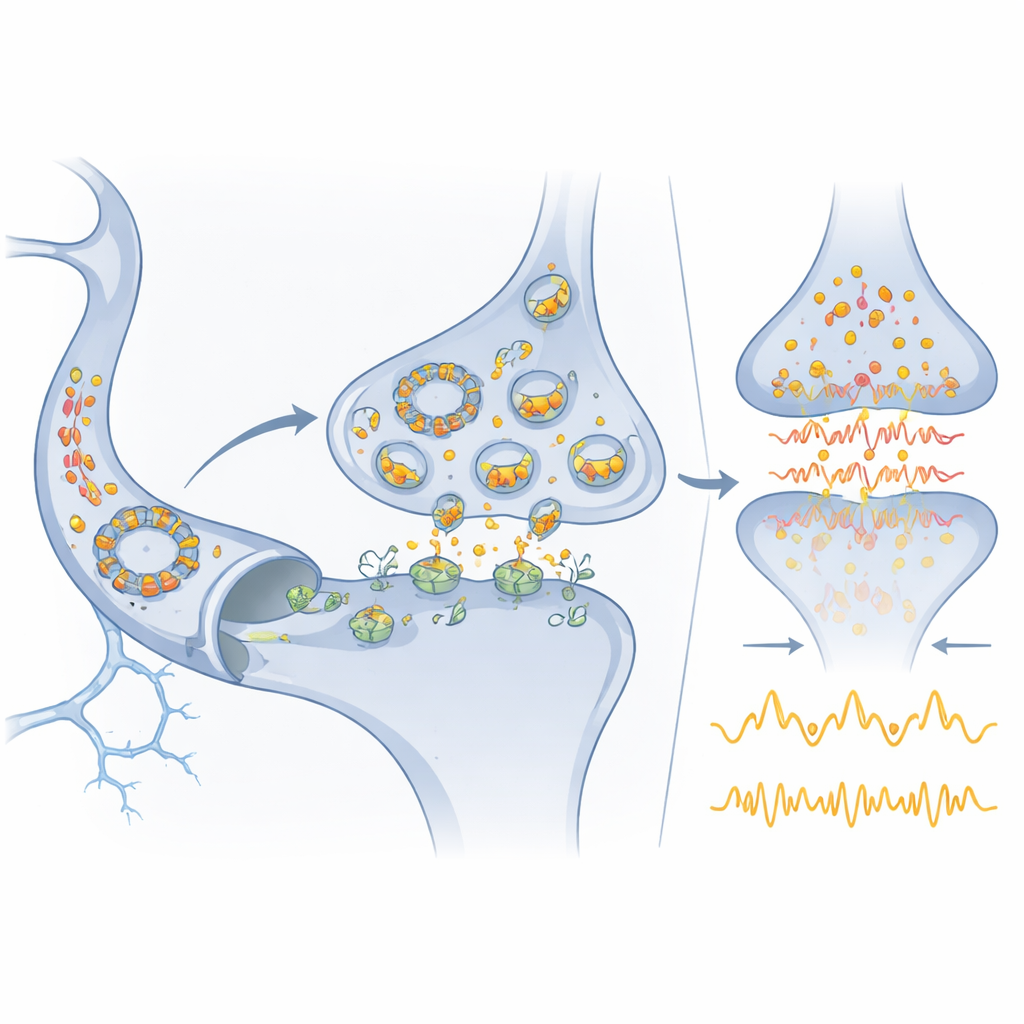
Dal circuito molecolare alla medicina
Poiché Cdr1as è così arricchito nel cervello ma sufficientemente stabile da essere rilevabile nel sangue, potrebbe servire come un marcatore comodo dello stato cerebrale nelle malattie neurologiche e psichiatriche. miR‑7, già rilevato in vari fluidi corporei, potrebbe similmente aiutare a monitorare o modificare i processi patologici. Gli autori delineano come farmaci o terapie a base di RNA mirate a miR‑7, Cdr1as o miR‑671 potrebbero un giorno attenuare i pericolosi picchi di glutammato nell’ictus o riequilibrare reti iperattive nei disturbi dell’umore e dello sviluppo. Allo stesso tempo, avvertono che la maggior parte dei regolatori basati su RNA circolari proposti probabilmente non possiede l’eccezionale abbondanza e capacità di legame di Cdr1as. Di conseguenza, questo sistema diventa un punto di riferimento: dimostra che circuiti composti solo da RNA possono rivaleggiare con le reti proteiche in precisione e robustezza, ma anche che veri e propri punti di forza regolatori tra gli RNA circolari sono probabilmente rari e devono essere identificati con test rigorosi e quantitativi.
Citazione: Cerda-Jara, C.A., Scoyni, F., Zolotarov, G. et al. The history and function of a circular RNA. Nat Commun 17, 3862 (2026). https://doi.org/10.1038/s41467-026-71822-0
Parole chiave: RNA circolare, microRNA-7, stress neuronale, segnalazione glutamatergica, biomarcatori RNA