Clear Sky Science · zh
基于L-RNA适配体抑制CXCL12联合放疗和贝伐单抗治疗新诊断胶质母细胞瘤:I/II期GLORIA试验扩展
这项脑癌研究的重要性
胶质母细胞瘤是最致命的脑癌之一,部分原因在于治疗后肿瘤几乎总会复发。即便外科尽可能切除肿瘤并随后给予放疗,肿瘤的血液供应也会迅速重建,使癌细胞得以恢复。该研究检验了一种新策略:阻断肿瘤重建血管的两条不同途径,并评估在放疗基础上加入这两重抑制是否能在通常预后很差的患者中更长时间地安全控制癌症。
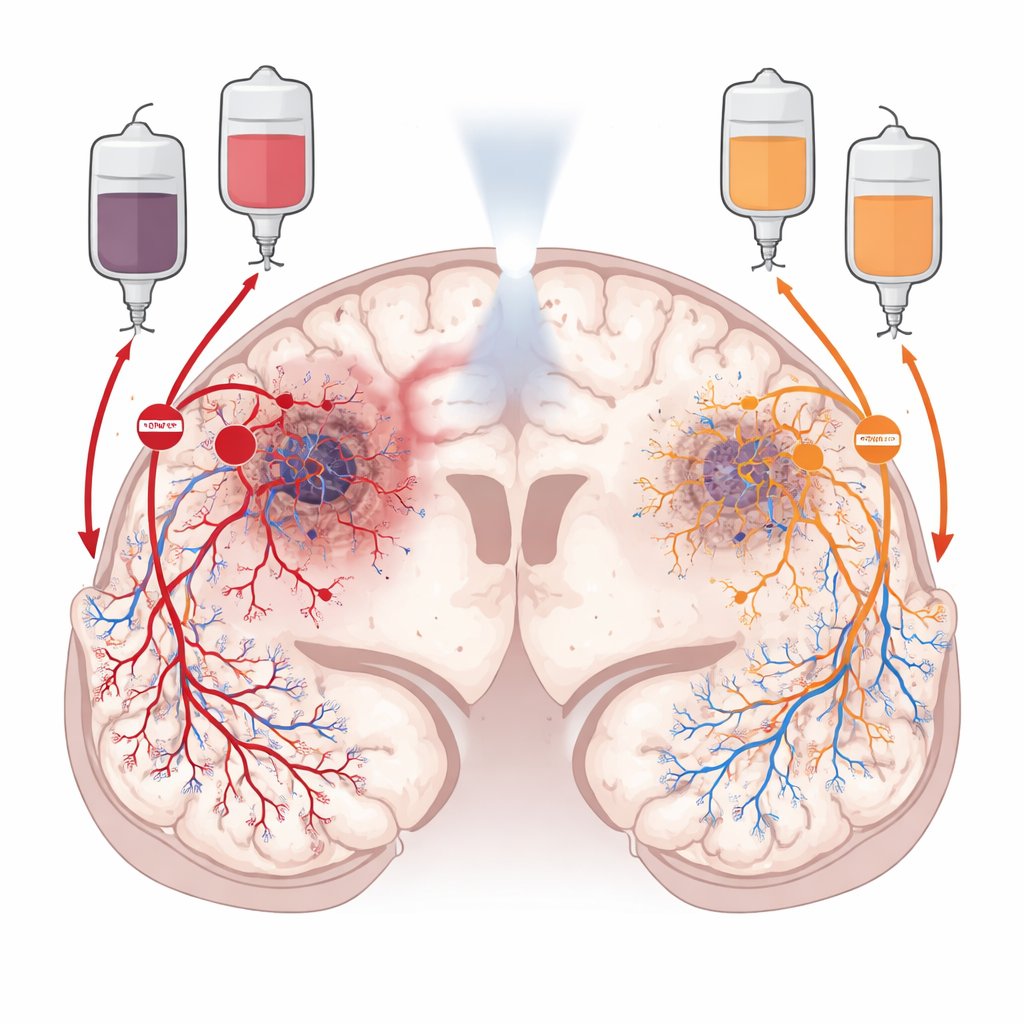
滋养肿瘤的两条隐秘通路
放疗后,胶质母细胞瘤并非静止不动。它会主动重塑周围环境以恢复血流。一条路径称为血管生成(angiogenesis),依赖促使附近血管向肿瘤内分支的新生长信号。另一条称为血管新生(vasculogenesis),通过招募来自骨髓的新血管形成前体细胞,这些细胞定向进入肿瘤并从零构建新血管。研究者关注两个指导这些通路的化学“交通指挥者”:驱动局部血管萌芽的VEGF,以及吸引循环中的前体和免疫细胞并帮助它们在肿瘤中定植的CXCL12。由于这些信号在肿瘤不同区域发挥作用,团队推测同时阻断两者可能比单独阻断任何一种更有效地“饿死”肿瘤。
在人体肿瘤中绘制信号作用位置
为了查看VEGF和CXCL12在胶质母细胞瘤内的分布,科学家们挖掘了大型公共基因数据集,并进一步研究来自真实患者肿瘤的高分辨率图像。他们发现VEGF与肿瘤深处缺氧、坏死区域密切相关,那里的受损组织紧急需要新血管。相比之下,CXCL12主要出现在更细胞丰富且血管化程度高的区域以及肿瘤细胞侵入健康脑组织的外周浸润区。通过先进的染色技术和空间基因谱分析,他们显示CXCL12不仅由肿瘤细胞产生,还由血管内皮、支持细胞以及肿瘤内外的免疫细胞(包括正常脑血管)产生。这进一步支持了VEGF和CXCL12作为互补且不重叠的血管重建驱动因子的观点。
一项将放疗与CXCL12捕捉剂和抗VEGF治疗相结合的试验
基于先前使用一种阻断CXCL12的药物NOX-A12的工作,GLORIA试验招募了新诊断且肿瘤无法完全切除、同时缺乏使标准化疗有效的DNA标志的成年胶质母细胞瘤患者。所有患者均接受放疗并持续静脉注射NOX-A12。在扩展阶段,6名患者中的一部分还接受了贝伐单抗——一种靶向VEGF的抗体,已在复发性胶质母细胞瘤中使用。主要目标是评估安全性;研究团队还跟踪了肿瘤受控时间、总体生存期、MRI上肿瘤血流变化,以及患者的神经功能和生活质量。
安全性及更强更持久反应的迹象
放疗、NOX-A12和贝伐单抗的三联组合耐受性良好。无与治疗相关的死亡,也无剂量限制性毒性。大多数不良事件为轻至中度,主要与肿瘤本身或放疗相关;贝伐单抗引起的血压升高可通过药物控制。影像学显示,加入贝伐单抗后肿瘤血容量和灌注显著下降,提示血管再生受到强烈抑制。在临床上,接受三联治疗的患者中位无进展期约略超过九个月,中位总生存期接近20个月——这两项指标均明显优于仅接受放疗加NOX-A12的患者,也优于与之精心匹配的标准治疗组。值得注意的是,接受三联治疗的6名患者中有2名生存超过两年,这对于该高风险人群来说是异常长的时间。
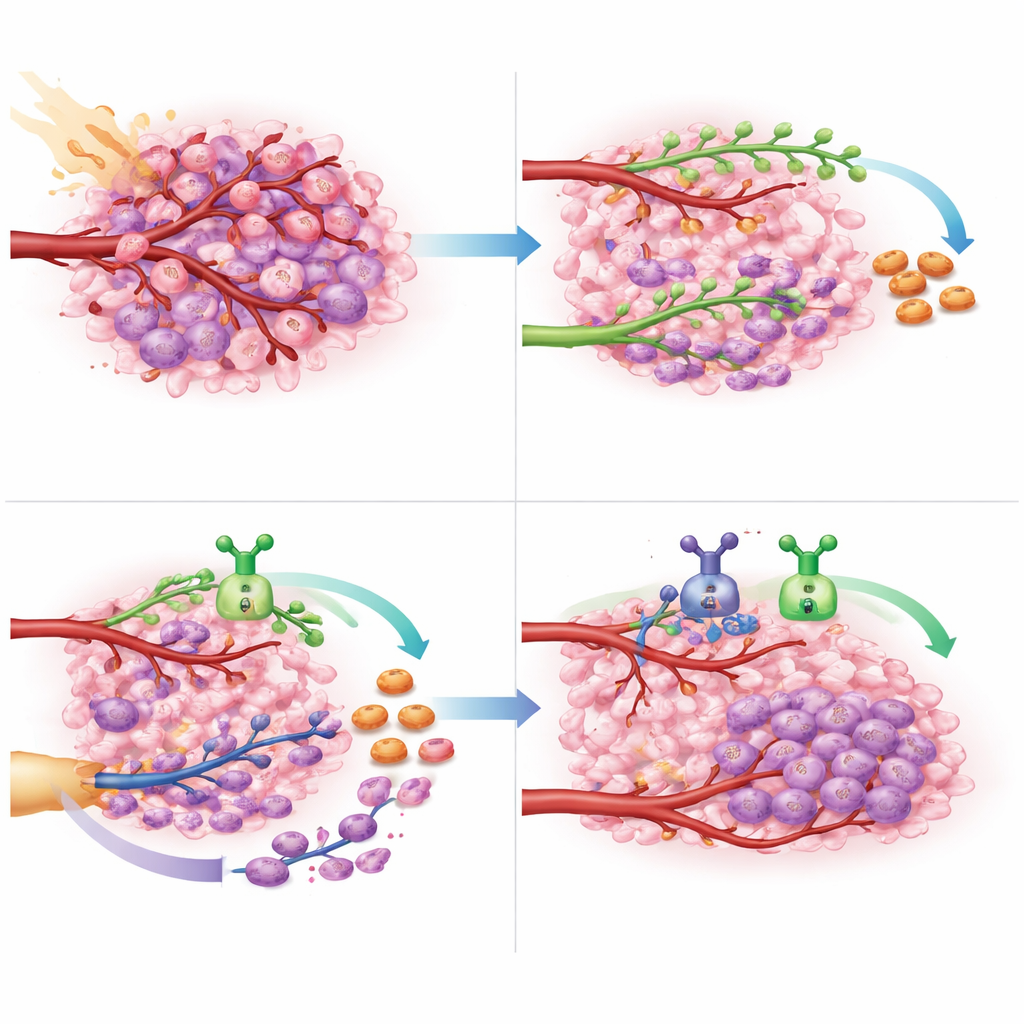
这对未来脑癌护理可能意味着什么
对于无法完全切除且对标准化疗耐药的胶质母细胞瘤患者,选择有限且预后悲观。本研究提供了原理性证明:在放疗期间及之后同时关闭两条主要的血管修复途径——VEGF驱动的萌芽和CXCL12驱动的新血管形成细胞招募——可以安全实施,并可能显著延缓肿瘤重建。尽管该试验规模较小且主要设计用于评估安全性,但生存获益足够令人鼓舞,值得开展更大规模、随机的研究以验证。如果得到证实,同时靶向这两种血管信号可能成为延长控制这种侵袭性脑癌的新一线策略。
引用: Giordano, F.A., Layer, J.P., Turiello, R. et al. L-RNA aptamer-based CXCL12 inhibition combined with radiotherapy and bevacizumab in newly-diagnosed glioblastoma: expansion of the phase I/II GLORIA trial. Nat Commun 17, 3405 (2026). https://doi.org/10.1038/s41467-026-71362-7
关键词: 胶质母细胞瘤, 脑癌, 肿瘤血管, 放疗, 靶向治疗