Clear Sky Science · de
L-RNA-Aptamer-basierte CXCL12-Inhibition kombiniert mit Strahlentherapie und Bevacizumab bei neu diagnostiziertem Glioblastom: Erweiterung der Phase-I/II-GLORIA-Studie
Warum diese Studie zu Hirntumoren wichtig ist
Das Glioblastom zählt zu den tödlichsten Hirntumoren, unter anderem weil es nach einer Behandlung nahezu immer wieder auftritt. Selbst wenn Chirurgen so viel Tumor wie möglich entfernen und anschließend bestrahlt wird, stellt der Tumor seine Blutversorgung schnell wieder her, wodurch sich Krebszellen erholen können. Diese Studie prüfte eine neue Strategie: zwei verschiedene Wege zu blockieren, über die der Tumor seine Blutgefäße regeneriert, und zu untersuchen, ob dieses doppelte Abschalten in Kombination mit Strahlentherapie den Krebs bei Patientinnen und Patienten, die sonst meist sehr schlechte Aussichten haben, länger kontrollieren kann.
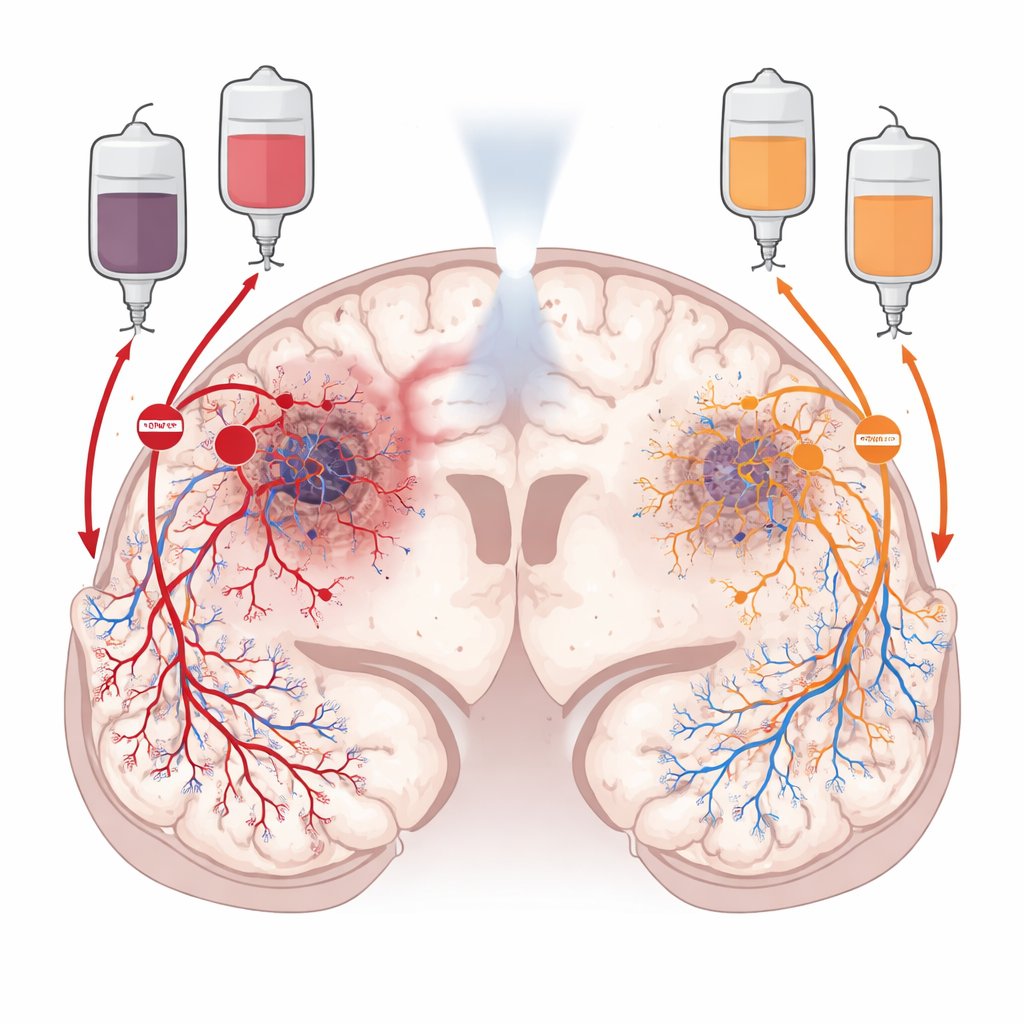
Zwei verborgene Wege, die den Tumor versorgen
Nach der Strahlentherapie ruht das Glioblastom nicht. Es formt aktiv seine Umgebung um, um die Durchblutung wiederherzustellen. Ein Weg, die Angiogenese, beruht auf einem Wachstumssignal, das benachbarte Blutgefäße dazu bringt, neue Äste in den Tumor zu sprießen. Der andere, die Vasculogenese, rekrutiert frische, gefäßbildende Zellen aus dem Knochenmark, die zum Tumor wandern und dort neue Gefäße von Grund auf aufbauen. Die Forschenden konzentrierten sich auf zwei chemische „Verkehrsregler“, die diese Wege steuern: VEGF, das das lokale Gefäßsprossen antreibt, und CXCL12, das zirkulierende Vorläufer- und Immunzellen anzieht und ihnen hilft, sich im Tumor anzusiedeln. Da diese Signale in unterschiedlichen Bereichen des Tumors wirken, gingen die Forschenden davon aus, dass das gleichzeitige Blockieren beider Signalwege den Krebs wirksamer aushungern könnte als die Hemmung eines einzelnen Wegs.
Kartierung, wo die Signale in menschlichen Tumoren wirken
Um zu untersuchen, wie VEGF und CXCL12 in Glioblastomen verteilt sind, werteten die Wissenschaftler große öffentliche Gen-Datensätze aus und betrachteten hochauflösende Bilder realer Patiententumoren. Sie fanden heraus, dass VEGF eng mit sauerstoffarmen, abstirbenden Regionen tief im Tumor korreliert, wo geschädigtes Gewebe dringend neue Gefäße verlangt. CXCL12 hingegen tritt vor allem in den zellreicheren, stark vaskularisierten Zonen und in den äußeren Infiltrationsbereichen auf, in denen Tumorzellen ins gesunde Gehirn einwandern. Mithilfe fortschrittlicher Färbetechniken und räumlicher Genprofilierung zeigten sie, dass CXCL12 nicht nur von Tumorzellen produziert wird, sondern auch von der Gefäßauskleidung, Stütz- und Immunzellen in und um den Tumor, einschließlich normaler Hirngefäße. Das untermauerte die Idee, dass VEGF und CXCL12 komplementäre, nicht überlappende Treiber der Gefäßerneuerung sind.
Eine Studie, die Strahlung mit einer CXCL12-Falle und Anti-VEGF-Therapie kombiniert
Aufbauend auf früheren Arbeiten mit einem CXCL12-blockierenden Wirkstoff namens NOX-A12 schrieb die GLORIA-Studie Erwachsene mit neu diagnostiziertem Glioblastom ein, deren Tumoren nicht vollständig entfernbar waren und die keinen DNA-Marker hatten, der die Standardchemotherapie wirksam macht. Alle Patientinnen und Patienten erhielten Strahlentherapie und eine kontinuierliche intravenöse Gabe von NOX-A12. In einer Erweiterungsphase erhielt eine Untergruppe von sechs Patienten zusätzlich Bevacizumab, einen Antikörper, der VEGF gezielt hemmt und bereits bei rezidivierendem Glioblastom eingesetzt wird. Hauptziel war die Prüfung der Sicherheit; zudem verfolgte das Team die Dauer der Tumorkontrolle, das Gesamtüberleben, Veränderungen der Tumordurchblutung im MRT sowie neurologische Funktion und Lebensqualität der Patienten.
Sicherheit und Hinweise auf stärkere, längere Ansprechraten
Die Dreifachkombination aus Strahlentherapie, NOX-A12 und Bevacizumab erwies sich als gut verträglich. Es gab keine behandlungsbedingten Todesfälle und keine dosislimitierenden toxischen Nebenwirkungen. Die meisten unerwünschten Ereignisse waren leicht bis mäßig und standen weitgehend im Zusammenhang mit dem Tumor oder der Strahlentherapie; Blutdruckanstiege durch Bevacizumab ließen sich medikamentös gut kontrollieren. Bildgebend zeigte sich, dass die Zugabe von Bevacizumab zu deutlich stärkeren Abnahmen von Tumorblutvolumen und Perfusion führte, was darauf hindeutet, dass die Gefäßneubildung stark unterdrückt wurde. Klinisch hatten Patientinnen und Patienten unter der Dreifachtherapie eine mediane progressionsfreie Zeit von knapp über neun Monaten und ein medianes Gesamtüberleben von nahezu 20 Monaten – beides deutlich länger als bei Patientengruppen, die nur Strahlentherapie mit NOX-A12 erhielten, und besser als sorgfältig abgeglichene Gruppen unter Standardtherapie. Bemerkenswert: Zwei der sechs Patienten mit Dreifachtherapie lebten länger als zwei Jahre, eine für diese Hochrisikogruppe ungewöhnlich lange Zeit.
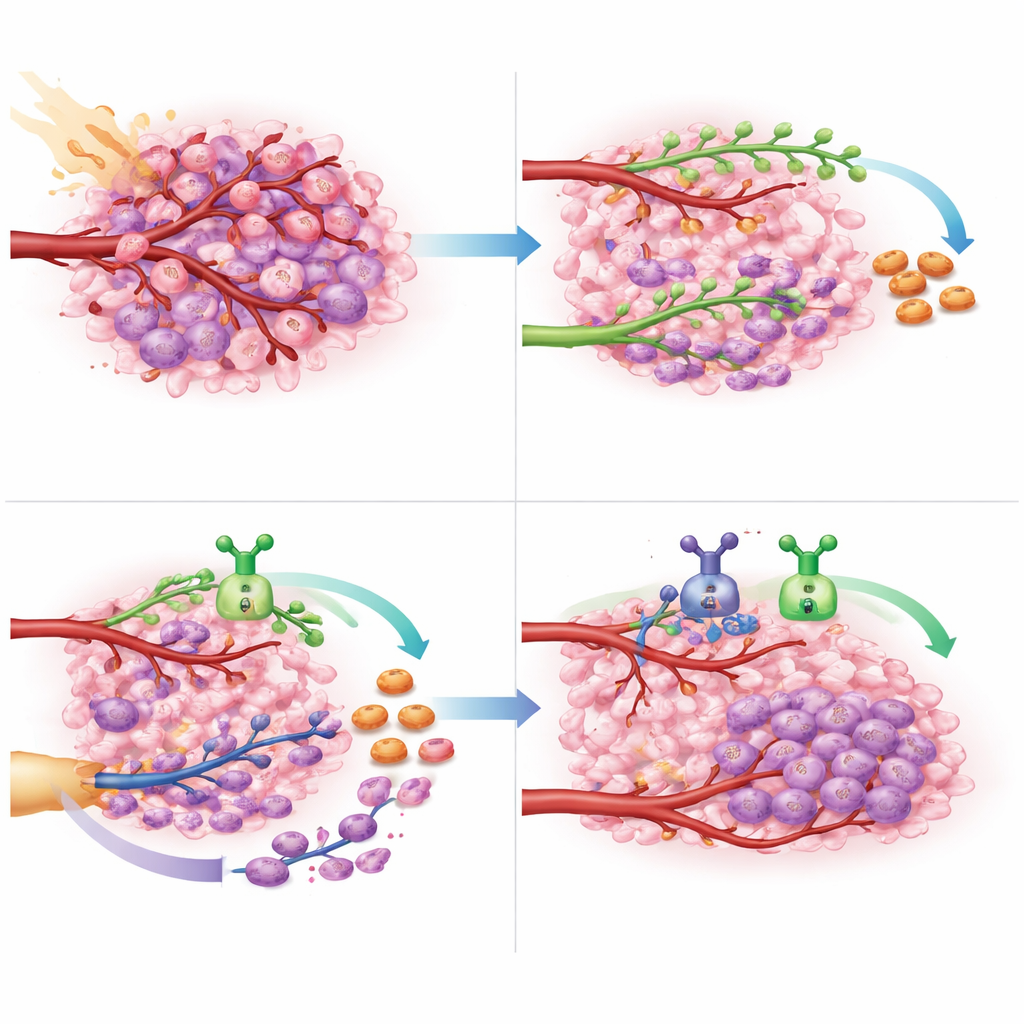
Was das für die zukünftige Behandlung von Hirntumoren bedeuten könnte
Für Patientinnen und Patienten mit einem nicht vollständig entfernbaren Glioblastom, das gegen die Standardchemotherapie resistent ist, sind die Optionen begrenzt und die Prognosen schlecht. Diese Studie liefert einen proof-of-concept, dass das gleichzeitige Abschalten beider wesentlicher Gefäßreparaturwege – VEGF-getriebener Ansatz und CXCL12-vermittelte Rekrutierung gefäßbildender Zellen – während und nach der Strahlentherapie sicher möglich ist und das Nachwachsen des Tumors deutlich verzögern kann. Da die Studie klein war und primär auf die Sicherheitsbewertung ausgelegt, sind die Überlebensvorteile zwar vielversprechend, rechtfertigen aber größere, randomisierte Studien. Bestätigen sich die Ergebnisse, könnte die doppelte Zielgerichtetheit dieser beiden vaskulären Signale zu einer neuen Erstlinienstrategie werden, um dieses aggressive Hirnkarzinom länger in Schach zu halten.
Zitation: Giordano, F.A., Layer, J.P., Turiello, R. et al. L-RNA aptamer-based CXCL12 inhibition combined with radiotherapy and bevacizumab in newly-diagnosed glioblastoma: expansion of the phase I/II GLORIA trial. Nat Commun 17, 3405 (2026). https://doi.org/10.1038/s41467-026-71362-7
Schlüsselwörter: Glioblastom, Hirntumor, Tumorblutgefäße, Strahlentherapie, zielgerichtete Therapie