Clear Sky Science · nl
L-RNA-aptameer-gebaseerde CXCL12-remming gecombineerd met radiotherapie en bevacizumab bij nieuw gediagnosticeerde glioblastoom: uitbreiding van de fase I/II GLORIA-studie
Waarom deze studie naar hersenkanker ertoe doet
Glioblastoom is een van de dodelijkste vormen van hersenkanker, deels omdat het bijna altijd terugkeert na behandeling. Zelfs wanneer chirurgen zoveel mogelijk tumor verwijderen en artsen daarop radiotherapie volgen, bouwt de bloedvoorziening van de tumor zich snel weer op, waardoor kankercellen zich kunnen herstellen. Deze studie testte een nieuwe strategie: het blokkeren van twee verschillende routes die de tumor gebruikt om zijn bloedvaten te herstellen, en de vraag of deze dubbele blokkade, toegevoegd aan radiotherapie, de ziekte bij patiënten die doorgaans slecht reageren langer veilig onder controle kan houden.
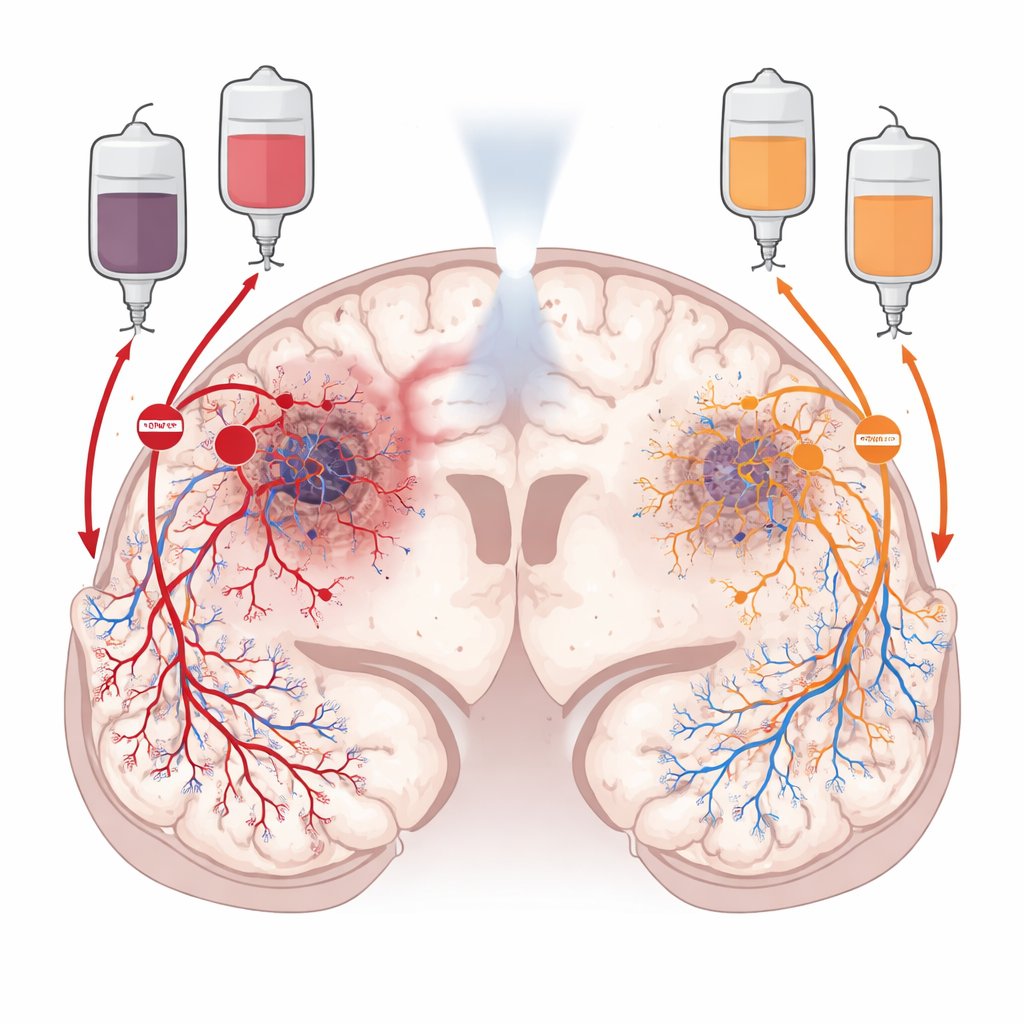
Twee verborgen routes die de tumor voeden
Na radiotherapie blijft glioblastoom niet passief. Het hervormt actief zijn omgeving om de bloedstroom te herstellen. De ene route, angiogenese genoemd, berust op een groeisignaal dat nabije bloedvaten nieuwe vertakkingen laat uitlopen naar de tumor. De andere, vasculogenese genoemd, werft nieuwe bloedvatvormende cellen uit het beenmerg, die naar de tumor migreren en daar van de grond af aan nieuwe vaten opbouwen. De onderzoekers richtten zich op twee chemische "verkeersregelaars" die deze routes sturen: VEGF, dat lokale vatvorming aanjaagt, en CXCL12, dat circulerende voorlopercellen en immuuncellen aantrekt en helpt bij hun vestiging in de tumor. Omdat deze signalen in verschillende delen van de tumor werken, stelden de onderzoekers dat het blokkeren van beide signalen de kanker mogelijk effectiever zou uithongeren dan het blokkeren van slechts één van beide.
In kaart brengen waar de signalen binnen menselijke tumoren werken
Om te zien hoe VEGF en CXCL12 binnen glioblastomen zijn verdeeld, doorzochten de wetenschappers grote openbare genetische datasets en gebruikten ze vervolgens hoge-resolutiebeelden van echte patiëntentumoren. Ze ontdekten dat VEGF sterk samenhangt met lage-zuurstof- en afstervingsregio's diep in de tumor, waar beschadigd weefsel dringend om nieuwe bloedvaten vraagt. CXCL12 daarentegen komt vooral voor in de meer cellulaire en sterk gevasculariseerde zones en in de buitenste infiltratiegebieden waar tumorcellen in gezond hersenweefsel binnendringen. Met geavanceerde kleuringstechnieken en ruimtelijke gengerichte profilering toonden ze aan dat CXCL12 niet alleen door tumorcellen wordt geproduceerd, maar ook door de vaatwand, ondersteunende cellen en immuuncellen in en rond de tumor, inclusief normale hersenvaten. Dit versterkte het idee dat VEGF en CXCL12 complementaire, niet-overlappende drijfveren zijn van bloedvathersteling.
Een studie die radiatie combineert met een CXCL12-val en anti-VEGF-therapie
Bouwend op eerder werk met een CXCL12-blokkerend middel genaamd NOX-A12, schreef de GLORIA-studie volwassenen in met nieuw gediagnosticeerd glioblastoom waarvan de tumoren niet volledig konden worden verwijderd en die een DNA-marker misten waardoor standaardchemotherapie effectief is. Alle patiënten kregen radiotherapie en continue intraveneuze NOX-A12. In een uitbreidingsfase kreeg een subset van zes patiënten daarnaast ook bevacizumab, een antilichaam dat VEGF target en dat al wordt gebruikt bij recidiverend glioblastoom. Het belangrijkste doel was het testen van veiligheid; het team volgde daarnaast hoe lang tumoren onder controle bleven, de totale overleving, veranderingen in tumorbloedstroom op MRI en de neurologische functie en kwaliteit van leven van patiënten.
Veiligheid en aanwijzingen voor sterkere, langere responsen
De drievoudige combinatie van radiotherapie, NOX-A12 en bevacizumab bleek goed verdraagbaar. Er waren geen behandelgerelateerde sterfgevallen en geen dosisbeperkende toxische bijwerkingen. De meeste bijwerkingen waren mild tot matig en grotendeels te relateren aan de tumor of aan de radiatie zelf; bloeddrukstijgingen door bevacizumab waren met medicatie beheersbaar. Beeldvorming toonde dat het toevoegen van bevacizumab leidde tot veel diepere dalingen in tumorbloedvolume en perfusie, wat suggereert dat vatgroei sterk werd onderdrukt. Klinisch hadden patiënten op de drievoudige therapie een mediane periode zonder tumorprogressie van iets meer dan negen maanden en een mediane totale overleving van bijna 20 maanden — beide duidelijk langer dan bij patiënten die alleen radiotherapie met NOX-A12 ontvingen, en beter dan zorgvuldig overeenkomende groepen behandeld met standaardzorg. Opvallend is dat twee van de zes patiënten op de drievoudige therapie langer dan twee jaar leefden, een ongewoon lange tijd voor deze hoogrisicopopulatie.
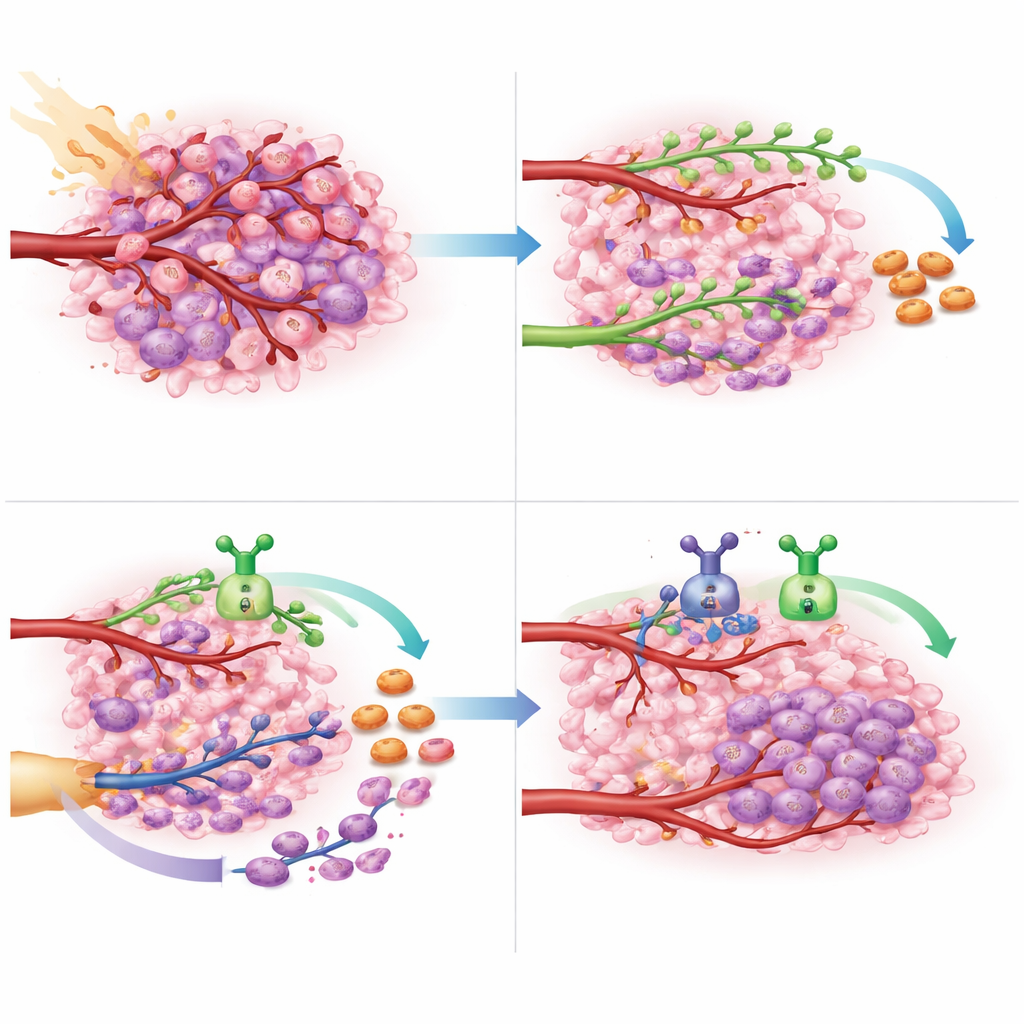
Wat dit zou kunnen betekenen voor toekomstige zorg bij hersenkanker
Voor patiënten met een glioblastoom dat niet volledig kan worden verwijderd en resistent is tegen standaardchemotherapie, zijn de opties schaars en de vooruitzichten somber. Deze studie levert proof-of-principle dat het afsluiten van beide belangrijke routes voor bloedvatreparatie — VEGF-gedreven uitlopers en CXCL12-gedreven werving van nieuwe vatvormende cellen — tijdens en na radiotherapie veilig uitvoerbaar is en de tumorhertgroei aanzienlijk kan vertragen. Hoewel de studie klein was en vooral op veiligheid was gericht, zijn de overlevingswinst en bevindingen bemoedigend genoeg om grotere, gerandomiseerde onderzoeken te rechtvaardigen. Als dit wordt bevestigd, zou het gelijktijdig richten op deze twee vasculaire signalen een nieuwe eerstelijnsstrategie kunnen worden om deze agressieve vorm van hersenkanker langer onder controle te houden.
Bronvermelding: Giordano, F.A., Layer, J.P., Turiello, R. et al. L-RNA aptamer-based CXCL12 inhibition combined with radiotherapy and bevacizumab in newly-diagnosed glioblastoma: expansion of the phase I/II GLORIA trial. Nat Commun 17, 3405 (2026). https://doi.org/10.1038/s41467-026-71362-7
Trefwoorden: glioblastoom, hersenkanker, tumorbloedvaten, radiotherapie, gerichte therapie