Clear Sky Science · tr
L-RNA aptamer tabanlı CXCL12 inhibisyonu ile radyoterapi ve bevacizumabın yeni tanı konmuş glioblastomada birleştirilmesi: Faz I/II GLORIA çalışmasının genişletilmesi
Bu beyin kanseri çalışması neden önemli
Glioblastom, tedavi sonrasında neredeyse her zaman tekrar büyüme gösterdiği için en ölümcül beyin kanserlerinden biridir. Cerrahlar tümörün mümkün olduğunca çok kısmını çıkarsalar ve doktorlar bunu radyoterapi ile izleseler bile tümörün kan desteği hızla yeniden kurularak kanser hücrelerinin toparlanmasına olanak tanır. Bu çalışma yeni bir stratejiyi test etti: tümörün damarlarını yeniden oluşturmak için kullandığı iki farklı yolu engellemek ve bu çiftlü kapatma stratejisinin radyoterapiye eklenince, genellikle kötü prognoza sahip hastalarda kanseri daha uzun süre güvenli şekilde kontrol altında tutup tutamayacağını sorgulamak.
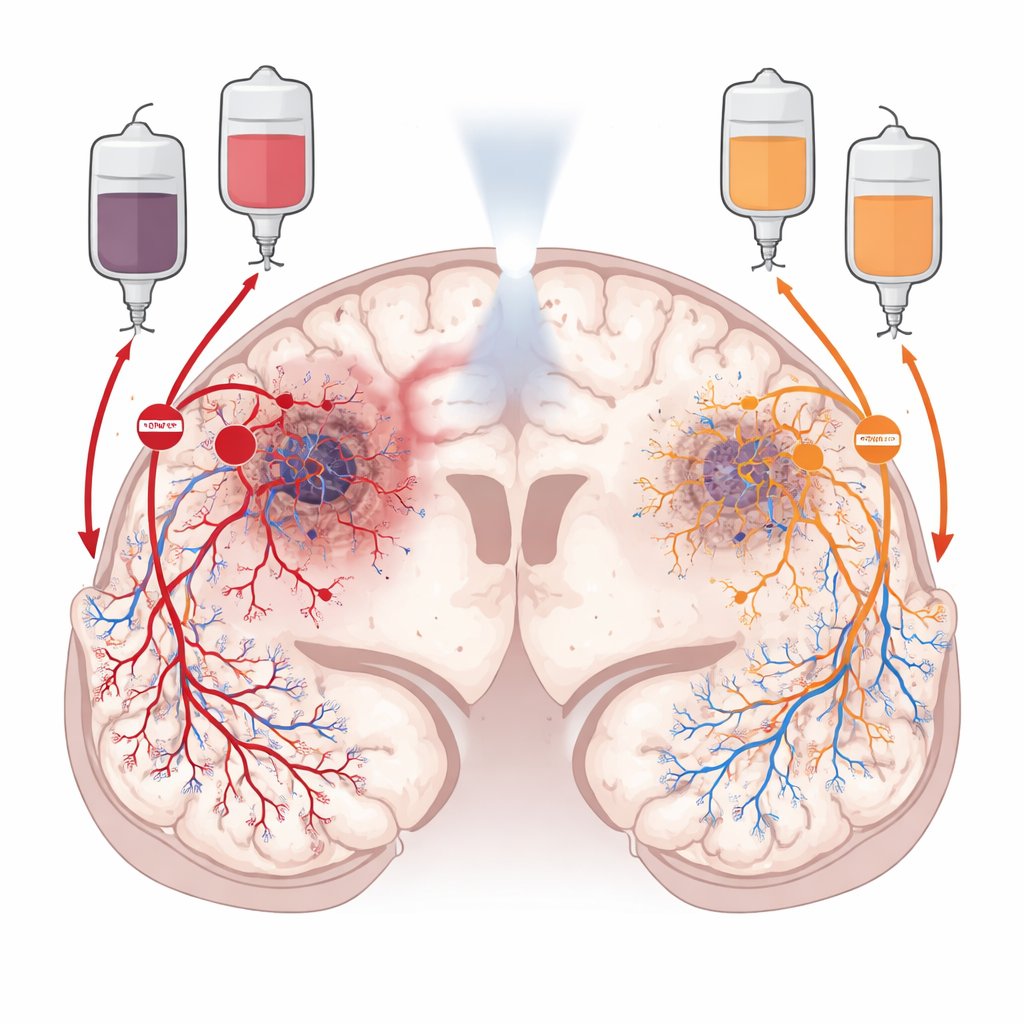
Tümörü besleyen iki gizli yol
Radyoterapiden sonra glioblastom hareketsiz kalmaz. Kan akışını geri getirmek için çevresini aktif olarak yeniden şekillendirir. Bir yol olan anjiyogenez, yakınlardaki kan damarlarının tümöre doğru yeni dallar çıkarmasını sağlayan bir büyüme sinyaline dayanır. Diğer yol olan vazjogenez ise kemik iliğinden yeni damar oluşturan hücreleri devreye sokar; bu hücreler tümöre yönelir ve sıfırdan yeni damarlar kurar. Araştırmacılar bu yolları yönlendiren iki kimyasal "trafik kontrolörü"ne odaklandı: yerel damar budağını teşvik eden VEGF ve dolaşımdaki progenitör ve bağışıklık hücrelerini çeken ve bunların tümör içinde yerleşmesine yardımcı olan CXCL12. Bu sinyaller tümörün farklı bölgelerinde işlediğinden, ekip her ikisini birden bloke etmenin tek başına blokajdan daha etkili şekilde kanseri aç bırakabileceği sonucuna vardı.
İnsan tümörleri içinde sinyallerin nerede etkin olduğunu haritalamak
VEGF ve CXCL12’nin glioblastomlar içinde nasıl düzenlendiğini görmek için bilim insanları büyük açık genetik veri setlerini inceledi ve ardından gerçek hasta tümörlerinin yüksek çözünürlüklü görüntülerine yöneldi. VEGF’nin tümörün derinlerindeki düşük oksijenli, hücre ölümü gösteren bölgelerle yakından ilişkili olduğunu buldular; hasarlı doku acil olarak yeni damar çağırıyor. Buna karşılık CXCL12 daha çok hücresel ve yoğun damarlı bölgelerde ve tümör hücrelerinin sağlıklı beyne doğru sızdığı dış infiltrasyon alanlarında yer alıyordu. Gelişmiş boyama teknikleri ve mekânsal gen profilleme kullanarak CXCL12’nin yalnızca tümör hücreleri tarafından değil, aynı zamanda damarların iç yüzeyini oluşturan hücreler, destek hücreleri ve tümör çevresindeki bağışıklık hücreleri dâhil olmak üzere normal beyin damarları tarafından da üretildiğini gösterdiler. Bu bulgu, VEGF ile CXCL12’nin tamamlayıcı ve örtüşmeyen damar yeniden inşa edici sürücüler olduğu fikrini güçlendirdi.
Radyoterapiyi CXCL12 kapanı ve anti-VEGF terapisi ile birleştiren bir çalışma
CXCL12’yi engelleyen NOX-A12 adlı bir ilaçla önceki çalışmalara dayanarak GLORIA denemesi, tümörü tamamen çıkarılamayan ve standart kemoterapiye yanıtı etkileyen bir DNA belirteci taşımayan yeni tanı konmuş erişkin glioblastom hastalarını kaydetti. Tüm hastalar radyoterapi ve sürekli intravenöz NOX-A12 aldı. Genişletme aşamasında, altı hastalık bir alt grup ayrıca rekürren glioblastomda zaten kullanılan ve VEGF’yi hedefleyen bir antikor olan bevacizumab da aldı. Ana amaç güvenliği test etmekti; ekip ayrıca tümör kontrolünün ne kadar sürdüğünü, genel sağkalımı, MR’daki tümör kan akışı değişikliklerini ve hastaların nörolojik fonksiyonları ile yaşam kalitesini izledi.
Güvenlik ve daha güçlü, daha uzun yanıtların işaretleri
Radyoterapi, NOX-A12 ve bevacizumabın üçlü kombinasyonu iyi tolere edildi. Tedaviye bağlı ölüm veya doz sınırlayıcı toksik yan etki görülmedi. Çoğu advers olay hafif ila orta şiddetteydi ve büyük ölçüde tümör veya radyasyonla ilişkiliydi; bevacizumab kaynaklı kan basıncı yükselmeleri ilaçla yönetilebilirdi. Görüntüleme, bevacizumab eklenmesinin tümör kan hacmi ve perfüzyonunda çok daha derin düşüşlere yol açtığını gösterdi; bu da damarların yeniden büyümesinin güçlü şekilde baskılandığını düşündürüyor. Klinik olarak, üçlü tedavi alan hastalarda tümör progresyonsuz medyan süre yaklaşık dokuz ayın biraz üzerindeydi ve medyan genel sağkalım neredeyse 20 aydı—her iki değer de yalnızca NOX-A12 ile radyoterapi alan hastalardan açıkça uzundu ve standart bakım ile dikkatle eşleştirilmiş gruplardan daha iyiydi. Dikkate değer şekilde, üçlü tedavi alan altı hastadan ikisi iki yıldan uzun yaşadı; bu, bu yüksek riskli popülasyon için alışılmadık uzun bir süre.
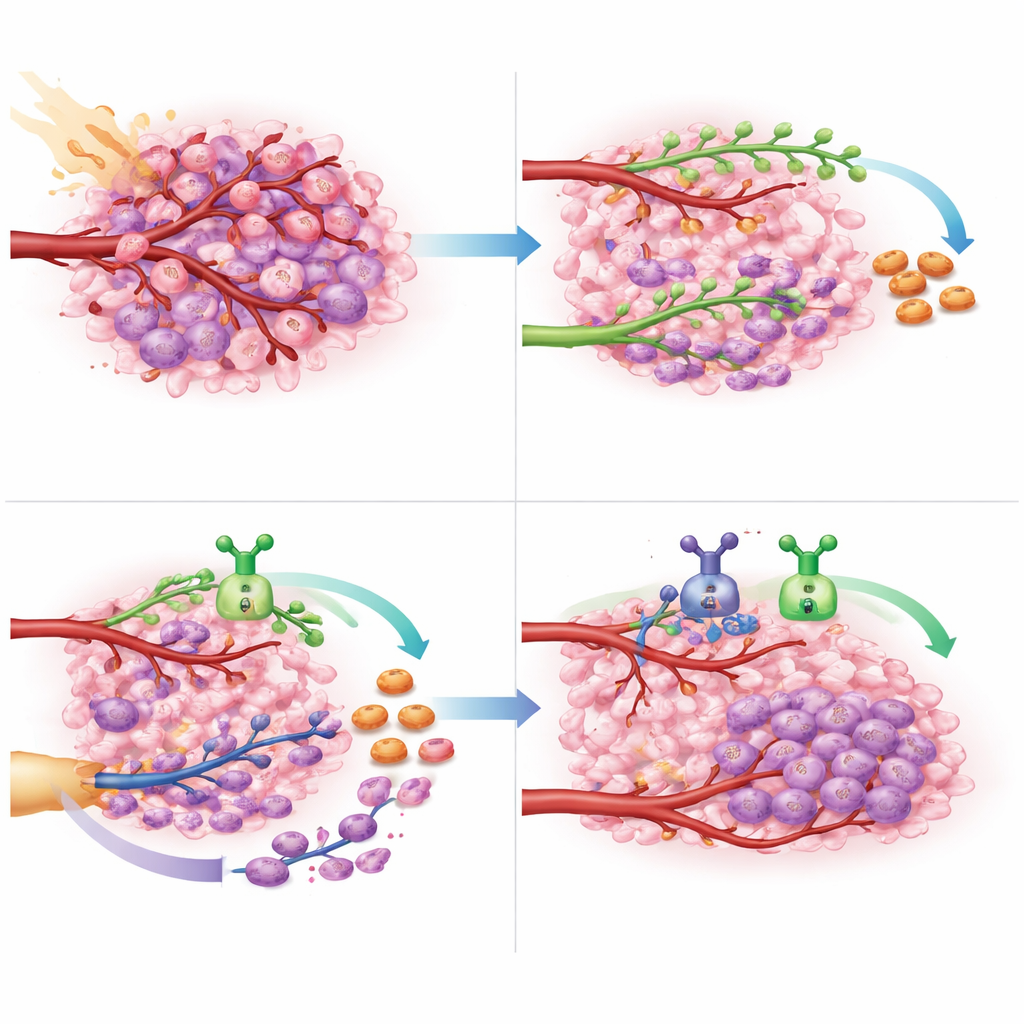
Bu bulgular gelecekteki beyin kanseri bakımına ne ifade edebilir
Tümörü tamamen çıkarılamayan ve standart kemoterapiye dirençli glioblastomlu hastalar için seçenekler sınırlı ve sonuçlar kötümserdir. Bu çalışma, radyoterapi sırasında ve sonrasında iki ana damar onarım yolunu—VEGF kaynaklı budama ve CXCL12 kaynaklı yeni damar oluşturan hücrelerin toplanmasını—aynı anda kapatmanın güvenli şekilde gerçekleştirilebileceğine ve tümörün yeniden büyümesini önemli ölçüde geciktirebileceğine dair ilk kanıtı sunuyor. Çalışma küçük ve esas olarak güvenliği değerlendirmek üzere tasarlanmış olsa da sağkalımdaki kazanımlar, daha büyük, randomize çalışmaları hak edecek kadar umut verici. Doğrulanırsa, bu iki vasküler sinyalin eşzamanlı hedeflenmesi, bu agresif beyin kanserini daha uzun süre kontrol altında tutmak için yeni bir birinci basamak stratejisi olabilir.
Atıf: Giordano, F.A., Layer, J.P., Turiello, R. et al. L-RNA aptamer-based CXCL12 inhibition combined with radiotherapy and bevacizumab in newly-diagnosed glioblastoma: expansion of the phase I/II GLORIA trial. Nat Commun 17, 3405 (2026). https://doi.org/10.1038/s41467-026-71362-7
Anahtar kelimeler: glioblastom, beyin kanseri, tümör kan damarları, radyoterapi, hedefe yönelik tedavi