Clear Sky Science · pt
Inibição de CXCL12 por aptâmero L-RNA combinada com radioterapia e bevacizumabe em glioblastoma recém-diagnosticado: expansão do ensaio de fase I/II GLORIA
Por que este estudo sobre câncer cerebral importa
O glioblastoma é um dos cânceres cerebrais mais letais, em parte porque quase sempre volta a crescer após o tratamento. Mesmo quando os cirurgiões removem o máximo possível do tumor e os médicos seguem com radioterapia, o suprimento sanguíneo do tumor se reconstrói rapidamente, permitindo que as células cancerígenas se recuperem. Este estudo testou uma nova estratégia: bloquear duas rotas diferentes que o tumor usa para regenerar seus vasos sanguíneos, e investigar se esse bloqueio duplo, adicionado à radioterapia, pode manter o câncer sob controle por mais tempo em pacientes que normalmente têm prognóstico muito ruim.
DuAS rotas ocultas que alimentam o tumor
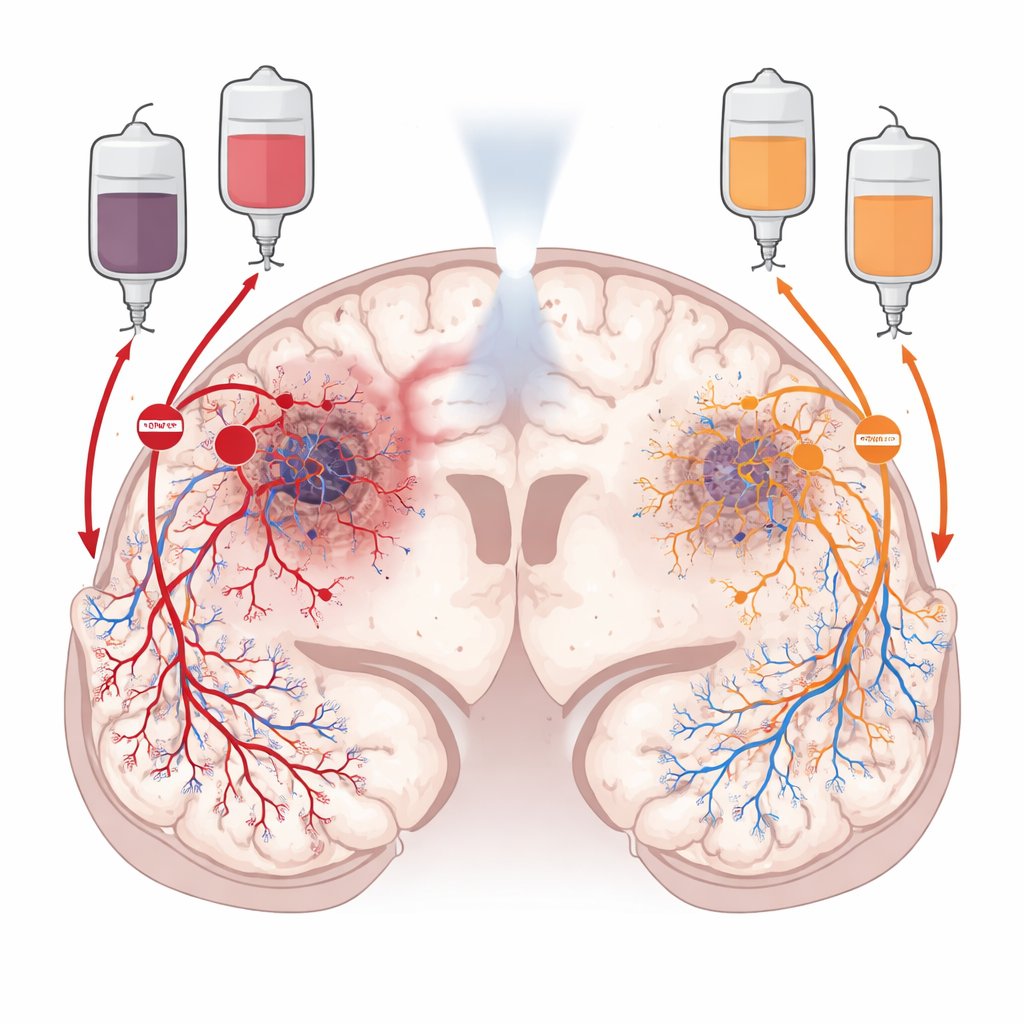
Após a radioterapia, o glioblastoma não permanece imóvel. Ele remodela ativamente seu entorno para restaurar o fluxo sanguíneo. Uma rota, chamada angiogênese, depende de um sinal de crescimento que faz com que vasos sanguíneos próximos brotem novos ramos para dentro do tumor. A outra, chamada vasculogênese, recruta células formadoras de vasos sanguíneos provenientes da medula óssea, que migram até o tumor e constroem novos vasos do zero. Os pesquisadores se concentraram em dois “controladores de tráfego” químicos que orientam essas rotas: o VEGF, que impulsiona a formação local de novos ramos vasculares, e o CXCL12, que atrai células progenitoras circulantes e células imunes e auxilia sua fixação no tumor. Como esses sinais atuam em regiões diferentes do tumor, a equipe raciocinou que bloquear ambos poderia privar o câncer de suprimento sanguíneo mais eficazmente do que bloquear apenas um.
Mapeando onde os sinais agem dentro de tumores humanos
Para ver como VEGF e CXCL12 estão distribuídos dentro dos glioblastomas, os cientistas exploraram grandes conjuntos de dados genéticos públicos e depois recorreram a imagens de alta resolução de tumores reais de pacientes. Eles descobriram que o VEGF acompanha de perto regiões de baixo oxigênio e tecido em degeneração nas profundezas do tumor, onde o tecido danificado solicita com urgência novos vasos. O CXCL12, em contraste, aparece principalmente nas zonas mais celulares e altamente vasculares e nas áreas de infiltração externas, onde células tumorais se estendem para o tecido cerebral saudável. Usando técnicas avançadas de coloração e perfilamento espacial de genes, mostraram que o CXCL12 é produzido não apenas pelas células tumorais, mas também pelo endotélio dos vasos, células de suporte e células imunes dentro e ao redor do tumor, incluindo vasos cerebrais normais. Isso reforça a ideia de que VEGF e CXCL12 são motores complementares e não sobrepostos da reconstrução vascular.
Um ensaio que combina radiação com uma armadilha para CXCL12 e terapia anti-VEGF
Com base em trabalhos anteriores com uma droga que bloqueia o CXCL12 chamada NOX-A12, o ensaio GLORIA recrutou adultos com glioblastoma recém-diagnosticado cujos tumores não puderam ser completamente removidos e que não tinham um marcador de DNA que torna a quimioterapia padrão eficaz. Todos os pacientes receberam radioterapia e NOX-A12 intravenoso contínuo. Em uma fase de expansão, um subconjunto de seis pacientes também recebeu bevacizumabe, um anticorpo que mira o VEGF e já é usado em glioblastoma recorrente. O objetivo principal foi testar a segurança; a equipe também acompanhou por quanto tempo os tumores permaneceram controlados, a sobrevida global, alterações no fluxo sanguíneo tumoral na ressonância magnética e a função neurológica e qualidade de vida dos pacientes.
Segurança e sinais de respostas mais fortes e duradouras
A combinação tripla de radioterapia, NOX-A12 e bevacizumabe mostrou-se bem tolerada. Não houve mortes relacionadas ao tratamento nem efeitos tóxicos limitantes de dose. A maioria dos eventos adversos foi leve a moderada e em grande parte associada ao próprio tumor ou à radiação; elevações da pressão arterial atribuídas ao bevacizumabe foram manejáveis com medicação. As imagens mostraram que a adição do bevacizumabe levou a quedas muito mais profundas no volume sanguíneo tumoral e na perfusão, sugerindo que a reabertura dos vasos foi fortemente suprimida. Clinicamente, pacientes na terapia tripla tiveram um período mediano sem progressão tumoral pouco superior a nove meses e uma sobrevida global mediana de quase 20 meses — ambos claramente mais longos que nos pacientes que receberam radioterapia com NOX-A12 isoladamente, e melhores que grupos cuidadosamente pareados tratados com o cuidado padrão. Notavelmente, dois dos seis pacientes na terapia tripla viveram mais de dois anos, um tempo surpreendentemente longo para essa população de alto risco.
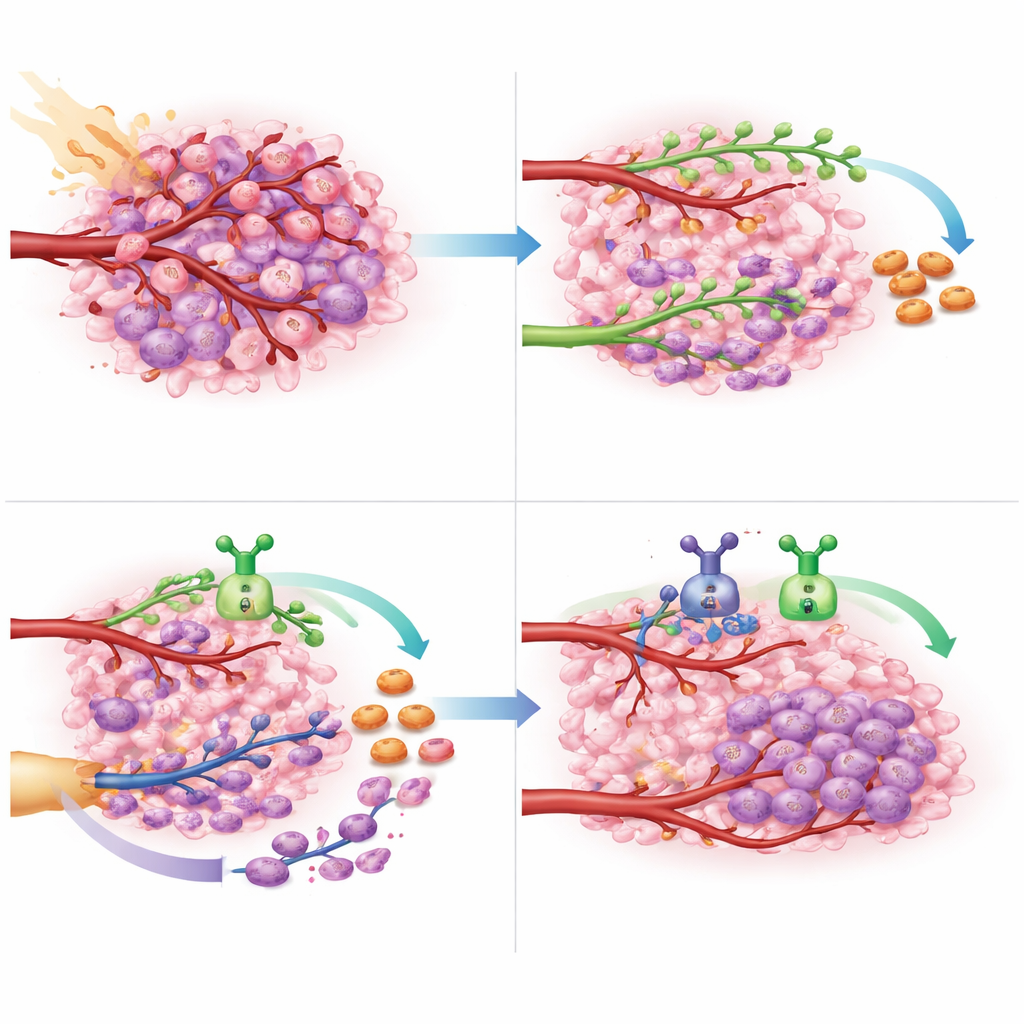
O que isso pode significar para o cuidado futuro do câncer cerebral
Para pacientes com glioblastoma que não pode ser totalmente removido e que é resistente à quimioterapia padrão, as opções são escassas e os desfechos são pessimistas. Este estudo oferece prova de princípio de que bloquear ambas as principais rotas de reparo vascular — o brotamento dirigido por VEGF e o recrutamento por CXCL12 de células formadoras de novos vasos — durante e após a radioterapia pode ser feito de forma segura e pode retardar substancialmente o re crescimento tumoral. Embora o ensaio tenha sido pequeno e projetado principalmente para avaliar segurança, os ganhos de sobrevida são animadores o suficiente para justificar estudos maiores e randomizados. Se confirmada, a abordagem de duplo direcionamento desses dois sinais vasculares poderia se tornar uma nova estratégia de primeira linha para manter esse câncer cerebral agressivo controlado por mais tempo.
Citação: Giordano, F.A., Layer, J.P., Turiello, R. et al. L-RNA aptamer-based CXCL12 inhibition combined with radiotherapy and bevacizumab in newly-diagnosed glioblastoma: expansion of the phase I/II GLORIA trial. Nat Commun 17, 3405 (2026). https://doi.org/10.1038/s41467-026-71362-7
Palavras-chave: glioblastoma, câncer cerebral, vasos sanguíneos tumorais, radioterapia, terapia direcionada