Clear Sky Science · pl
Hamowanie CXCL12 za pomocą aptameru L-RNA w połączeniu z radioterapią i bewacyzumabem w pierwotnie rozpoznanym glejaku wielopostaciowym: rozszerzenie badania fazy I/II GLORIA
Dlaczego to badanie nad rakiem mózgu ma znaczenie
Glejaki wielopostaciowe należą do najbardziej śmiertelnych nowotworów mózgu, między innymi dlatego, że prawie zawsze odrastają po leczeniu. Nawet gdy chirurdzy usuną jak najwięcej guza, a następnie zastosuje się radioterapię, układ naczyń guza szybko się odbudowuje, umożliwiając przeżycie komórek nowotworowych. W tym badaniu przetestowano nową strategię: zablokowanie dwóch różnych dróg, których guz używa do odtwarzania unaczynienia, i sprawdzenie, czy takie podwójne wyłączenie, dodane do radioterapii, może bezpiecznie utrzymywać nowotwór pod kontrolą dłużej u pacjentów o zwykle złym rokowaniu.
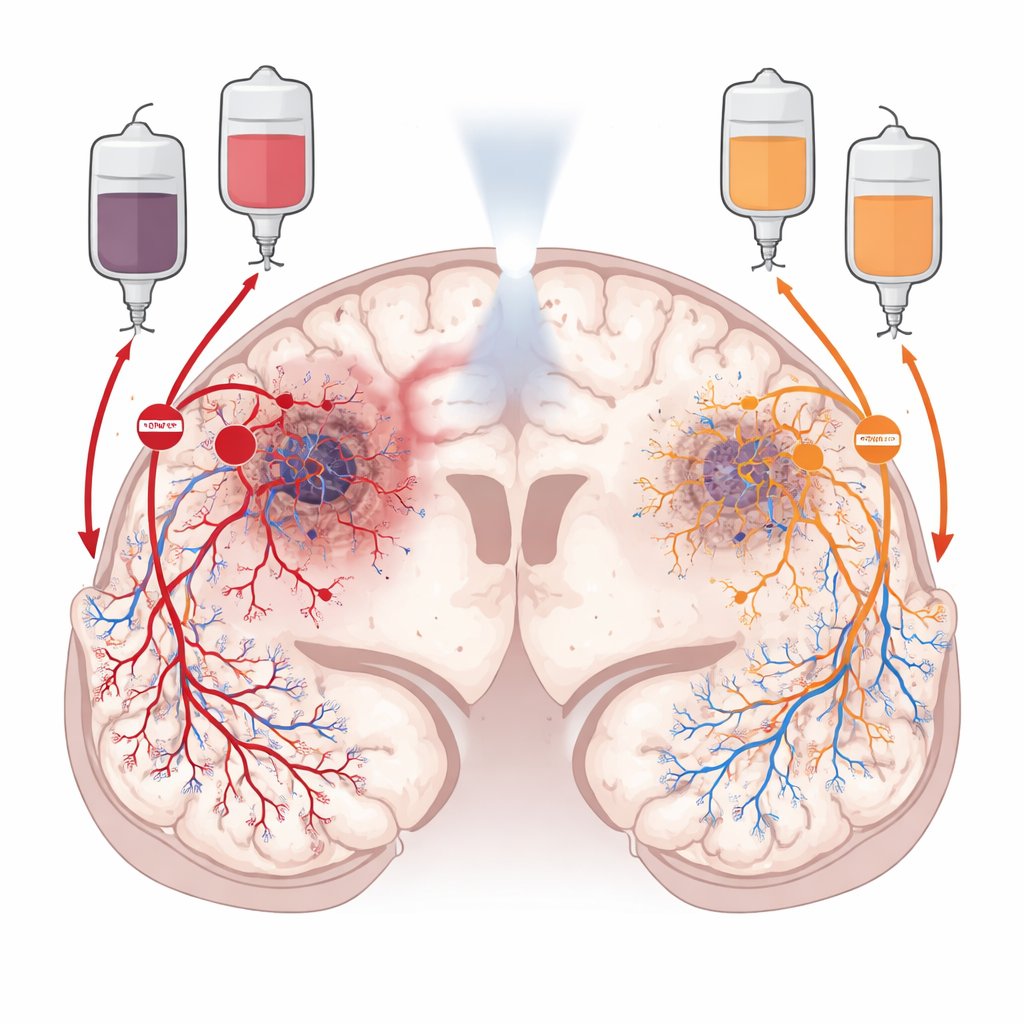
Dwie ukryte drogi zaopatrujące guz
Po radioterapii glejak nie pozostaje bierny. Aktywnie przekształca swoje otoczenie, aby przywrócić przepływ krwi. Jedna droga, zwana angiogenezą, opiera się na sygnale wzrostowym, który powoduje, że pobliskie naczynia krwionośne wypuszczają nowe odgałęzienia do guza. Druga, nazywana wazokulogenezą, rekrutuje z szpiku kostnego świeże komórki tworzące naczynia, które migrują do guza i budują nowe naczynia od podstaw. Badacze skupili się na dwóch chemicznych „kierowcach ruchu”, które kierują tymi drogami: VEGF, który napędza miejscowe rozgałęzianie naczyń, oraz CXCL12, który przyciąga krążące komórki progenitorowe i komórki układu odpornościowego i pomaga im zasiedlić się w guzie. Ponieważ te sygnały działają w różnych obszarach guza, zespół wnioskował, że zablokowanie obu może bardziej efektywnie „zagłodzić” nowotwór niż blokada tylko jednego z nich.
Mapowanie miejsc działania sygnałów w ludzkich guzach
Aby zobaczyć, jak VEGF i CXCL12 są rozmieszczone wewnątrz glejaków, naukowcy przeanalizowali duże publiczne zbiory danych genetycznych, a następnie zwrócili się do obrazów o wysokiej rozdzielczości pochodzących z rzeczywistych guzów pacjentów. Odkryli, że VEGF silnie koreluje z obszarami o niskim utlenowaniu i obumierającą tkanką w głębi guza, gdzie uszkodzona tkanka pilnie potrzebuje nowych naczyń. CXCL12 natomiast występuje głównie w bardziej komórkowych i silnie unaczynionych strefach oraz w zewnętrznych obszarach nacieku, gdzie komórki nowotworowe wnikają w zdrową tkankę mózgową. Zastosowawszy zaawansowane techniki barwienia i przestrzenne profilowanie genów, wykazali, że CXCL12 jest produkowany nie tylko przez komórki guza, lecz także przez śródbłonek naczyń, komórki podporowe i komórki układu odpornościowego w obrębie i wokół guza, włączając w to normalne naczynia mózgowe. Wzmocniło to ideę, że VEGF i CXCL12 są komplementarnymi, niepokrywającymi się czynnikami napędzającymi odbudowę naczyń.
Badanie łączące radioterapię z pułapką na CXCL12 i terapią anty-VEGF
W oparciu o wcześniejsze prace nad lekiem blokującym CXCL12 o nazwie NOX-A12, badanie GLORIA zrekrutowało dorosłych z nowo rozpoznanym glejakiem wielopostaciowym, których guzy nie mogły być całkowicie usunięte i którzy nie mieli markera DNA czyniącego standardową chemioterapię skuteczną. Wszyscy pacjenci otrzymali radioterapię i ciągłe dożylne podawanie NOX-A12. W fazie rozszerzeniowej podgrupa sześciu pacjentów otrzymała dodatkowo bewacyzumab — przeciwciało ukierunkowane przeciwko VEGF, stosowane już w nawrotowym glejaku. Głównym celem była ocena bezpieczeństwa; zespół monitorował także czas utrzymania kontroli nad guzem, przeżycie całkowite, zmiany w przepływie krwi w guzie w badaniach MRI oraz funkcje neurologiczne i jakość życia pacjentów.
Bezpieczeństwo i sygnały na rzecz silniejszych, dłuższych odpowiedzi
Potrójna kombinacja radioterapii, NOX-A12 i bewacyzumabu okazała się dobrze tolerowana. Nie odnotowano zgonów związanych z leczeniem ani działań toksycznych ograniczających dawkę. Większość zdarzeń niepożądanych miała łagodny do umiarkowanego charakter i była w dużej mierze związana z guzem lub samą radioterapią; wzrosty ciśnienia krwi po bewacyzumabie były możliwe do opanowania leczeniem farmakologicznym. Obrazowanie wykazało, że dodanie bewacyzumabu prowadziło do znacznie głębszych spadków objętości krwi w guzie i perfuzji, co sugeruje silne zahamowanie odbudowy naczyń. Klinicznie pacjenci otrzymujący potrójną terapię mieli medianę okresu bez progresji nieco ponad dziewięć miesięcy oraz medianę przeżycia całkowitego bliską 20 miesięcy — oba wyniki były wyraźnie dłuższe niż u pacjentów, którzy otrzymali radioterapię z NOX-A12 samodzielnie, a także lepsze od starannie dopasowanych grup leczonych standardowo. Co godne uwagi, dwoje z sześciu pacjentów na terapii potrójnej przeżyło ponad dwa lata, co jest nietypowo długim okresem dla tej grupy wysokiego ryzyka.
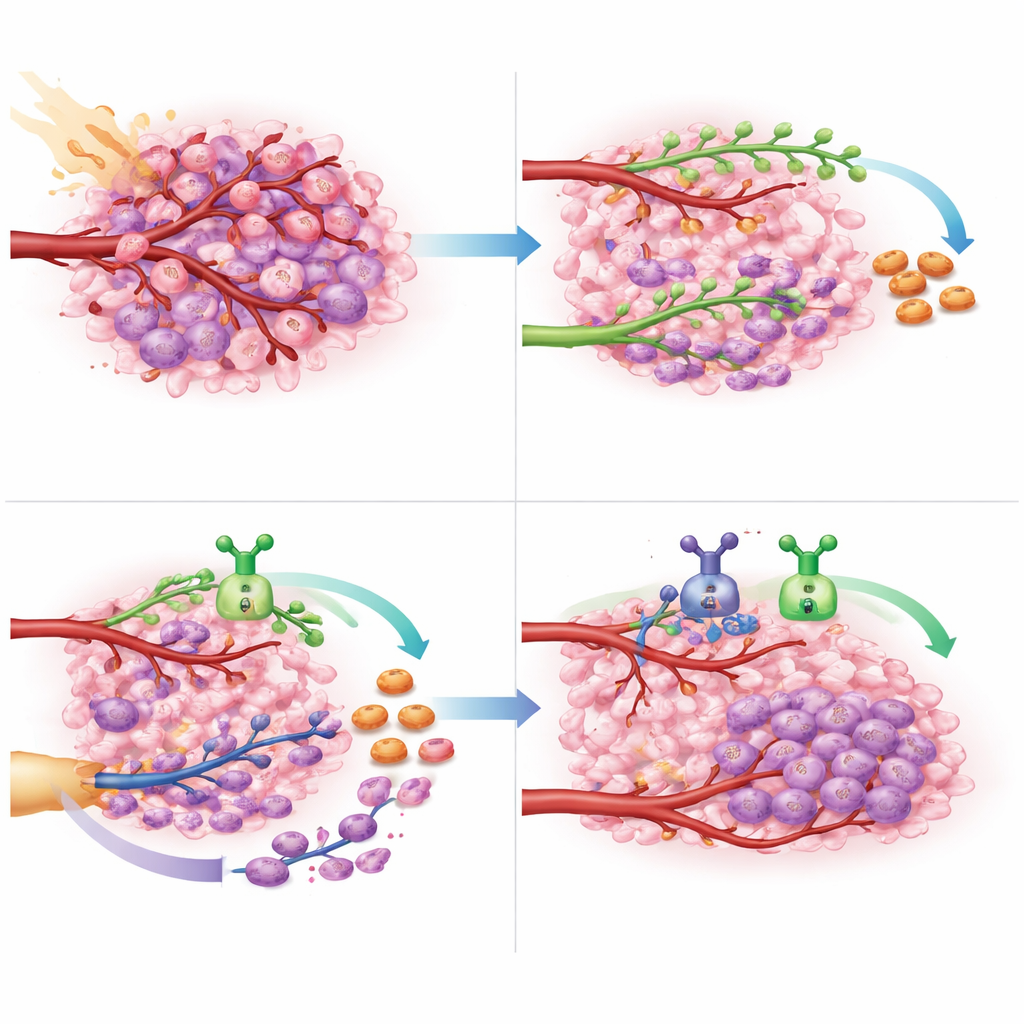
Co to może znaczyć dla przyszłej opieki nad rakiem mózgu
Dla pacjentów z glejakiem, którego nie da się całkowicie usunąć i który jest oporny na standardową chemioterapię, opcje terapeutyczne są ograniczone, a rokowanie złe. To badanie dostarcza dowodu koncepcji, że jednoczesne zablokowanie obu głównych dróg naprawy naczyń — rozgałęziania napędzanego przez VEGF oraz rekrutacji komórek tworzących naczynia kierowanej przez CXCL12 — podczas i po radioterapii można przeprowadzić bezpiecznie i że może to istotnie opóźnić odrost guza. Ponieważ badanie było małe i miało głównie charakter oceny bezpieczeństwa, uzyskane korzyści w zakresie przeżycia są na tyle obiecujące, że uzasadniają przeprowadzenie większych, randomizowanych badań. Jeśli zostaną potwierdzone, podwójne ukierunkowanie tych dwóch sygnałów naczyniowych mogłoby stać się nową strategią pierwszego wyboru, mającą na celu dłuższe utrzymanie pod kontrolą tego agresywnego nowotworu mózgu.
Cytowanie: Giordano, F.A., Layer, J.P., Turiello, R. et al. L-RNA aptamer-based CXCL12 inhibition combined with radiotherapy and bevacizumab in newly-diagnosed glioblastoma: expansion of the phase I/II GLORIA trial. Nat Commun 17, 3405 (2026). https://doi.org/10.1038/s41467-026-71362-7
Słowa kluczowe: glejak wielopostaciowy, rak mózgu, naczynia guza, radioterapia, terapia celowana