Clear Sky Science · es
Inhibición de CXCL12 basada en aptámeros L-ARN combinada con radioterapia y bevacizumab en glioblastoma recién diagnosticado: ampliación del ensayo fase I/II GLORIA
Por qué importa este estudio sobre el cáncer cerebral
El glioblastoma es uno de los cánceres cerebrales más letales, en parte porque casi siempre vuelve después del tratamiento. Incluso cuando los cirujanos extirpan tanto tumor como es posible y los médicos administran radiación a continuación, el suministro de sangre del tumor se reconstruye con rapidez, lo que permite que las células cancerosas se recuperen. Este estudio probó una nueva estrategia: bloquear dos rutas diferentes que el tumor utiliza para regenerar sus vasos sanguíneos, y evaluar si este cierre dual, añadido a la radioterapia, puede contener el cáncer por más tiempo de forma segura en pacientes que habitualmente tienen un pronóstico muy malo.
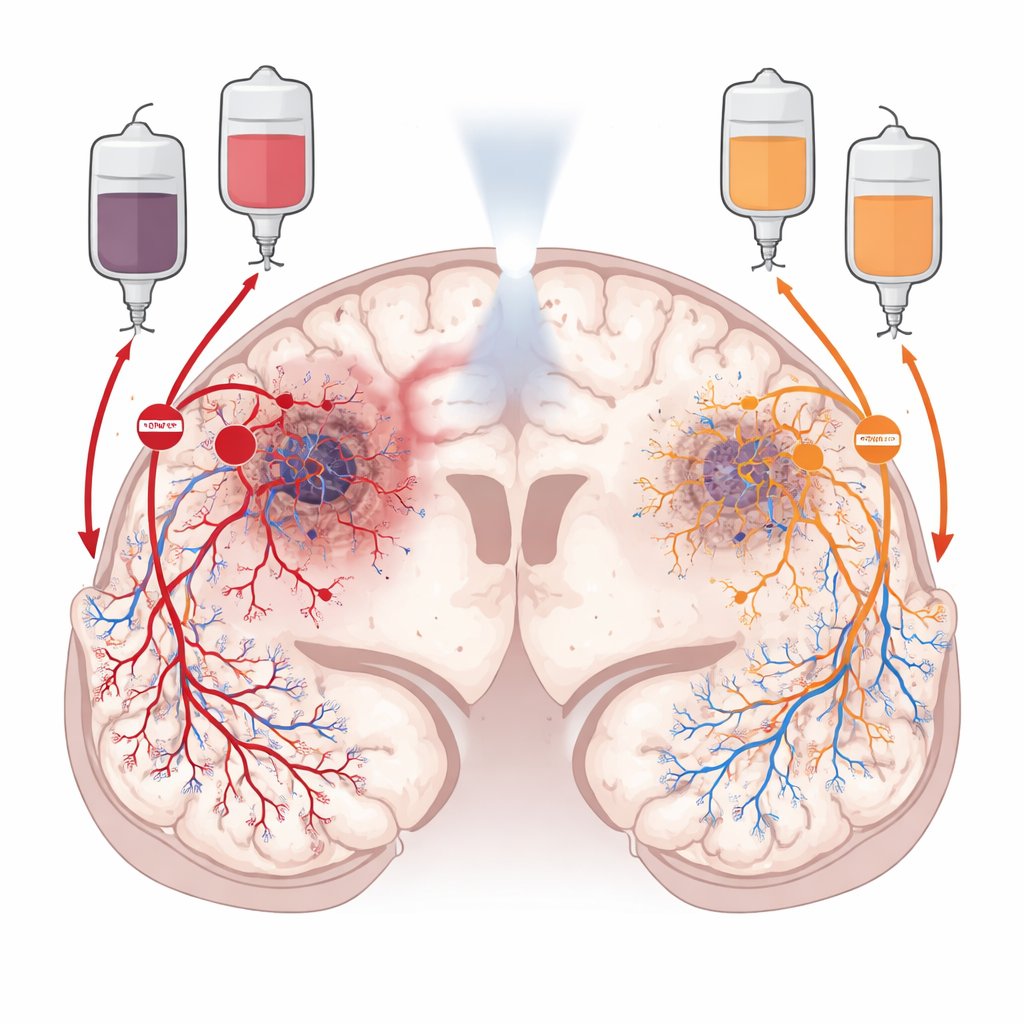
Dos rutas ocultas que alimentan al tumor
Tras la radioterapia, el glioblastoma no se queda quieto. Remodela activamente su entorno para restaurar el flujo sanguíneo. Una ruta, llamada angiogénesis, depende de una señal de crecimiento que hace que los vasos sanguíneos cercanos broten nuevas ramas hacia el tumor. La otra, llamada vasculogénesis, recluta células formadoras de vasos sanguíneos desde la médula ósea, que se dirigen al tumor y construyen nuevos vasos desde cero. Los investigadores se centraron en dos “controladores de tráfico” químicos que guían estas rutas: el VEGF, que impulsa el brote local de vasos, y la CXCL12, que atrae progenitores circulantes y células inmunitarias y les ayuda a asentarse en el tumor. Dado que estas señales actúan en distintas regiones del tumor, el equipo razonó que bloquear ambas podría privar al cáncer de sangre con más eficacia que inhibir solo una.
Mapeando dónde actúan las señales dentro de los tumores humanos
Para ver cómo se disponen VEGF y CXCL12 dentro de los glioblastomas, los científicos exploraron grandes bases de datos genéticas públicas y luego recurrieron a imágenes de alta resolución de tumores reales de pacientes. Encontraron que el VEGF se asocia estrechamente con regiones profundas del tumor con bajo oxígeno y tejido en descomposición, donde el tejido dañado reclama con urgencia nuevos vasos. La CXCL12, en contraste, aparece principalmente en las zonas más celulares y altamente vasculares y en las áreas de infiltración externas donde las células tumorales se extienden hacia el cerebro sano. Mediante técnicas avanzadas de tinción y perfilado espacial de genes, mostraron que la CXCL12 no solo la producen las células tumorales, sino también el revestimiento de los vasos sanguíneos, células de sostén y células inmunitarias dentro y alrededor del tumor, incluidos vasos cerebrales normales. Esto reforzó la idea de que VEGF y CXCL12 son impulsores complementarios y no solapados de la reconstrucción vascular.
Un ensayo que combina radiación con una trampa para CXCL12 y terapia anti-VEGF
Basándose en trabajos previos con un fármaco bloqueador de CXCL12 llamado NOX-A12, el ensayo GLORIA reclutó adultos con glioblastoma recién diagnosticado cuyos tumores no podían extirparse por completo y que carecían de un marcador genético que hace que la quimioterapia estándar sea eficaz. Todos los pacientes recibieron radioterapia y NOX-A12 por vía intravenosa continua. En una fase de ampliación, un subconjunto de seis pacientes también recibió bevacizumab, un anticuerpo que apunta al VEGF y que ya se usa en glioblastoma recurrente. El objetivo principal fue evaluar la seguridad; el equipo también siguió el tiempo de control tumoral, la supervivencia global, los cambios en el flujo sanguíneo tumoral en resonancia magnética y la función neurológica y la calidad de vida de los pacientes.
Seguridad y señales de respuestas más intensas y duraderas
La combinación triple de radioterapia, NOX-A12 y bevacizumab resultó bien tolerada. No hubo muertes relacionadas con el tratamiento ni efectos tóxicos que limitaran la dosis. La mayoría de los eventos adversos fueron leves a moderados y estuvieron en gran medida relacionados con el tumor o con la propia radiación; las elevaciones de la presión arterial por bevacizumab se pudieron manejar con medicación. La imagenología mostró que añadir bevacizumab provocó descensos mucho más pronunciados en el volumen y la perfusión sanguínea del tumor, lo que sugiere que la regeneración de vasos quedó fuertemente suprimida. Clínicamente, los pacientes con la terapia triple tuvieron un período medio sin progresión tumoral de algo más de nueve meses y una mediana de supervivencia global de casi 20 meses: ambos claramente superiores a los de los pacientes que recibieron solo radioterapia con NOX-A12, y mejores que grupos cuidadosamente emparejados tratados con la atención estándar. De forma notable, dos de los seis pacientes con la terapia triple vivieron más de dos años, un tiempo inusualmente largo para esta población de alto riesgo.
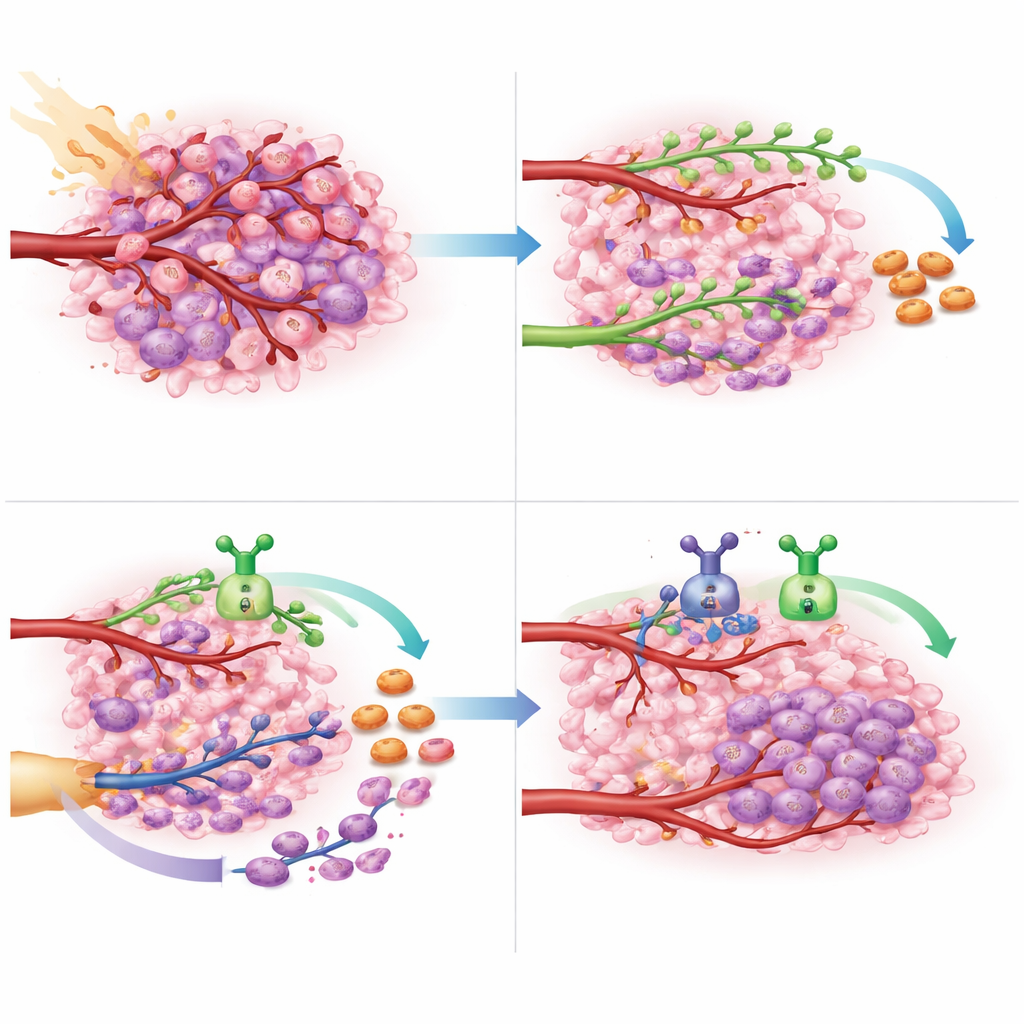
Qué podría significar esto para la atención futura del cáncer cerebral
Para pacientes con glioblastoma que no puede extirparse por completo y que es resistente a la quimioterapia estándar, las opciones son limitadas y los resultados son sombríos. Este estudio ofrece una prueba de concepto de que cerrar ambas rutas principales de reparación vascular—el brote impulsado por VEGF y el reclutamiento de células formadoras de vasos guiado por CXCL12—durante y después de la radioterapia puede realizarse de forma segura y puede retrasar sustancialmente la reaparición tumoral. Aunque el ensayo fue pequeño y diseñado principalmente para valorar la seguridad, las ganancias en supervivencia son lo bastante alentadoras como para justificar estudios aleatorizados más amplios. Si se confirman, la doble diana sobre estas dos señales vasculares podría convertirse en una nueva estrategia de primera línea para mantener este cáncer cerebral agresivo controlado por más tiempo.
Cita: Giordano, F.A., Layer, J.P., Turiello, R. et al. L-RNA aptamer-based CXCL12 inhibition combined with radiotherapy and bevacizumab in newly-diagnosed glioblastoma: expansion of the phase I/II GLORIA trial. Nat Commun 17, 3405 (2026). https://doi.org/10.1038/s41467-026-71362-7
Palabras clave: glioblastoma, cáncer de cerebro, vasos sanguíneos del tumor, radioterapia, terapia dirigida