Clear Sky Science · fr
Inhibition de CXCL12 par aptamère L-ARN combinée à la radiothérapie et au bevacizumab dans le glioblastome nouvellement diagnostiqué : extension de l’essai de phase I/II GLORIA
Pourquoi cette étude sur le cancer du cerveau est importante
Le glioblastome est l’un des cancers du cerveau les plus mortels, en partie parce qu’il récidive presque toujours après traitement. Même lorsque les chirurgiens retirent la plus grande partie de la tumeur et que les médecins poursuivent par une radiothérapie, l’apport sanguin tumoral se reconstitue rapidement, permettant aux cellules cancéreuses de se rétablir. Cette étude a testé une nouvelle stratégie : bloquer deux voies différentes que la tumeur utilise pour regénérer ses vaisseaux sanguins, et vérifier si cette double inhibition, ajoutée à la radiothérapie, peut contenir la maladie plus longtemps de façon sûre chez des patients qui ont généralement un pronostic très défavorable.
Deux voies cachées qui alimentent la tumeur
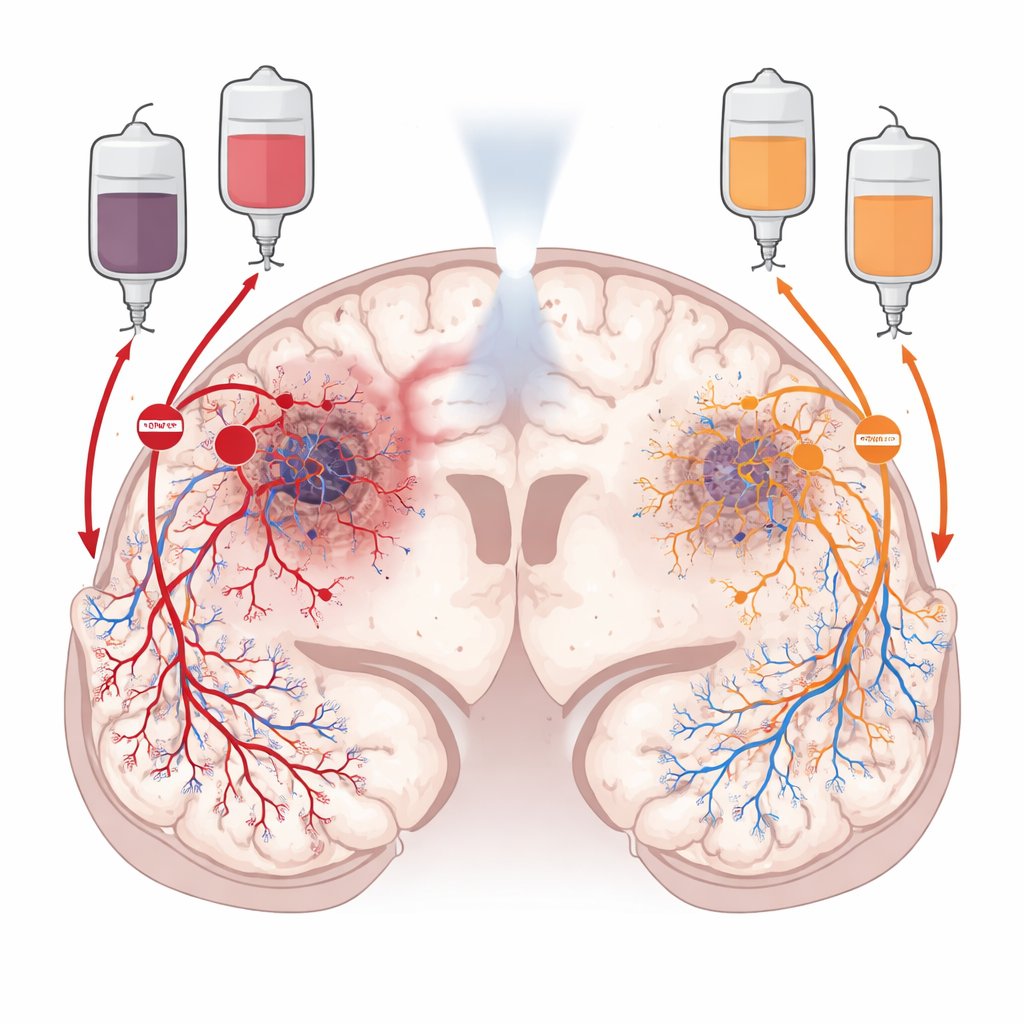
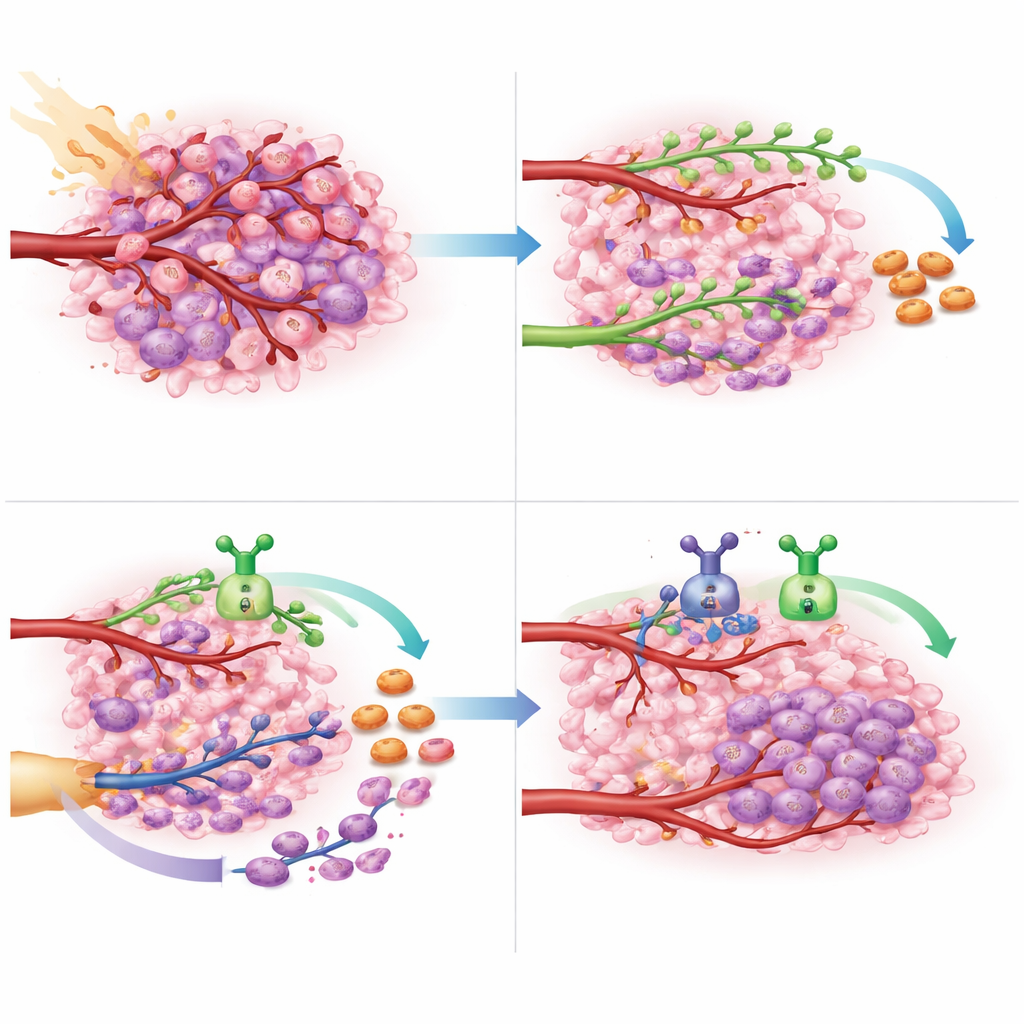
Après la radiothérapie, le glioblastome ne reste pas inerte. Il réaménage activement son environnement pour restaurer la vascularisation. Une voie, appelée angiogenèse, repose sur un signal de croissance qui fait bourgeonner les vaisseaux voisins vers la tumeur. L’autre, appelée vasculogenèse, recrute des cellules formatrices de vaisseaux provenant de la moelle osseuse, qui migrent vers la tumeur et construisent de nouveaux vaisseaux à partir de zéro. Les chercheurs se sont concentrés sur deux « régulateurs » chimiques qui orientent ces voies : le VEGF, qui stimule le bourgeonnement local des vaisseaux, et le CXCL12, qui attire des cellules progénitrices et immunitaires circulantes et facilite leur implantation dans la tumeur. Parce que ces signaux opèrent dans des régions différentes de la tumeur, l’équipe a émis l’hypothèse que bloquer les deux pourrait affamer la tumeur plus efficacement que bloquer l’un ou l’autre seul.
Cartographier où les signaux s’exercent à l’intérieur des tumeurs humaines
Pour voir comment le VEGF et le CXCL12 sont distribués dans les glioblastomes, les scientifiques ont exploité de larges jeux de données génétiques publics puis se sont tournés vers des images haute résolution de véritables tumeurs de patients. Ils ont constaté que le VEGF coïncide étroitement avec les zones profondément hypoxiques et nécrosées de la tumeur, où le tissu lésé appelle d’urgence de nouveaux vaisseaux. Le CXCL12, en revanche, apparaît principalement dans les zones beaucoup plus cellulaires et hautement vascularisées et dans les zones d’infiltration périphériques où les cellules tumorales s’étendent dans le cerveau sain. Grâce à des techniques de coloration avancées et au profilage spatial de l’expression génique, ils ont montré que le CXCL12 est produit non seulement par les cellules tumorales, mais aussi par l’endothélium vasculaire, les cellules de soutien et les cellules immunitaires à l’intérieur et autour de la tumeur, y compris les vaisseaux cérébraux normaux. Cela a renforcé l’idée que VEGF et CXCL12 sont des moteurs complémentaires et non redondants de la reconstruction vasculaire.
Un essai combinant radiothérapie, leurre de CXCL12 et thérapie anti-VEGF
Reposant sur des travaux antérieurs avec un médicament bloquant CXCL12 nommé NOX-A12, l’essai GLORIA a inclus des adultes atteints de glioblastome nouvellement diagnostiqué dont les tumeurs n’étaient pas résécables complètement et qui ne présentaient pas un marqueur génétique rendant la chimiothérapie standard efficace. Tous les patients ont reçu une radiothérapie et une perfusion intraveineuse continue de NOX-A12. Lors d’une phase d’extension, un sous-groupe de six patients a également reçu du bevacizumab, un anticorps ciblant le VEGF déjà utilisé dans le glioblastome récidivant. L’objectif principal était d’évaluer la sécurité ; l’équipe a aussi suivi la durée de contrôle tumoral, la survie globale, les modifications du flux sanguin tumoral en IRM, ainsi que la fonction neurologique et la qualité de vie des patients.
Sécurité et signes de réponses plus fortes et plus durables
La combinaison triple radiothérapie, NOX-A12 et bevacizumab s’est avérée bien tolérée. Il n’y a eu ni décès lié au traitement ni toxicités limitantes à la dose. La plupart des effets indésirables étaient légers à modérés et liés majoritairement à la tumeur ou à la radiothérapie elle-même ; les élévations de la tension artérielle liées au bevacizumab ont été gérées par des médicaments. L’imagerie a montré que l’ajout du bevacizumab entraînait des baisses beaucoup plus marquées du volume sanguin tumoral et de la perfusion, suggérant que la regénération vasculaire était fortement supprimée. Sur le plan clinique, les patients recevant la triple thérapie ont présenté une médiane de contrôle sans progression de juste plus de neuf mois et une survie globale médiane de près de 20 mois — des durées nettement supérieures à celles des patients traités par radiothérapie et NOX-A12 seuls, et meilleures que celles de groupes appariés recevant les soins standard. De façon remarquable, deux des six patients sous triple thérapie ont vécu plus de deux ans, ce qui est inhabituel pour cette population à haut risque.
Ce que cela pourrait signifier pour les soins futurs du cancer du cerveau
Pour les patients atteints d’un glioblastome non complètement résécable et résistant à la chimiothérapie standard, les options sont rares et le pronostic sombre. Cette étude apporte une preuve de principe que bloquer simultanément les deux grandes voies de réparation vasculaire — le bourgeonnement induit par le VEGF et le recrutement de cellules formatrices de vaisseaux induit par le CXCL12 — pendant et après la radiothérapie peut être réalisé de façon sûre et retarder substantiellement la repousse tumorale. Bien que l’essai soit de petite taille et conçu principalement pour évaluer la sécurité, les gains de survie sont suffisamment encourageants pour justifier des études randomisées plus larges. Si ces résultats sont confirmés, le double ciblage de ces deux signaux vasculaires pourrait devenir une nouvelle stratégie de première ligne pour contenir plus longtemps ce cancer cérébral agressif.
Citation: Giordano, F.A., Layer, J.P., Turiello, R. et al. L-RNA aptamer-based CXCL12 inhibition combined with radiotherapy and bevacizumab in newly-diagnosed glioblastoma: expansion of the phase I/II GLORIA trial. Nat Commun 17, 3405 (2026). https://doi.org/10.1038/s41467-026-71362-7
Mots-clés: glioblastome, cancer du cerveau, vaisseaux tumoraux, radiothérapie, thérapie ciblée