Clear Sky Science · sv
L-RNA-aptamer-baserad CXCL12-hämning i kombination med strålbehandling och bevacizumab vid nyligen diagnostiserad glioblastom: expansion av fas I/II-studien GLORIA
Varför denna studie om hjärncancer är viktig
Glioblastom är en av de dödligaste hjärntumörerna, delvis därför att den nästan alltid växer tillbaka efter behandling. Även när kirurger tar bort så mycket tumör som möjligt och läkare följer upp med strålbehandling, återuppbyggs tumörens blodtillförsel snabbt, vilket gör att cancercellerna kan återhämta sig. Denna studie testade en ny strategi: att blockera två olika vägar som tumören använder för att återbilda sina blodkärl, och undersöka om denna dubbla avstängning, tillagd strålbehandling, säkert kan hålla cancern i schack längre hos patienter som i regel har dålig prognos.
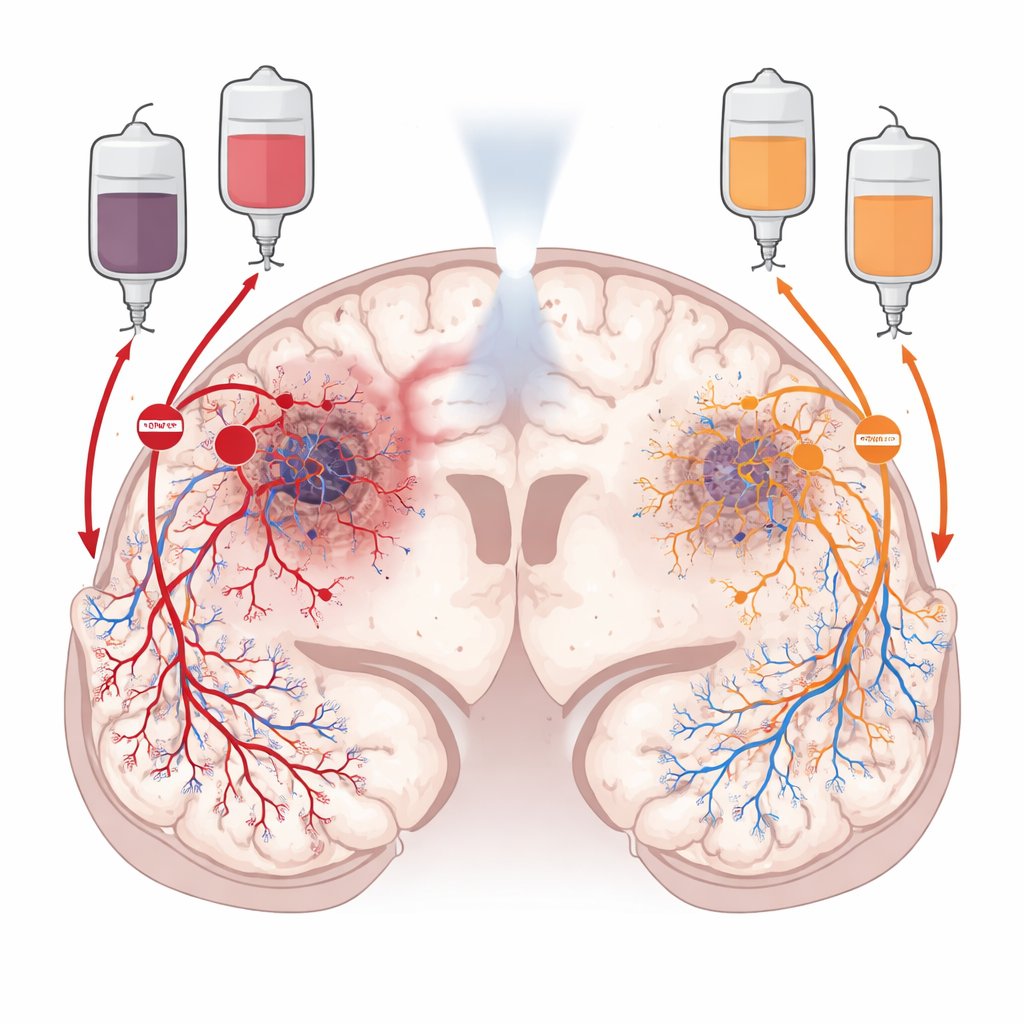
Två dolda vägar som matar tumören
Efter strålbehandling sitter glioblastom inte stilla. Tumören omformar aktivt sin omgivning för att återställa blodflödet. Den ena vägen, kallad angiogenes, bygger på ett tillväxtsignal som får närliggande blodkärl att skjuta ut nya grenar in i tumören. Den andra, kallad vaskulogenes, rekryterar nya blodkärlsbildande celler från benmärgen, som söker sig till tumören och bygger nya kärl från grunden. Forskarna fokuserade på två kemiska ”trafikledare” som styr dessa vägar: VEGF, som driver lokal kärlutsprång, och CXCL12, som attraherar cirkulerande progenitor- och immunceller och hjälper dem att etablera sig i tumören. Eftersom dessa signaler verkar i olika delar av tumören resonerade teamet att blockering av båda kunde svälta ut cancern mer effektivt än att blockera endera ensam.
Kartläggning av var signalerna verkar i mänskliga tumörer
För att se hur VEGF och CXCL12 är ordnade i glioblastom grävde forskarna i stora offentliga genetiska datamängder och vände sig sedan till högupplösta bilder av verkliga patienttumörer. De fann att VEGF följer nära syrefattiga, döende områden djupt i tumören, där skadad vävnad ropar efter nya blodkärl. CXCL12 däremot förekommer främst i mer cellrika och mycket vaskulariserade zoner samt i de yttre infiltrationsområden där tumörceller slingrar sig in i frisk hjärna. Med avancerade färgningstekniker och rumslig genprofilering visade de att CXCL12 inte bara produceras av tumörceller utan också av blodkärlens beklädnad, stödjeceller och immunceller i och runt tumören, inklusive normala hjärnans kärl. Detta stärkte idén att VEGF och CXCL12 är kompletterande, icke-överlappande drivkrafter för återuppbyggnad av blodkärl.
En studie som kombinerar strålning med en CXCL12-fälla och anti-VEGF-behandling
Med utgångspunkt i tidigare arbete med ett CXCL12-blockerande läkemedel kallat NOX-A12, rekryterade GLORIA-studien vuxna med nyligen diagnostiserat glioblastom vars tumörer inte kunde avlägsnas helt och som saknade en DNA-markör som gör standardkemoterapi effektiv. Alla patienter fick strålbehandling och kontinuerlig intravenös NOX-A12. I en expansionsfas fick en undergrupp om sex patienter också bevacizumab, en antikropp som riktar sig mot VEGF och redan används vid återkommande glioblastom. Huvudmålet var att pröva säkerheten; teamet följde även hur länge tumörerna förblev kontrollerade, total överlevnad, förändringar i tumörblodflöde på MR och patienternas neurologiska funktion och livskvalitet.
Säkerhet och tecken på starkare, längre svar
Trippelkombinationen av strålbehandling, NOX-A12 och bevacizumab visade sig vara väl tolererad. Det förekom inga behandlingsrelaterade dödsfall och inga dosbegränsande toxiska biverkningar. De flesta biverkningar var milda till måttliga och i stor utsträckning kopplade till tumören eller till strålningen i sig; blodtrycksförhöjningar från bevacizumab kunde hanteras med medicinering. Avbildning visade att tillsatsen av bevacizumab ledde till mycket djupare minskningar i tumörblodvolym och perfusion, vilket antyder att kärligenväxten kraftigt undertrycktes. Kliniskt hade patienter på trippelterapin en median tid utan tumörprogress på strax över nio månader och en median totalöverlevnad på nästan 20 månader — båda tydligt längre än patienter som fick strålbehandling med NOX-A12 ensam, och bättre än noggrant matchade grupper behandlade med standardvård. Anmärkningsvärt nog levde två av de sex patienterna på trippelterapin mer än två år, en ovanligt lång tid för denna högriskgrupp.
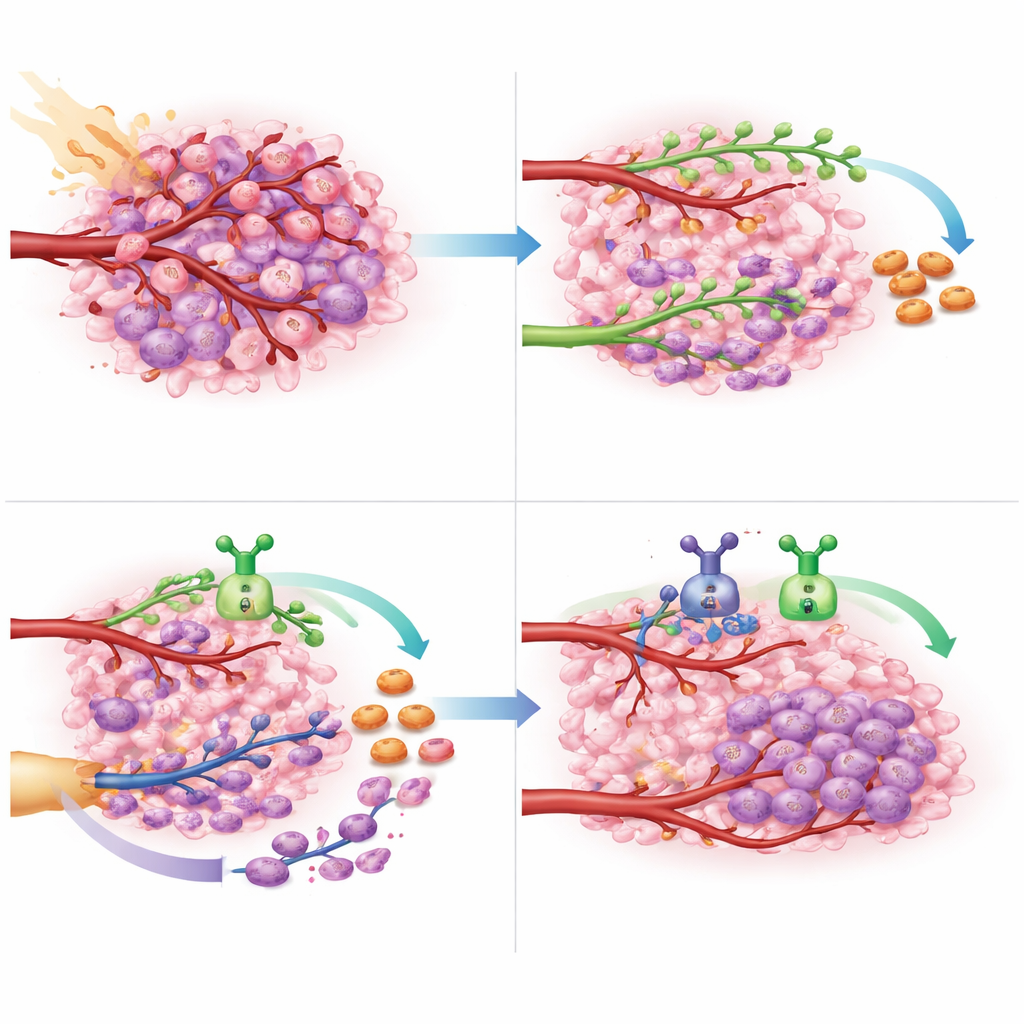
Vad detta kan betyda för framtida vård av hjärncancer
För patienter med glioblastom som inte kan avlägsnas helt och är resistent mot standardkemoterapi är alternativen få och prognosen dyster. Denna studie ger en proof-of-principle att stänga ner båda huvudvägarna för kärlreparation — VEGF-driven utsprångsbildning och CXCL12-driven rekrytering av nya kärlbildande celler — under och efter strålbehandling kan genomföras säkert och kan avsevärt fördröja tumörens återväxt. Eftersom studien var liten och främst utformad för att bedöma säkerhet är överlevnadsförbättringarna ändå tillräckligt uppmuntrande för att motivera större, randomiserade studier. Om resultaten bekräftas kan dubbelriktad inriktning på dessa två vaskulära signaler bli en ny förstalinjesstrategi för att hålla denna aggressiva hjärntumör i schack längre.
Citering: Giordano, F.A., Layer, J.P., Turiello, R. et al. L-RNA aptamer-based CXCL12 inhibition combined with radiotherapy and bevacizumab in newly-diagnosed glioblastoma: expansion of the phase I/II GLORIA trial. Nat Commun 17, 3405 (2026). https://doi.org/10.1038/s41467-026-71362-7
Nyckelord: glioblastom, hjärntumör, tumörblodkärl, strålbehandling, målinriktad behandling