Clear Sky Science · ru
Ингибирование CXCL12 на основе L-RNA аптамера в комбинации с радиотерапией и бевацизумабом при впервые диагностированной глиобластоме: расширение фазы I/II исследования GLORIA
Почему это исследование рака мозга важно
Глиобластома — одна из самых смертельных опухолей мозга, отчасти потому, что она почти всегда возвращается после лечения. Даже если хирурги удаляют максимально возможный объём опухоли и врачи проводят радиотерапию, кровоснабжение опухоли быстро восстанавливается, что позволяет раковым клеткам восстановиться. В этом исследовании проверяли новую стратегию: блокировать два разных пути, которыми опухоль восстанавливает свои сосуды, и выяснить, может ли такое двойное подавление, дополненное радиотерапией, безопасно дольше сдерживать прогрессирование у пациентов из группы высокого риска.
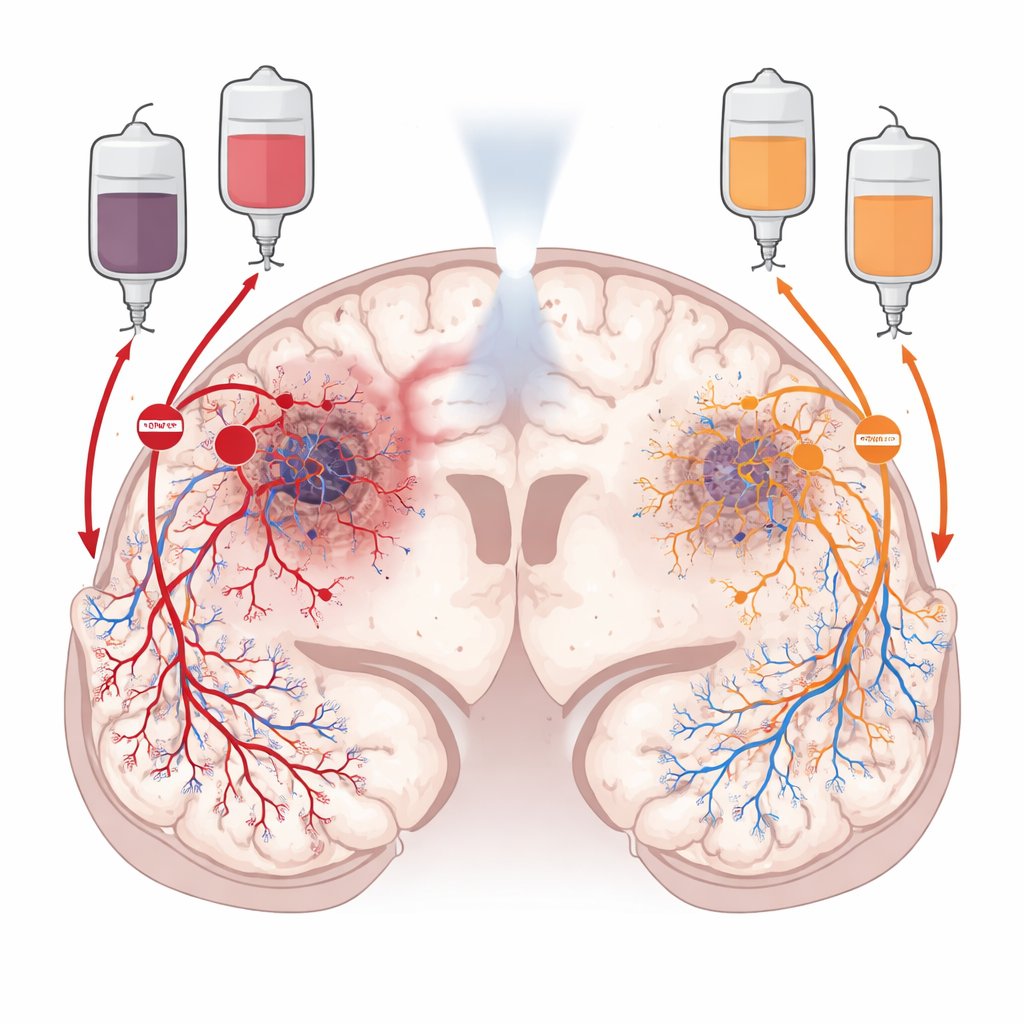
Два скрытых пути, питающие опухоль
После радиотерапии глиобластома не остаётся пассивной. Она активно перестраивает окружение, чтобы восстановить кровоток. Один путь, называемый ангиогенезом, опирается на сигналы роста, заставляющие соседние сосуды давать новые ответвления в опухоль. Другой, сосудогенез, привлекает из костного мозга клетки, формирующие сосуды, которые стягиваются к опухоли и строят новые сосуды «с нуля». Исследователи сосредоточились на двух химических «регулировщиках движения», направляющих эти маршруты: VEGF, который стимулирует местное разветвление сосудов, и CXCL12, который притягивает циркулирующие прогениторные и иммунные клетки и помогает им оседать в опухоли. Поскольку эти сигналы действуют в разных участках опухоли, команда предположила, что блокада обоих может эффектнее «истощить» опухоль, чем блокада только одного из них.
Карта распределения сигналов внутри человеческих опухолей
Чтобы увидеть, как VEGF и CXCL12 расположены внутри глиобластом, учёные проанализировали большие публичные генетические наборы данных, а затем обратились к высокоразрешающим изображениям реальных опухолей пациентов. Они обнаружили, что VEGF тесно связан с зонами низкого кислорода и умирающей ткани в глубине опухоли, где повреждённые участки остро нуждаются в новых сосудах. CXCL12, напротив, преимущественно присутствовал в более клеточных и высокососудистых зонах и в наружных зонах инфильтрации, где клетки опухоли проникают в здоровую ткань мозга. С помощью продвинутых методов окрашивания и пространственного профилирования экспрессии генов они показали, что CXCL12 вырабатывается не только самими опухолевыми клетками, но и эндотелием сосудов, поддерживающими клетками и иммунными клетками в и вокруг опухоли, включая нормальные сосуды мозга. Это укрепило представление о том, что VEGF и CXCL12 являются комплементарными, не перекрывающимися драйверами восстановления сосудов.
Исследование, комбинирующее радиацию с «ловушкой» для CXCL12 и анти-VEGF терапией
Опираясь на предыдущие работы с препаратом, блокирующим CXCL12, под названием NOX-A12, исследование GLORIA привлекло взрослых пациентов с впервые диагностированной глиобластомой, у которых опухоль нельзя было полностью удалить и у которых отсутствовал маркер в ДНК, делающий стандартную химиотерапию эффективной. Все пациенты получали радиотерапию и непрерывную внутривенную инфузию NOX-A12. На этапе расширения небольшой подгруппе из шести пациентов также назначали бевацизумаб — антитело против VEGF, уже применяемое при рецидивирующей глиобластоме. Основной целью было оценить безопасность; кроме того, команда отслеживала длительность контроля над опухолью, общую выживаемость, изменения кровотока в опухоли по МРТ, а также неврологическое состояние и качество жизни пациентов.
Безопасность и признаки более сильных, более продолжительных ответов
Тройная комбинация радиотерапии, NOX-A12 и бевацизумаба оказалась хорошо переносимой. Не было летальных исходов, связанных с лечением, и не выявлено токсичности, ограничивающей дозу. Большинство нежелательных явлений были лёгкой или умеренной степени и в основном связаны с самой опухолью или радиацией; повышение артериального давления, вызванное бевацизумабом, контролировалось лекарствами. Визуализация показала, что добавление бевацизумаба приводило к значительно более глубокому снижению объёма и перфузии опухолевой ткани, что указывает на сильное подавление повторного роста сосудов. Клинически пациенты на тройной терапии имели медиану периода без прогрессирования чуть более девяти месяцев и медиану общей выживаемости почти 20 месяцев — оба показателя явно превосходили результаты у пациентов, получавших радиотерапию с NOX-A12 без бевацизумаба, а также были лучше, чем у тщательно подобранных групп, лечившихся стандартно. Примечательно, что двое из шести пациентов на тройной терапии прожили более двух лет — необычно длительное время для этой группы высокого риска.
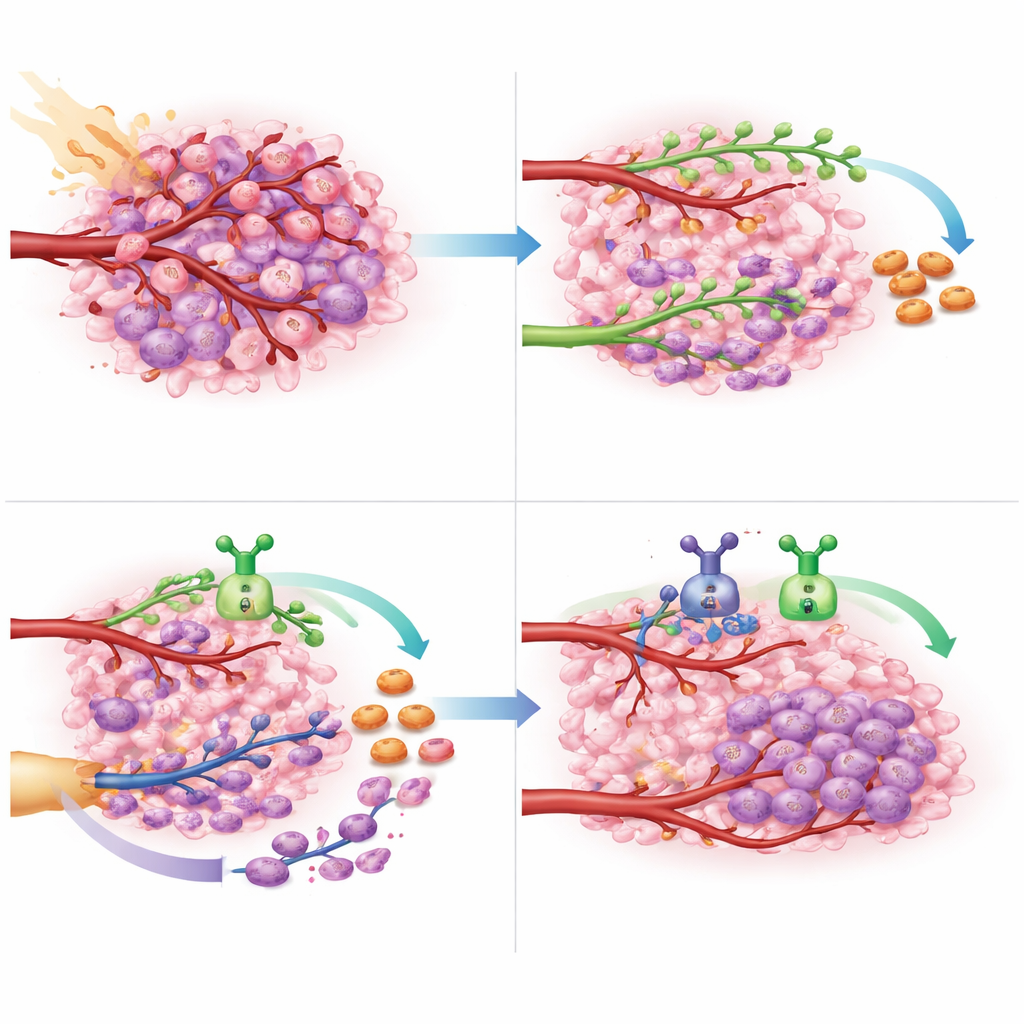
Что это может означать для будущей помощи больным раком мозга
Для пациентов с глиобластомой, которую нельзя полностью удалить и которая устойчива к стандартной химиотерапии, вариантов мало, а прогноз плох. Это исследование демонстрирует принципиальную возможность: одновременное подавление двух основных путей восстановления сосудов — разветвления, управляемого VEGF, и рекрутирования клеток‑построителей сосудов под действием CXCL12 — во время и после радиотерапии может быть безопасным и существенно отсрочить повторный рост опухоли. Поскольку исследование было небольшим и в основном нацелено на оценку безопасности, полученные приросты выживаемости достаточно обнадеживают, чтобы оправдать более крупные рандомизированные исследования. Если результаты подтвердятся, двойное таргетирование этих двух сосудистых сигналов может стать новой первой линией стратегии для более дленного сдерживания этой агрессивной опухоли мозга.
Цитирование: Giordano, F.A., Layer, J.P., Turiello, R. et al. L-RNA aptamer-based CXCL12 inhibition combined with radiotherapy and bevacizumab in newly-diagnosed glioblastoma: expansion of the phase I/II GLORIA trial. Nat Commun 17, 3405 (2026). https://doi.org/10.1038/s41467-026-71362-7
Ключевые слова: глиобластома, опухоль мозга, сосуды опухоли, радиотерапия, таргетная терапия