Clear Sky Science · it
Inibizione del CXCL12 tramite aptamero L-RNA combinata con radioterapia e bevacizumab nei glioblastomi di nuova diagnosi: espansione dello studio di fase I/II GLORIA
Perché questo studio sul cancro cerebrale è importante
Il glioblastoma è uno dei tumori cerebrali più letali, in parte perché quasi sempre recidiva dopo il trattamento. Anche quando i chirurghi rimuovono quanto più tumore possibile e i medici seguono con la radioterapia, l’apporto di sangue al tumore si ricostituisce rapidamente, permettendo alle cellule tumorali di riprendersi. Questo studio ha testato una nuova strategia: bloccare due vie differenti che il tumore utilizza per rigenerare i vasi sanguigni, e valutare se questa doppia interruzione, aggiunta alla radioterapia, possa tenere la malattia sotto controllo più a lungo in pazienti che, di norma, hanno una prognosi molto sfavorevole.
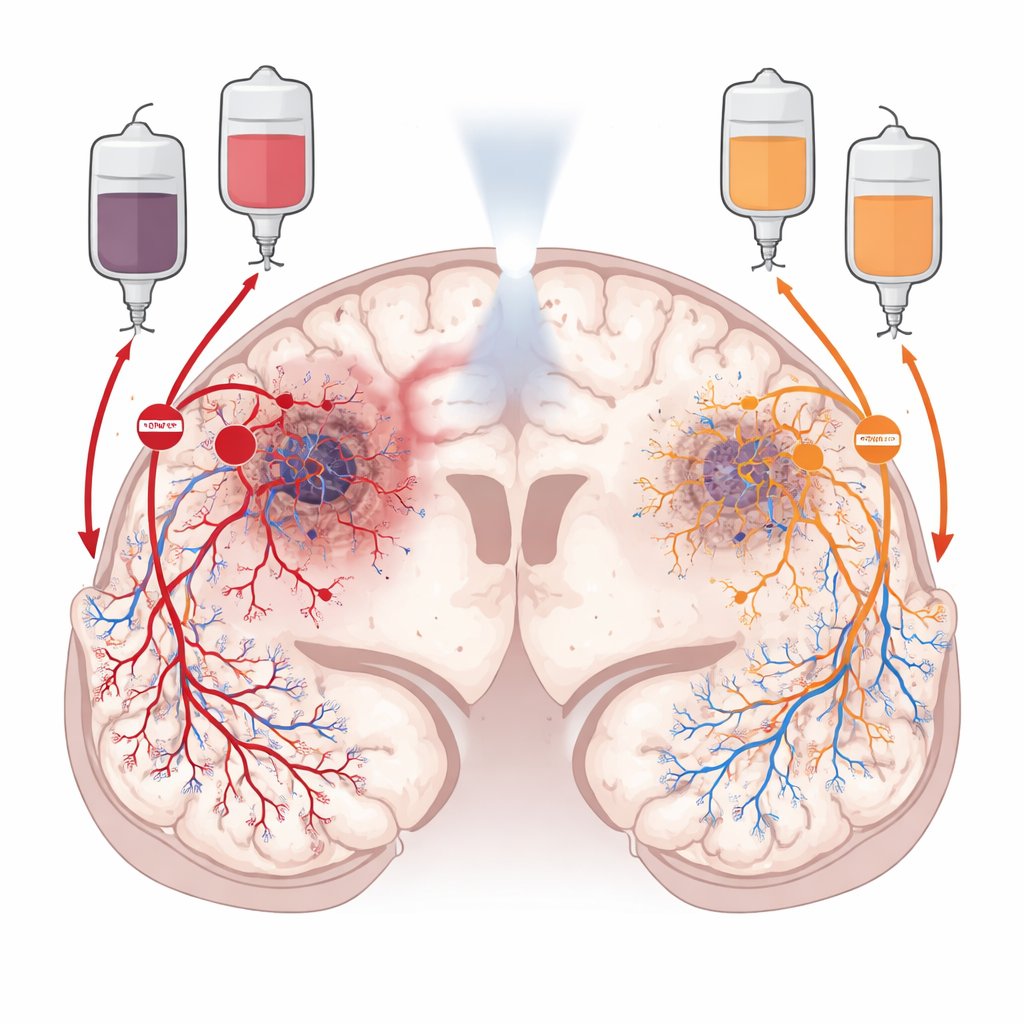
Due vie nascoste che alimentano il tumore
Dopo la radioterapia, il glioblastoma non rimane passivo. Rimodella attivamente il contesto circostante per ripristinare il flusso sanguigno. Una via, chiamata angiogenesi, dipende da un segnale di crescita che induce i vasi vicini a generare nuovi rami che penetrano nel tumore. L’altra, chiamata vasculogenesi, recluta cellule fresche capaci di formare vasi dal midollo osseo, che si dirigono verso il tumore e costruiscono nuovi vasi da zero. I ricercatori si sono concentrati su due “controllori del traffico” chimici che guidano queste vie: il VEGF, che promuove lo spuntare locale dei vasi, e il CXCL12, che attira cellule progenitrici circolanti e cellule immunitarie e ne favorisce l’insediamento nel tumore. Poiché questi segnali operano in regioni diverse del tumore, il gruppo ha ipotizzato che bloccarli entrambi potesse affamare il tumore più efficacemente rispetto all’inibizione di uno solo.
Mappare dove agiscono i segnali all’interno dei tumori umani
Per capire come VEGF e CXCL12 siano distribuiti nei glioblastomi, gli scienziati hanno analizzato ampi dataset genetici pubblici e poi si sono rivolti a immagini ad alta risoluzione di tumori reali di pazienti. Hanno scoperto che il VEGF è strettamente associato a regioni ipossiche e in necrosi nelle zone profonde del tumore, dove il tessuto danneggiato richiede urgentemente nuovi vasi. Il CXCL12, al contrario, appare soprattutto nelle zone più cellulari e altamente vascolarizzate e nelle aree periferiche di infiltrazione dove le cellule tumorali si insinuano nel cervello sano. Utilizzando tecniche avanzate di colorazione e profilazione genica spaziale, hanno dimostrato che il CXCL12 è prodotto non solo dalle cellule tumorali, ma anche dall’endotelio vascolare, dalle cellule di supporto e dalle cellule immunitarie dentro e intorno al tumore, inclusi i vasi cerebrali normali. Ciò ha rafforzato l’idea che VEGF e CXCL12 siano conducenti complementari e non sovrapposti della ricostruzione vascolare.
Uno studio che combina radioterapia con una trappola per CXCL12 e terapia anti-VEGF
Sulla base di lavori precedenti con un farmaco inibitore del CXCL12 chiamato NOX-A12, lo studio GLORIA ha arruolato adulti con glioblastoma di nuova diagnosi i cui tumori non potevano essere rimossi completamente e che erano privi di un marcatore del DNA che rende efficace la chemioterapia standard. Tutti i pazienti hanno ricevuto radioterapia e infusione endovenosa continua di NOX-A12. In una fase di espansione, un sottogruppo di sei pazienti ha ricevuto anche bevacizumab, un anticorpo che prende di mira il VEGF e già impiegato nel glioblastoma recidivante. L’obiettivo principale era valutare la sicurezza; il team ha anche monitorato per quanto tempo i tumori restavano controllati, la sopravvivenza globale, le variazioni del flusso ematico tumorale alla risonanza magnetica e la funzione neurologica e la qualità di vita dei pazienti.
Sicurezza e segnali di risposte più profonde e durature
La tripla combinazione di radioterapia, NOX-A12 e bevacizumab si è dimostrata ben tollerata. Non ci sono stati decessi correlati al trattamento né eventi tossici dose-limitanti. La maggior parte degli eventi avversi è stata lieve o moderata e in gran parte correlata al tumore o alla radioterapia stessa; gli aumenti della pressione arteriosa dovuti al bevacizumab sono stati gestibili con farmaci. Le immagini hanno mostrato che l’aggiunta di bevacizumab ha prodotto cali molto più marcati del volume ematico tumorale e della perfusione, suggerendo che la ricrescita dei vasi è stata fortemente soppressa. Sul piano clinico, i pazienti sottoposti alla tripla terapia hanno avuto un intervallo mediano senza progressione di poco superiore ai nove mesi e una sopravvivenza globale mediana di quasi 20 mesi—entrambi chiaramente più lunghi rispetto ai pazienti trattati con radioterapia e NOX-A12 da soli, e migliori rispetto a gruppi attentamente accoppiati trattati con le cure standard. Notevolmente, due dei sei pazienti in tripla terapia hanno vissuto più di due anni, un periodo insolitamente lungo per questa popolazione ad alto rischio.
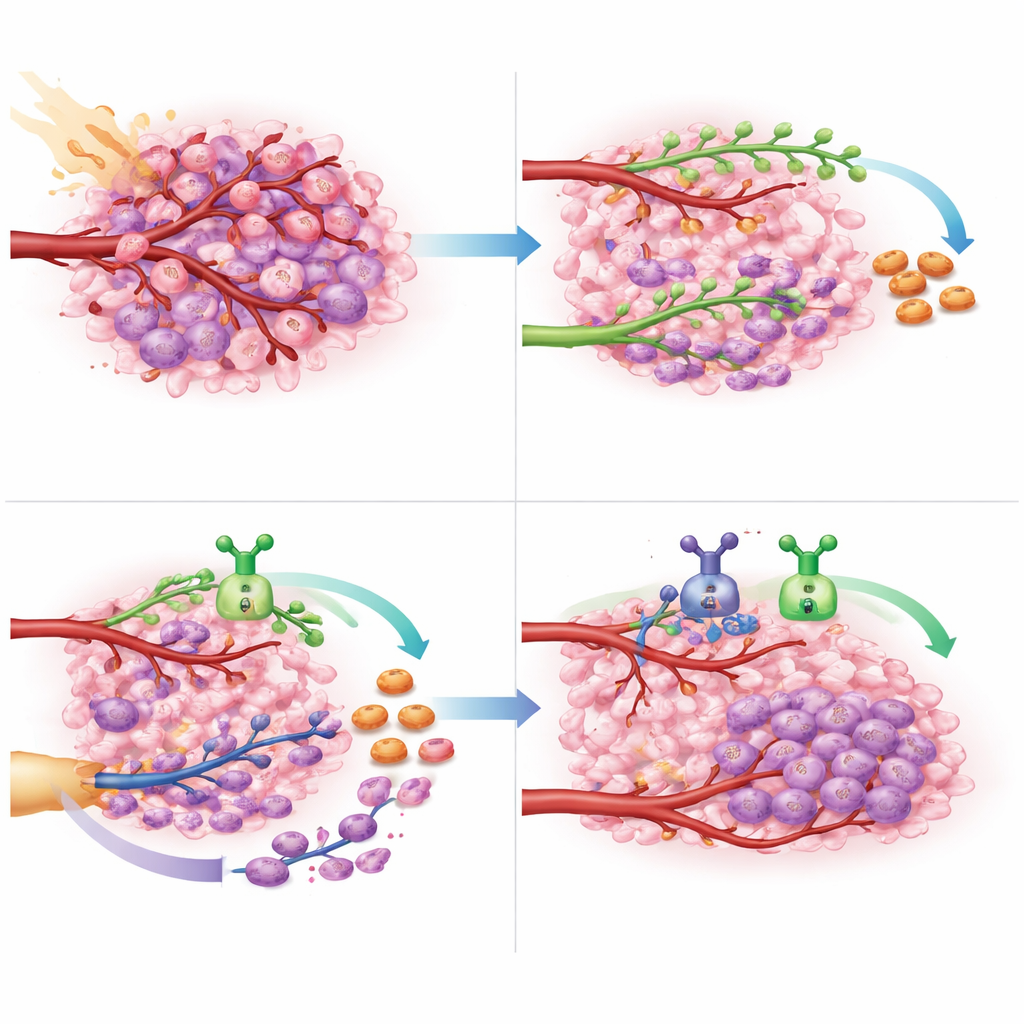
Cosa potrebbe significare per la cura futura del cancro cerebrale
Per i pazienti con glioblastoma non completamente asportabile e resistente alla chemioterapia standard, le opzioni sono scarse e gli esiti sono gravi. Questo studio fornisce una prova di principio che bloccare entrambe le principali vie di riparazione vascolare—la spinta allo spuntare dei vasi mediata da VEGF e il reclutamento mediante CXCL12 di nuove cellule formanti vasi—durante e dopo la radioterapia è fattibile in sicurezza e può ritardare in modo sostanziale la ricrescita tumorale. Sebbene lo studio fosse piccolo e progettato principalmente per valutare la sicurezza, i guadagni di sopravvivenza sono abbastanza incoraggianti da giustificare studi più ampi e randomizzati. Se confermata, la doppia modulazione di questi due segnali vascolari potrebbe diventare una nuova strategia di prima linea per contenere più a lungo questo tumore cerebrale aggressivo.
Citazione: Giordano, F.A., Layer, J.P., Turiello, R. et al. L-RNA aptamer-based CXCL12 inhibition combined with radiotherapy and bevacizumab in newly-diagnosed glioblastoma: expansion of the phase I/II GLORIA trial. Nat Commun 17, 3405 (2026). https://doi.org/10.1038/s41467-026-71362-7
Parole chiave: glioblastoma, cancro al cervello, vasi tumorali, radioterapia, terapia mirata