Clear Sky Science · zh
辅助亚基重塑异四聚体GluA1/A2 AMPA受体核心的结构不对称性和功能可塑性
大脑信号门控如何影响学习与疾病
每一个想法、记忆或动作都依赖于让带电原子在神经细胞间流动的微小蛋白质机器。本研究聚焦于大脑中最重要的此类机器之一——GluA1/A2 AMPA受体——并揭示了小型辅助蛋白如何微妙地改变其形状与行为。理解这些变化可能为治疗癫痫、中风和阿尔茨海默病等疾病提供更安全、更精确的药物途径。
大脑的快速开关
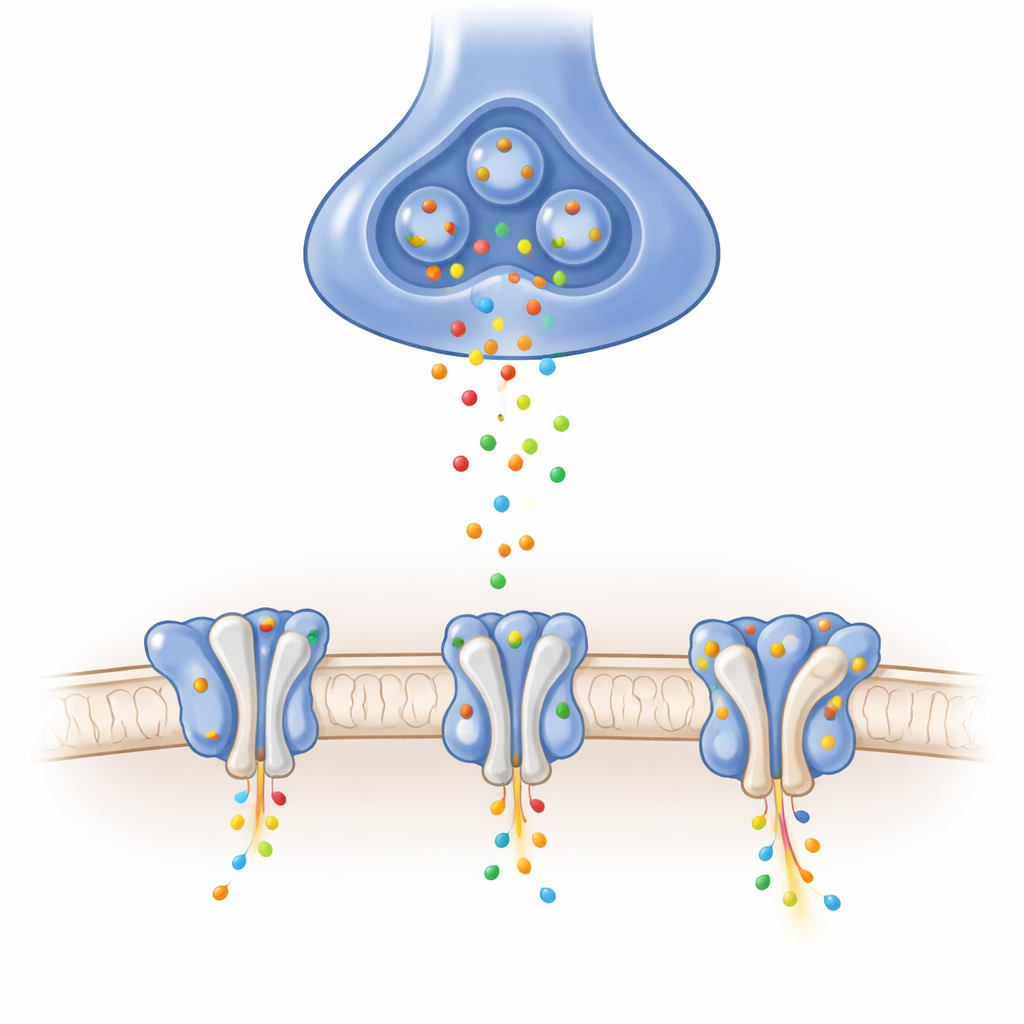
在大脑中,许多兴奋性信号由位于突触受体膜上的AMPA受体传递。当化学信使谷氨酸到达时,这些受体会打开一个孔,使带正电的离子短暂涌入细胞,在几毫秒内产生电信号。每个受体的确切组成,以及哪些辅助蛋白附着在其侧面,会调节它开启和关闭的速度、电流大小以及在频繁使用后如何恢复。其中一种特定组合——称为GluA1/A2异四聚体——在海马等关键学习中枢中占主导地位,但在没有任何辅助蛋白附着时的详细结构一直难以描绘清楚。
捕捉受体的三种关键构象
作者们利用高分辨率冷冻电子显微镜纯化了GluA1/A2受体,并将其固定在三种基本功能构象中:关闭且准备响应、打开且导电,以及失活——在长时间刺激后进入的一种保护性、暂时失去响应的状态。他们通过电生理记录验证了略作工程改造的受体在行为上与天然受体非常相似。图像显示出由四个亚基成对排列构成的Y形结构,更重要的是,清晰解析出了构成离子选择滤器一部分的短环,这一区域在许多早期结构中曾模糊不清。这些基线构象展示了谷氨酸诱导的配体结合“蛤壳”如何牵动连接子并撬开该生理学上关键受体的通道门。
辅助蛋白拓宽通道门
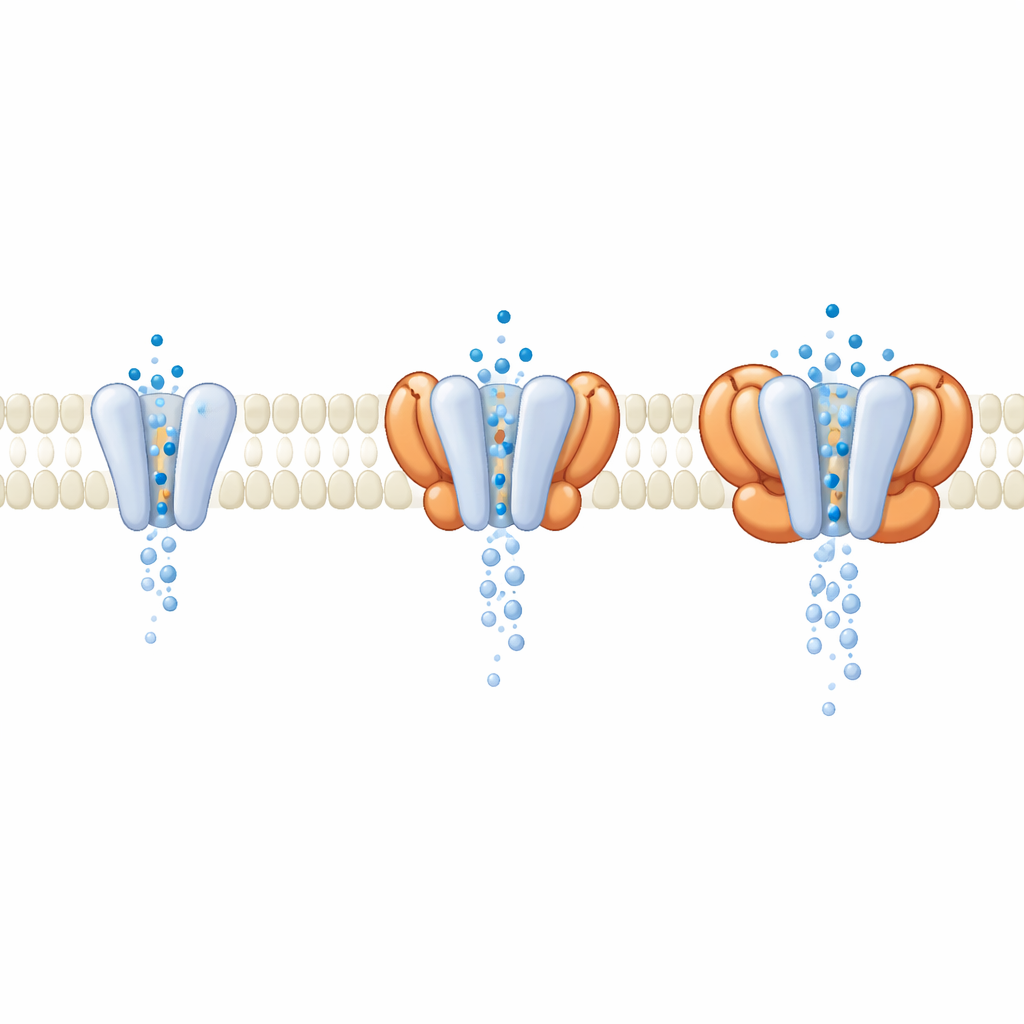
在细胞中,GluA1/A2很少单独行动;它通常伴随在膜侧的辅助蛋白。数据处理过程中,研究者发现一部分受体天然地结合了来自表达细胞的四个cornichon (CNIH) 辅助单元。将这些带有辅助蛋白的复合体与裸核心相比,他们发现当通道打开时,外层负责信号识别的部分几乎相同。关键差异出现在膜更深处,CNIH及相关辅助家族改变了孔本身的几何形状。对水分子通过通道流动的分子动力学模拟显示,含有特定辅助蛋白的复合体产生了更宽、更易水化的孔和更高的模拟导电性,尽管感知谷氨酸的结构域几乎没有变化。这表明许多调节因子并非通过改变受体如何感知谷氨酸来发挥作用,而是通过重塑离子通过的门来调节功能。
不对称性与恢复的艺术
团队还研究了受体失活时的状态——仍与谷氨酸结合但不再导电。在这一构象中,蛤壳重新排列,使在活性状态下将它们连接在一起的界面裂开,而蛤壳的下半部仍然保持足够接近以保持孔关闭。通过将GluA1/A2与多种已解析的、包含不同辅助蛋白的AMPA受体复合体比较,作者们量化了每对蛤壳从整齐的二重对称中扭曲的程度。他们发现了强相关性:这种扭曲越大,受体从失活中恢复并再次准备响应的速度越慢。有些辅助蛋白保持二聚体近乎对称,从而允许快速恢复;而另一些则促进畸变,从而延长无响应时间。
对调节脑回路与治疗的启示
这些结构和模拟结果共同表明,核心亚基的身份以及特定的辅助蛋白组合协同决定了AMPA受体如何门控电信号。辅助单元可以扩展或收窄孔径,并控制受体在频繁使用后保持沉默的时间长度,而不必改变对谷氨酸的感知方式。鉴于AMPA受体功能失调与癫痫发作、中风损伤和神经退行性疾病相关,受体—辅助界面和门控活动部位的详细图谱突出了有前景的新药物靶点。未来的药物或许不再广泛阻断这些关键受体,而是精细调整特定组装体,微妙地改变离子流动与恢复速度,精确作用于需要干预的回路。
引用: Yen, L.Y., Newton, T.P., Yelshanskaya, M.V. et al. Auxiliary subunits reshape structural asymmetry and functional plasticity in heterotetrameric GluA1/A2 AMPA receptor core. Nat Commun 17, 4191 (2026). https://doi.org/10.1038/s41467-026-71063-1
关键词: AMPA受体, 突触可塑性, 辅助亚基, 低温电子显微镜, 离子通道门控