Clear Sky Science · pt
Subunidades auxiliares remodelam a assimetria estrutural e a plasticidade funcional no núcleo heterotetramérico do receptor AMPA GluA1/A2
Como as comportas dos sinais cerebrais moldam aprendizado e doença
Cada pensamento, memória ou movimento que você realiza depende de minúsculas máquinas proteicas que permitem que átomos carregados fluam entre neurônios. Este estudo aprofunda-se em uma das mais importantes dessas máquinas no cérebro — o receptor AMPA GluA1/A2 — e revela como pequenas proteínas auxiliares alteram sutilmente sua forma e comportamento. Compreender essas mudanças pode abrir caminho para medicamentos mais seguros e precisos para condições como epilepsia, AVC e doença de Alzheimer.
Os interruptores rápidos do cérebro
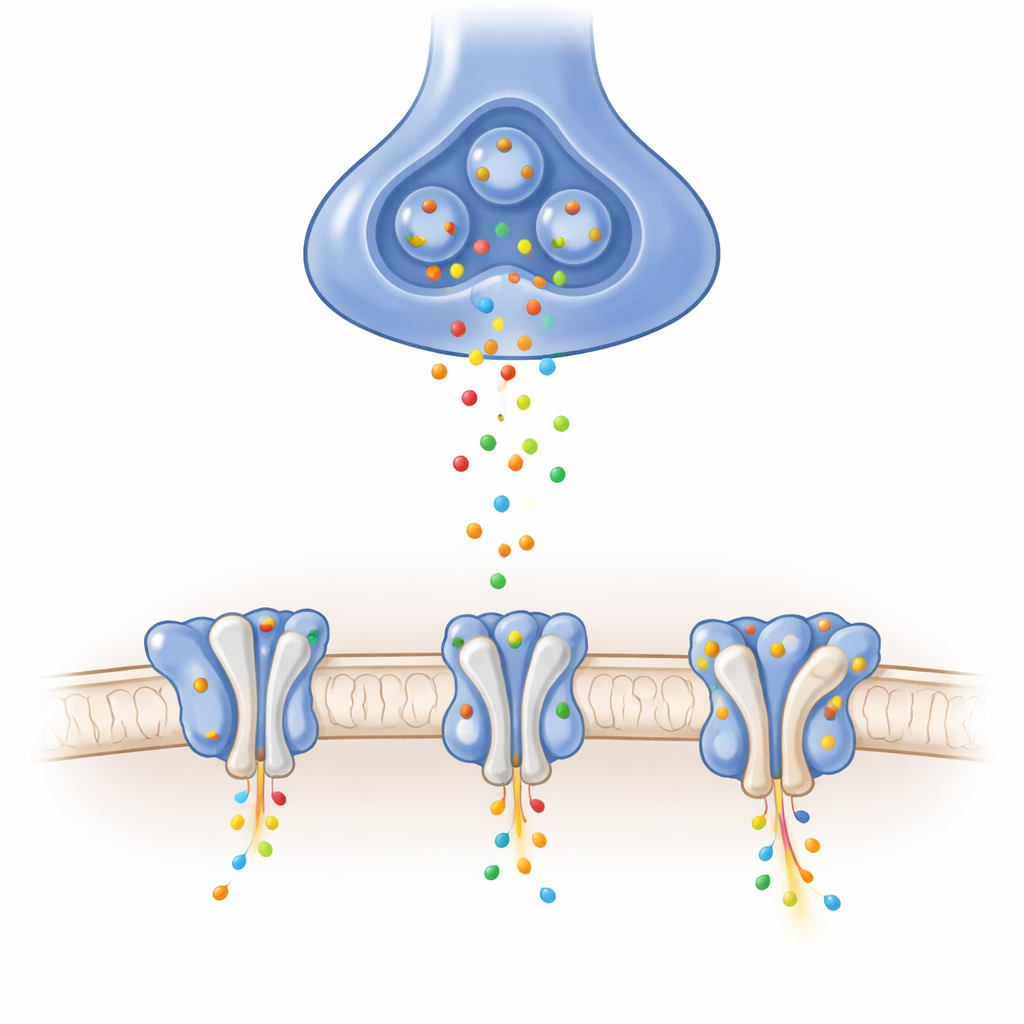
No cérebro, muitos sinais excitatórios são conduzidos por receptores AMPA, que se situam na membrana receptora das sinapses. Quando o mensageiro químico glutamato chega, esses receptores abrem um poro que permite brevemente a entrada de íons positivamente carregados na célula, produzindo sinais elétricos em questão de milissegundos. A composição exata de cada receptor, e quais proteínas auxiliares o acompanham, ajusta quão rápido ele se abre e fecha, quanta corrente passa e como ele se recupera após uso intenso. Uma combinação particular, chamada heterotetrâmero GluA1/A2, é a forma dominante em centros de aprendizagem como o hipocampo, embora sua estrutura detalhada sem auxiliares permanecesse elusiva.
Capturando o receptor em três poses-chave
Usando crio‑microscopia eletrônica em alta resolução, os autores purificaram receptores GluA1/A2 e os aprisionaram em três poses funcionais essenciais: fechado e pronto para responder, aberto e conduzindo íons, e dessensibilizado — um estado protetor e temporariamente não responsivo após estimulação prolongada. Eles verificaram por meio de registros elétricos que seus receptores ligeiramente modificados se comportavam de forma muito semelhante aos naturais. As imagens revelaram uma arquitetura em Y construída por quatro subunidades dispostas em pares e, crucialmente, resolveram com clareza o curto laço que compõe parte do filtro de seletividade iônica, uma região que havia ficado borrada em muitas estruturas anteriores. Essas visões de referência mostram como movimentos induzidos pelo glutamato nas “conchas” de ligação ao ligante puxam os conectores e abrem a comporta do canal neste receptor central fisiologicamente.
Proteínas auxiliares alargam a comporta
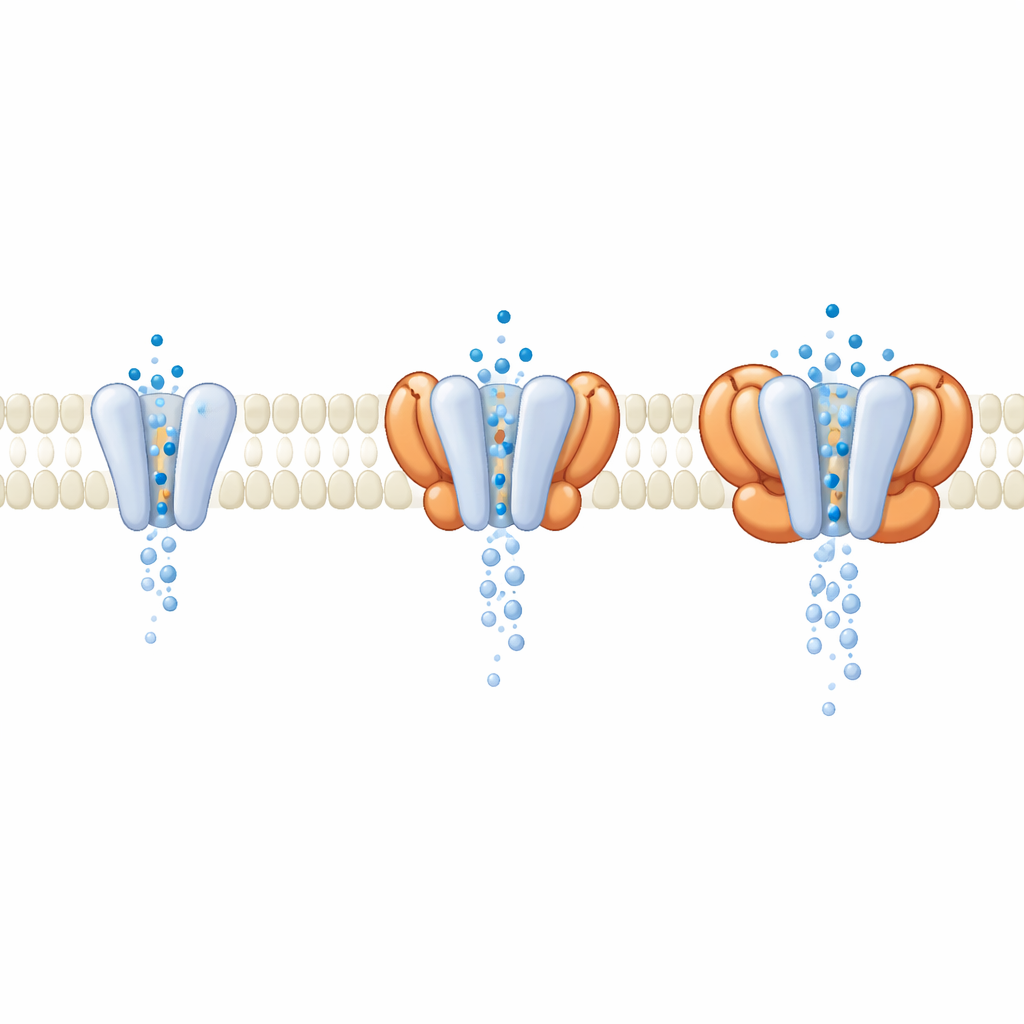
Nas células, o GluA1/A2 raramente atua sozinho; costuma ser acompanhado por proteínas auxiliares que se alojam na membrana ao seu lado. Durante o processamento dos dados, os pesquisadores descobriram um subconjunto de receptores ligado naturalmente a quatro unidades cornichon (CNIH) trazidas pelas células de expressão. Comparando esses receptores com auxiliares ao núcleo nu, eles observaram que as partes externas, responsáveis pela detecção do sinal, pareciam quase idênticas quando o canal estava aberto. As diferenças-chave surgiram mais profundamente na membrana, onde o CNIH e famílias auxiliares relacionadas alteravam a geometria do próprio poro. Simulações de dinâmica molecular do fluxo de água através do canal mostraram que complexos contendo certos auxiliares produziam um poro mais largo, melhor hidratado e com maior condutância simulada, mesmo que os domínios sensíveis ao glutamato mal se alterassem. Isso sugere que muitos moduladores atuam não mudando como os receptores detectam glutamato, mas remodelando a comporta pela qual os íons passam.
Assimetria e a arte da recuperação
A equipe também examinou o que acontece quando o receptor se dessensibiliza — ainda ligado ao glutamato, mas sem conduzir. Nessa pose, as conchas rearranjam‑se de modo que a interface que as mantém juntas no estado ativo se abre, enquanto suas metades inferiores permanecem próximas o suficiente para manter o poro fechado. Ao comparar GluA1/A2 com uma variedade de complexos de receptores AMPA já resolvidos contendo diferentes proteínas auxiliares, os autores quantificaram o quanto cada par de conchas gira, rompendo uma simetria de dois‑dois perfeita. Eles encontraram uma correlação forte: quanto maior esse giro, mais lenta é a recuperação do receptor da dessensibilização e mais tempo leva para ficar pronto para responder novamente. Alguns auxiliares mantêm o dímero quase simétrico, permitindo recuperação rápida, enquanto outros promovem distorção e, assim, prolongam a não responsividade.
Implicações para ajustar circuitos cerebrais e terapias
Em conjunto, esses resultados estruturais e de simulação mostram que tanto a identidade das subunidades centrais quanto o conjunto particular de proteínas auxiliares definem como os receptores AMPA regulam sinais elétricos. Unidades auxiliares podem alargar ou estreitar o poro e controlar quanto tempo os receptores permanecem silenciosos após uso intenso, sem necessariamente alterar como o glutamato é detectado. Como o mau funcionamento dos receptores AMPA está ligado a distúrbios convulsivos, danos por AVC e neurodegeneração, os mapas detalhados das interfaces receptor–auxiliar e das partes móveis da comporta destacam novos alvos promissores para fármacos. Em vez de bloquear amplamente esses receptores cruciais, medicamentos futuros poderão ajustar finamente montagens específicas, modulando sutilmente o fluxo iônico e a recuperação exatamente nos circuitos que precisam disso.
Citação: Yen, L.Y., Newton, T.P., Yelshanskaya, M.V. et al. Auxiliary subunits reshape structural asymmetry and functional plasticity in heterotetrameric GluA1/A2 AMPA receptor core. Nat Commun 17, 4191 (2026). https://doi.org/10.1038/s41467-026-71063-1
Palavras-chave: receptor AMPA, plasticidade sináptica, subunidades auxiliares, crio microscopia eletrônica, abertura de canal iônico