Clear Sky Science · de
Auxiliäre Untereinheiten formen strukturelle Asymmetrie und funktionelle Plastizität im heterotetrameren GluA1/A2-AMPA-Rezeptorkern
Wie Gehirnsignal-Gates Lernen und Krankheit formen
Jeder Gedanke, jede Erinnerung und jede Bewegung beruht auf winzigen Proteinmaschinen, die geladene Atome zwischen Nervenzellen fließen lassen. Diese Studie fokussiert auf eine der wichtigsten dieser Maschinen im Gehirn — den GluA1/A2-AMPA-Rezeptor — und zeigt, wie kleine Helferproteine seine Form und sein Verhalten fein verändern. Das Verständnis dieser Veränderungen könnte Wege zu sichereren, präziseren Arzneien bei Erkrankungen wie Epilepsie, Schlaganfall und Alzheimer eröffnen.
Die schnellen Schalter des Gehirns
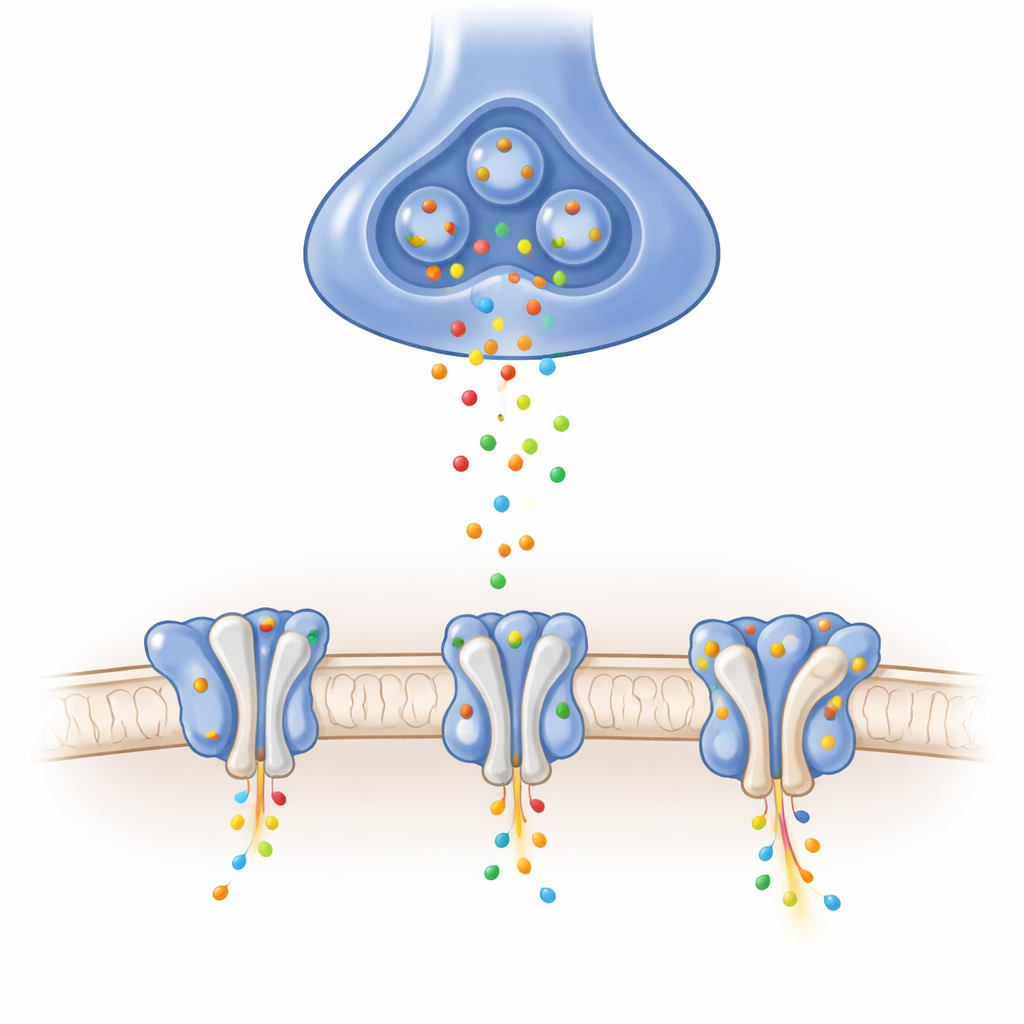
Im Gehirn werden viele exzitatorische Signale durch AMPA-Rezeptoren vermittelt, die in der postsynaptischen Membran sitzen. Wenn der Botenstoff Glutamat ankommt, öffnen diese Rezeptoren eine Pore, die kurzzeitig positiv geladene Ionen in die Zelle strömen lässt und so innerhalb von Millisekunden elektrische Signale erzeugt. Die genaue Zusammensetzung jedes Rezeptors und welche Helferproteine an seinen Seiten anhaften, bestimmt, wie schnell er sich öffnet und schließt, wie viel Strom fließt und wie er sich nach intensiver Nutzung erholt. Eine besondere Kombination, der GluA1/A2-Heterotetramer, ist die vorherrschende Form in wichtigen Lernzentren wie dem Hippocampus, doch seine detaillierte Struktur ohne gebundene Helfer blieb bislang schwer fassbar.
Den Rezeptor in drei Schlüsselposen einfangen
Mithilfe hochauflösender Kryo‑Elektronenmikroskopie reinigten die Autoren GluA1/A2-Rezeptoren und fixierten sie in drei wesentlichen funktionellen Zuständen: geschlossen und bereit zur Reaktion, geöffnet und leitend, sowie desensibilisiert — ein schützender, vorübergehend nicht reagierender Zustand nach anhaltender Stimulation. Elektrische Messungen bestätigten, dass die leicht modifizierten Rezeptoren sich ähnlich wie natürliche verhalten. Die Aufnahmen zeigten eine Y-förmige Architektur aus vier Untereinheiten, die paarweise angeordnet sind, und lösten entscheidend die kurze Schleife auf, die Teil des Ionenselektivitätsfilters bildet — ein Bereich, der in vielen früheren Strukturen verschwommen war. Diese Basisansichten zeigen, wie glutamatinduzierte Bewegungen in den Ligandenbindungs‑„Muscheln“ an Verbindungsstücken ziehen und das Kanalgate in diesem physiologisch zentralen Rezeptor aufdrücken.
Helferproteine weiten das Gate
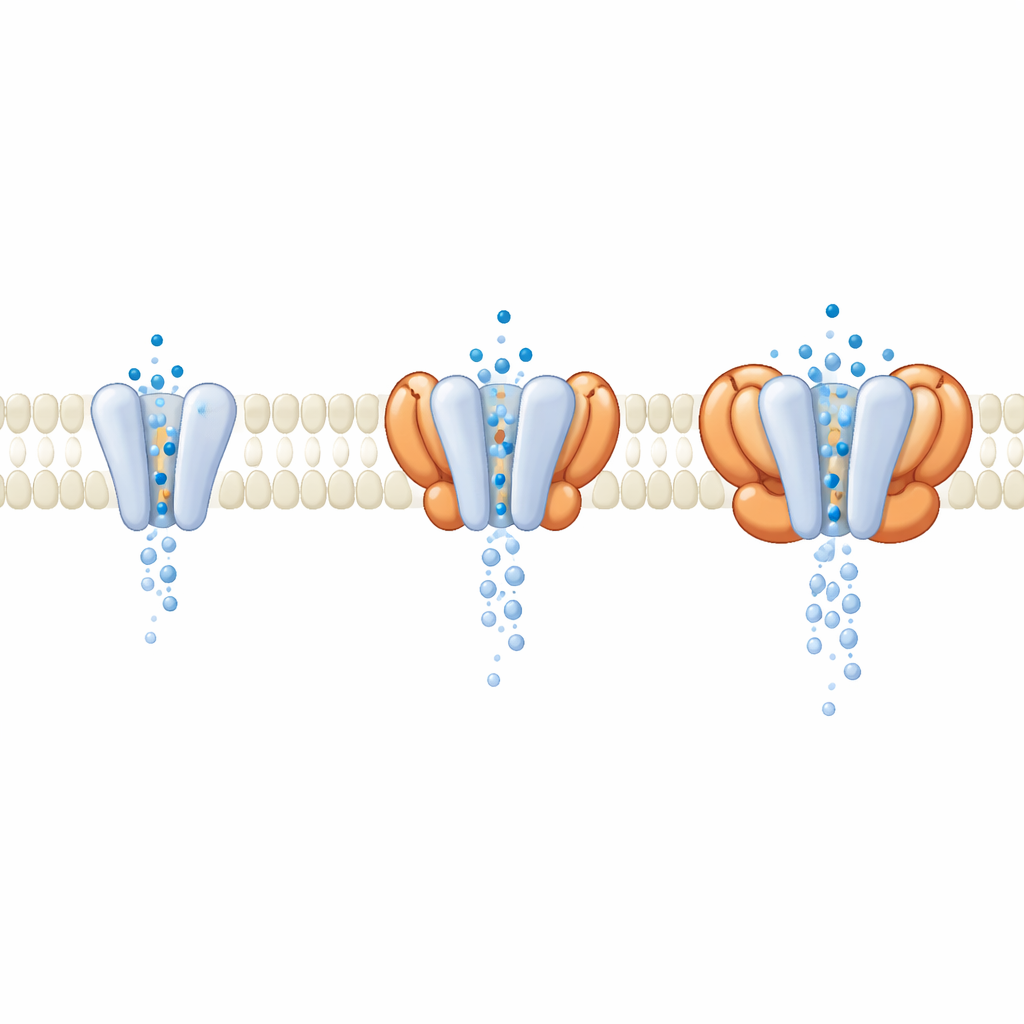
Im Zellkontext wirkt GluA1/A2 selten allein; üblicherweise sind auxiliäre Proteine in der Membran daneben eingebettet. Bei der Datenverarbeitung entdeckten die Forscher eine Untergruppe von Rezeptoren, die natürlich mit vier Cornichon-(CNIH)-Helfereinheiten aus den Expressionszellen behaftet waren. Im Vergleich der mit Helfern beladenen Komplexe mit dem nackten Kern zeigten die äußeren, signalerkennenden Domänen im geöffneten Zustand fast identische Erscheinungen. Die entscheidenden Unterschiede traten tiefer in der Membran auf, wo CNIH und verwandte Helferfamilien die Geometrie der Pore veränderten. Molekulardynamik-Simulationen des Wasserflusses durch den Kanal zeigten, dass Komplexe mit bestimmten Helfern eine weitere, besser hydratisierte Pore und eine höhere simulierte Leitfähigkeit erzeugten, obwohl die glutamaterkennenden Domänen kaum verändert waren. Das legt nahe, dass viele Modulatoren nicht primär die Glutamaterkennung ändern, sondern das Gate umgestalten, durch das die Ionen fließen.
Asymmetrie und die Kunst der Erholung
Das Team untersuchte außerdem den desensibilisierten Zustand — noch an Glutamat gebunden, aber nicht leitend. In dieser Pose ordnen sich die Muscheln so um, dass die Schnittstelle, die sie im aktiven Zustand zusammenhält, aufbricht, während ihre unteren Hälften nahe genug bleiben, um die Pore geschlossen zu halten. Durch den Vergleich von GluA1/A2 mit einer Reihe zuvor gelöster AMPA-Rezeptor‑Komplexe mit unterschiedlichen Helferproteinen quantifizierten die Autoren, wie stark sich jedes Muschelpaar aus einer sauberen Zwei‑Fach-Symmetrie herausdreht. Sie fanden eine starke Korrelation: Je größer diese Verdrehung, desto langsamer erholt sich der Rezeptor aus der Desensibilisierung und wird wieder reagierbereit. Manche Helfer erhalten das Dimer nahezu symmetrisch und erlauben so eine schnelle Erholung, andere fördern Verzerrung und damit verlängerte Unempfindlichkeit.
Folgen für die Feinabstimmung neuronaler Schaltkreise und Therapien
Zusammen zeigen diese strukturellen und Simulations‑Ergebnisse, dass sowohl die Identität der Kernuntereinheiten als auch die genaue Zusammensetzung der Helferproteine gemeinsam bestimmen, wie AMPA-Rezeptoren elektrische Signale steuern. Helfereinheiten können die Pore weiter oder enger machen und kontrollieren, wie lange Rezeptoren nach intensiver Nutzung stumm bleiben, ohne notwendigerweise die Glutamat-Erkennung zu verändern. Da Fehlfunktionen von AMPA-Rezeptoren mit Anfallsleiden, Schlaganfallschäden und Neurodegeneration in Verbindung stehen, heben die detaillierten Karten der Rezeptor‑Helfer‑Schnittstellen und der beweglichen Teile des Gates vielversprechende neue Angriffspunkte für Medikamente hervor. Anstatt diese lebenswichtigen Rezeptoren breit zu blockieren, könnten künftige Therapien spezifische Assemblies feinjustieren und so den Ionenfluss und die Erholung gezielt in den betroffenen Schaltkreisen modulieren.
Zitation: Yen, L.Y., Newton, T.P., Yelshanskaya, M.V. et al. Auxiliary subunits reshape structural asymmetry and functional plasticity in heterotetrameric GluA1/A2 AMPA receptor core. Nat Commun 17, 4191 (2026). https://doi.org/10.1038/s41467-026-71063-1
Schlüsselwörter: AMPA-Rezeptor, synaptische Plastizität, auxiliäre Untereinheiten, Kryo-Elektronenmikroskopie, Ionenkanal-Öffnung