Clear Sky Science · pl
Podjednostki pomocnicze przekształcają asymetrię strukturalną i plastyczność funkcjonalną w heterotetramerycznym rdzeniu receptora GluA1/A2 typu AMPA
Jak bramki sygnałów mózgowych kształtują uczenie się i choroby
Każda myśl, pamięć czy ruch zależy od mikroskopijnych maszyn białkowych przepuszczających naładowane atomy między komórkami nerwowymi. To badanie przygląda się jednemu z najważniejszych takich mechanizmów w mózgu — receptorowi AMPA GluA1/A2 — i ujawnia, jak niewielkie białka pomocnicze subtelnie zmieniają jego kształt i zachowanie. Zrozumienie tych zmian może otworzyć drogę do bezpieczniejszych i bardziej precyzyjnych leków na schorzenia takie jak padaczka, udar czy choroba Alzheimera.
Szybkie przełączniki mózgu
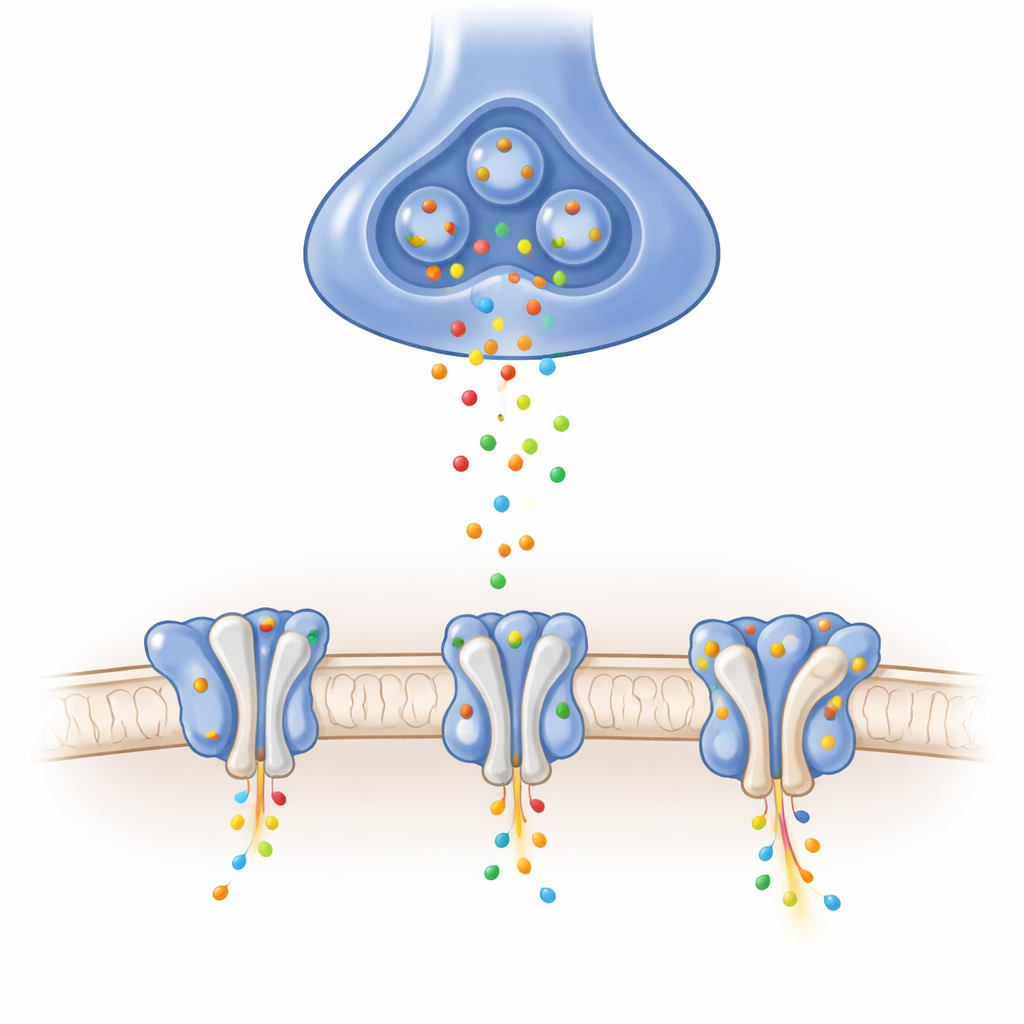
W mózgu wiele sygnałów pobudzających przekazywanych jest przez receptory AMPA, które znajdują się w błonie postsynaptycznej. Gdy pojawia się przekaźnik glutaminian, te receptory otwierają por, który na krótko pozwala dodatnio naładowanym jonom wpłynąć do komórki, generując sygnały elektryczne w ciągu zaledwie milisekund. Dokładny skład każdego receptora oraz to, które białka pomocnicze towarzyszą mu po bokach, regulują szybkość otwierania i zamykania, natężenie prądu oraz zdolność do odzyskiwania po intensywnym użyciu. Jeden szczególny zestaw, zwany heterotetramerem GluA1/A2, dominuje w kluczowych ośrodkach uczenia, takich jak hipokamp, ale szczegółowa struktura tej formy bez podjednostek pomocniczych pozostawała wcześniej nieuchwytna.
Zatrzymanie receptora w trzech kluczowych pozach
Używając wysokorozdzielczej kriomikroskopii elektronowej, autorzy oczyścili receptory GluA1/A2 i uwięzili je w trzech istotnych stanach funkcjonalnych: zamkniętym i gotowym do reakcji, otwartym przewodzącym jony oraz zdezensytyzowanym — ochronnym, tymczasowo niewrażliwym stanie po przedłużonej stymulacji. Potwierdzili za pomocą pomiarów elektrycznych, że ich lekko zmodyfikowane receptory zachowują się podobnie do naturalnych. Obrazy ujawniły architekturę w kształcie litery Y zbudowaną z czterech podjednostek ułożonych w pary i, co kluczowe, wyraźnie rozdzieliły krótką pętlę będącą częścią filtra selektywności jonowej — obszar, który w wielu wcześniejszych strukturach był rozmyty. Te widoki referencyjne pokazują, jak ruchy „muszli” wiążących ligand pod wpływem glutaminianu napinają łączniki i rozchylają zasuwnicę kanału w tym fizjologicznie istotnym receptorze.
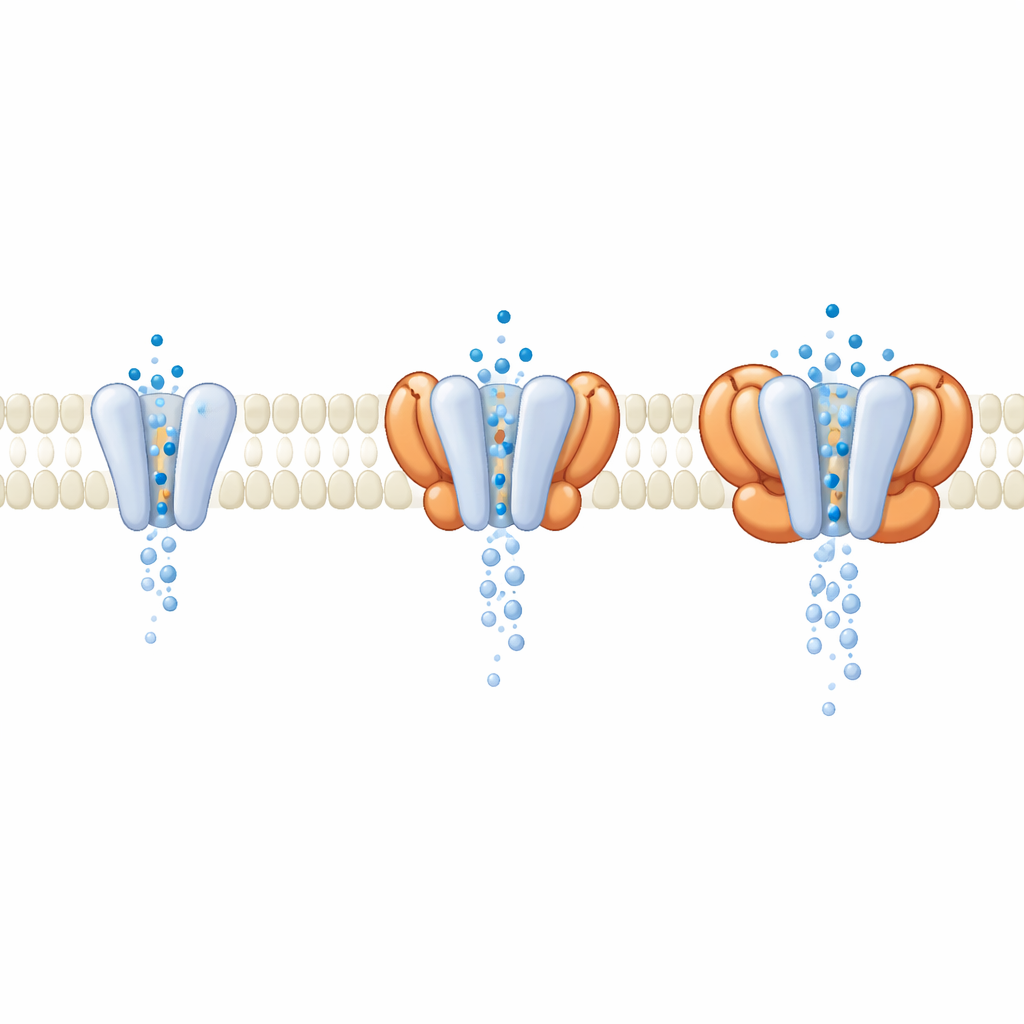
Białka pomocnicze rozszerzają zasuwnicę
W komórkach GluA1/A2 rzadko działa samotnie; zazwyczaj towarzyszą mu podjednostki pomocnicze osadzone w błonie. Podczas analizy danych badacze odkryli podzbiór receptorów naturalnie związanych z czterema jednostkami cornichon (CNIH) przeniesionymi z komórek ekspresyjnych. Porównując te receptory z pomocą z rdzeniem pozbawionym pomocników, stwierdzili, że zewnętrzne, wykrywające sygnał części wyglądały niemal identycznie w stanie otwartym. Kluczowe różnice pojawiały się głębiej w błonie, gdzie CNIH i spokrewnione rodziny modulatorów zmieniały geometrię samego poru. Symulacje dynamiki molekularnej przepływu wody przez kanał wykazały, że kompleksy zawierające określone pomocnicze jednostki tworzyły szerszy, lepiej nawodniony por i wyższą symulowaną przewodność, mimo że domeny wykrywające glutaminian prawie się nie zmieniły. Sugestia jest taka, że wielu modulatorów działa nie przez zmianę wykrywania glutaminianu, lecz przez przekształcanie bramki, przez którą przepływają jony.
Asymetria i sztuka odzyskiwania
Zespół zbadał także, co dzieje się, gdy receptor ulega zdezensytyzowaniu — nadal związany z glutaminianem, ale przestaje przewodzić. W tej pozycji muszle przeorganizowują się tak, że interfejs utrzymujący je razem w stanie aktywnym pęka, podczas gdy ich dolne połowy pozostają dostatecznie blisko, by utrzymać por zamknięty. Porównując GluA1/A2 z różnymi uprzednio rozwiązanymi kompleksami receptorów AMPA zawierającymi różne podjednostki pomocnicze, autorzy zmierzyli, jak bardzo każda para muszli odchyla się od prostego symetrycznego układu o dwukrotnej osi. Stwierdzili silną korelację: im większe to skręcenie, tym wolniejsze odzyskiwanie receptora z zdezensytyzowanego stanu i powrót do gotowości reakcji. Niektóre pomocniki utrzymują dimer niemal symetryczny, co pozwala na szybkie odzyskiwanie, podczas gdy inne sprzyjają deformacji i tym samym wydłużonej niewrażliwości.
Implikacje dla strojenia obwodów mózgowych i terapii
Razem te wyniki strukturalne i symulacyjne pokazują, że zarówno tożsamość podjednostek rdzeniowych, jak i konkretny zestaw białek pomocniczych współdziałają, aby określić, jak receptory AMPA bramkują sygnały elektryczne. Jednostki pomocnicze mogą poszerzać lub zwężać por i kontrolować, jak długo receptory pozostają nieme po intensywnym użytkowaniu, nie zmieniając przy tym koniecznie sposobu wykrywania glutaminianu. Ponieważ zaburzenia funkcji receptorów AMPA wiążą się z napadami padaczkowymi, uszkodzeniami pourazowymi po udarze i neurodegeneracją, szczegółowe mapy interfejsów między receptorem a pomocnikami oraz ruchomych części bramki wskazują obiecujące cele terapeutyczne. Zamiast szeroko blokować te kluczowe receptory, przyszłe leki mogłyby precyzyjnie modulować konkretne zespoły, subtelnie dostrajając przepływ jonów i tempo odzyskiwania w dokładnie tych obwodach, które tego potrzebują.
Cytowanie: Yen, L.Y., Newton, T.P., Yelshanskaya, M.V. et al. Auxiliary subunits reshape structural asymmetry and functional plasticity in heterotetrameric GluA1/A2 AMPA receptor core. Nat Commun 17, 4191 (2026). https://doi.org/10.1038/s41467-026-71063-1
Słowa kluczowe: receptor AMPA, plastyczność synaptyczna, podjednostki pomocnicze, kriomikroskopia elektronowa, zamknięcie kanału jonowego