Clear Sky Science · nl
Hulp-eenheden herschikken structurele asymmetrie en functionele plasticiteit in het heterotetramere GluA1/A2 AMPA-receptorcore
Hoe poorten van hersensignalen leren en ziekte vormen
Elke gedachte, herinnering of beweging berust op kleine eiwitmachines die geladen deeltjes tussen zenuwcellen laten stromen. Deze studie zoomt in op een van de belangrijkste van die machines in de hersenen — de GluA1/A2 AMPA-receptor — en laat zien hoe kleine helper-eiwitten diens vorm en gedrag subtiel veranderen. Inzicht in die veranderingen kan deuren openen naar veiligere, meer precieze geneesmiddelen voor aandoeningen zoals epilepsie, beroerte en de ziekte van Alzheimer.
De snelle schakelaars van de hersenen
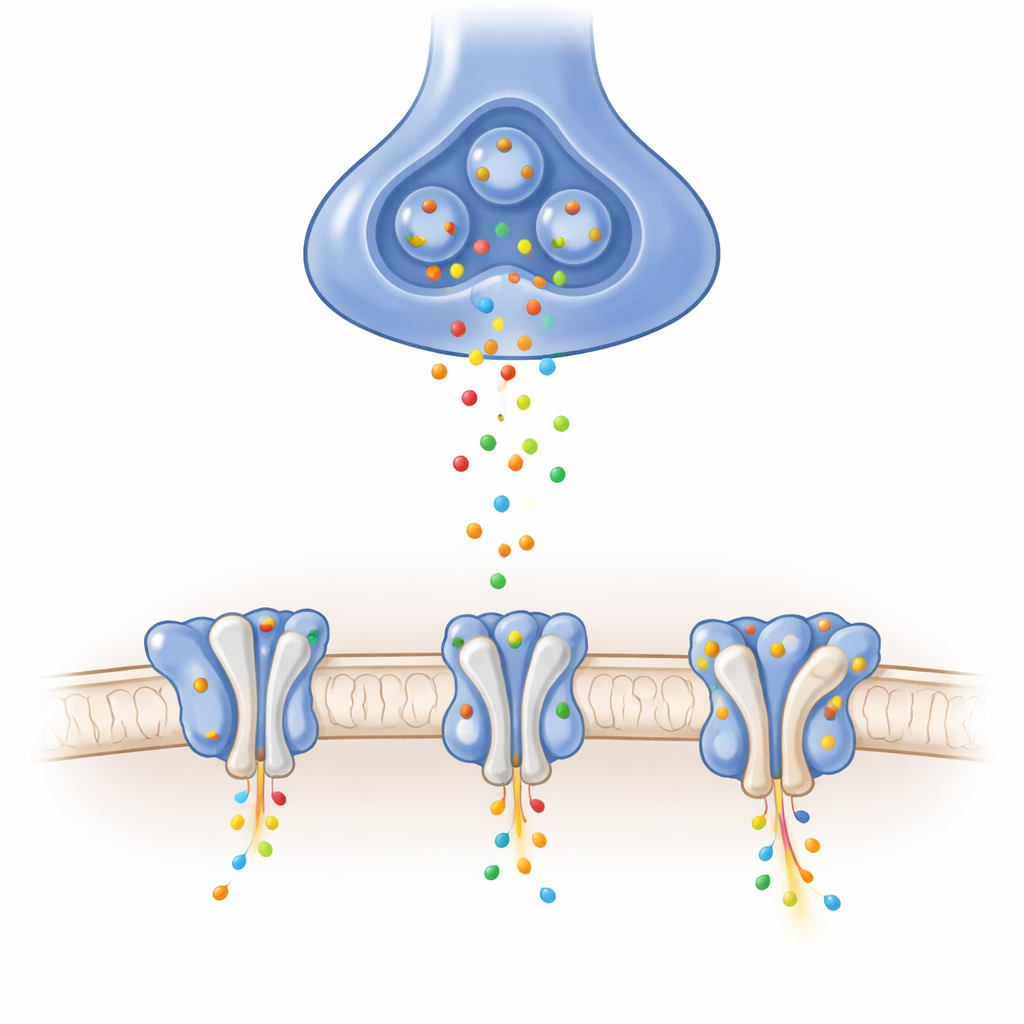
In de hersenen worden veel exciterende signalen overgedragen door AMPA-receptoren, die in het ontvangende membraan van synapsen liggen. Wanneer de chemische boodschapper glutamaat aankomt, opent deze receptor een porie die kortstondig positief geladen ionen in de cel laat stromen, waardoor in milliseconden elektrische signalen ontstaan. De precieze samenstelling van elke receptor, en welke hulp-eiwitten eraan binden, stemt af hoe snel hij opent en sluit, hoeveel stroom er doorheen gaat en hoe hij herstelt na intensief gebruik. Eén specifieke combinatie, het zogenaamde GluA1/A2-heterotetramer, is de dominante vorm in belangrijke leercentra zoals de hippocampus, maar de gedetailleerde structuur zonder hulp-eiwitten was tot nu toe onduidelijk gebleven.
De receptor vastgelegd in drie sleutelhoudingen
Met hoogresolutie cryo-elektronenmicroscopie zuiverden de onderzoekers GluA1/A2-receptoren en bevroor ze in drie essentiële functionele toestanden: gesloten en klaar om te reageren, open en ionen geleidende, en gedesensitiseerd — een beschermende, tijdelijk ongevoelige staat na langdurige stimulatie. Met elektrische opnames verifieerden zij dat hun licht aangepaste receptoren zich vergelijkbaar gedroegen als natuurlijke exemplaren. De beelden toonden een Y‑vormige architectuur van vier subunits gerangschikt als paren, en wezenlijk zichtbaar werd de korte lus die deel uitmaakt van het selectiviteitsfilter voor ionen, een regio die in veel eerdere structuren wazig was. Deze basisbeelden laten zien hoe glutamaat-geïnduceerde bewegingen in de ligand-bindende "schelpen" aan linkers trekken en het kanaalmechanisme opendoen in deze fysiologisch centrale receptor.
Hulp-eiwitten verwijden de poort
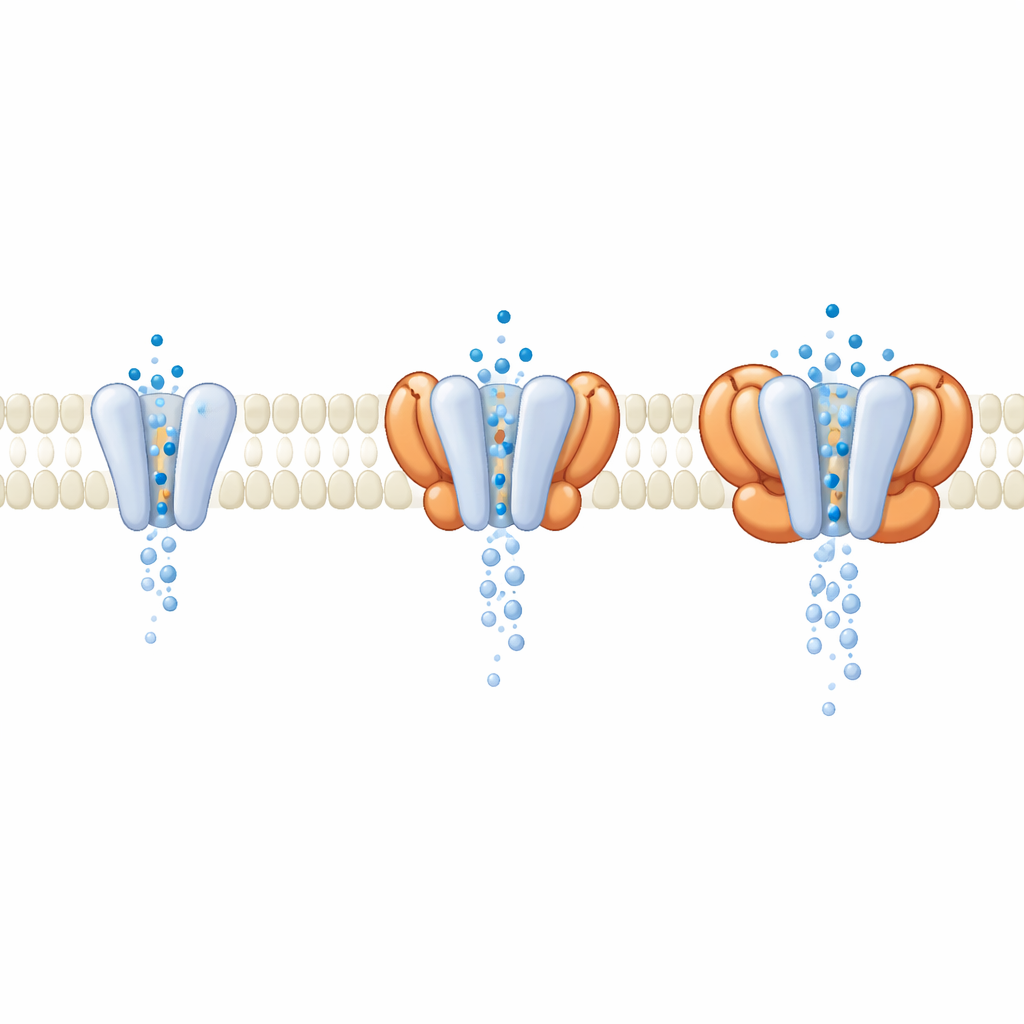
In cellen treedt GluA1/A2 zelden alleen op; doorgaans gaat het vergezeld van auxilaire eiwitten die in het membraan ernaast zitten. Tijdens de gegevensverwerking ontdekten de onderzoekers een subpopulatie receptoren die van nature gebonden waren aan vier cornichon (CNIH) helper-eenheden die waren meegekomen uit de expressiecellen. Vergelijking van deze met helpers geladen receptoren met de kale kern liet zien dat de buitenste, signaalontvangende delen vrijwel identiek waren wanneer het kanaal openstond. De belangrijke verschillen deden zich dieper in het membraan voor, waar CNIH en verwante helperfamilies de geometrie van de porie zelf veranderden. Moleculaire dynamica-simulaties van waterstroom door het kanaal toonden dat complexen met bepaalde helpers een bredere, beter gehydrateerde porie en een hogere gesimuleerde conductantie opleverden, hoewel de glutamaat-sensende domeinen nauwelijks veranderden. Dit suggereert dat veel modulatoren niet werken door de glutamaat-detectie aan te passen, maar door de poort waarlangs ionen passeren van vorm te doen veranderen.
Asymmetrie en de kunst van herstel
Het team onderzocht ook wat er gebeurt wanneer de receptor gedesensitiseerd raakt — nog steeds aan glutamaat gebonden maar niet langer geleidend. In deze houding herschikken de schelpen zich zodanig dat de interface die ze in de actieve staat bijeenhoudt opengaat, terwijl hun onderste helften dicht genoeg blijven om de porie gesloten te houden. Door GluA1/A2 te vergelijken met verschillende eerder opgeloste AMPA-receptorcomplexen die uiteenlopende helper-eiwitten bevatten, kwantificeerden de auteurs hoeveel elk paar schelpen uit een nette tweevoudige symmetrie draait. Ze vonden een sterke correlatie: hoe groter deze twist, hoe trager de receptor herstelt van desensitisatie en weer klaar is om te reageren. Sommige helpers houden het dimer bijna symmetrisch, waardoor snel herstel mogelijk is, terwijl andere vervorming bevorderen en zo langdurige ongevoeligheid veroorzaken.
Gevolgen voor het afstemmen van hersencircuits en therapieën
Gezamenlijk laten deze structurele en simulatie-resultaten zien dat zowel de identiteit van de kerneiwitten als de specifieke set helper-eenheden samen bepalen hoe AMPA-receptoren elektrische signalen gate. Helper-eenheden kunnen de porie verwijden of vernauwen en bepalen hoe lang receptoren stil blijven na intensief gebruik, zonder per se te veranderen hoe glutamaat wordt waargenomen. Omdat AMPA-receptorfunctiestoornissen gelinkt zijn aan epileptische aanvallen, beroerteletsel en neurodegeneratie, benadrukken de gedetailleerde kaarten van receptor–helperinterfaces en de bewegende onderdelen van de poort veelbelovende nieuwe geneesmiddelendoelen. In plaats van deze cruciale receptoren breed te blokkeren, zouden toekomstige medicijnen specifieke assemblages subtiel kunnen bijsturen en zo de ionstroom en het herstel precies in de circuits aanpassen die dat nodig hebben.
Bronvermelding: Yen, L.Y., Newton, T.P., Yelshanskaya, M.V. et al. Auxiliary subunits reshape structural asymmetry and functional plasticity in heterotetrameric GluA1/A2 AMPA receptor core. Nat Commun 17, 4191 (2026). https://doi.org/10.1038/s41467-026-71063-1
Trefwoorden: AMPA-receptor, synaptische plasticiteit, hulp-eenheden, cryo-elektronenmicroscopie, ionkanaal-gating