Clear Sky Science · ru
Вспомогательные субъединицы перестраивают структурную асимметрию и функциональную пластичность в гетеротетрамерном ядре AMPA-рецептора GluA1/A2
Как каналы мозговых сигналов формируют обучение и болезни
Каждая мысль, воспоминание или движение зависят от крошечных белковых машин, которые пропускают заряженные атомы между нервными клетками. В этом исследовании детально изучен один из самых важных таких комплексов мозга — AMPA‑рецептор GluA1/A2 — и показано, как мелкие вспомогательные белки тонко меняют его форму и поведение. Понимание этих изменений может открыть путь к более безопасным и точным препаратам для лечения эпилепсии, инсульта и болезни Альцгеймера.
Быстрые переключатели мозга
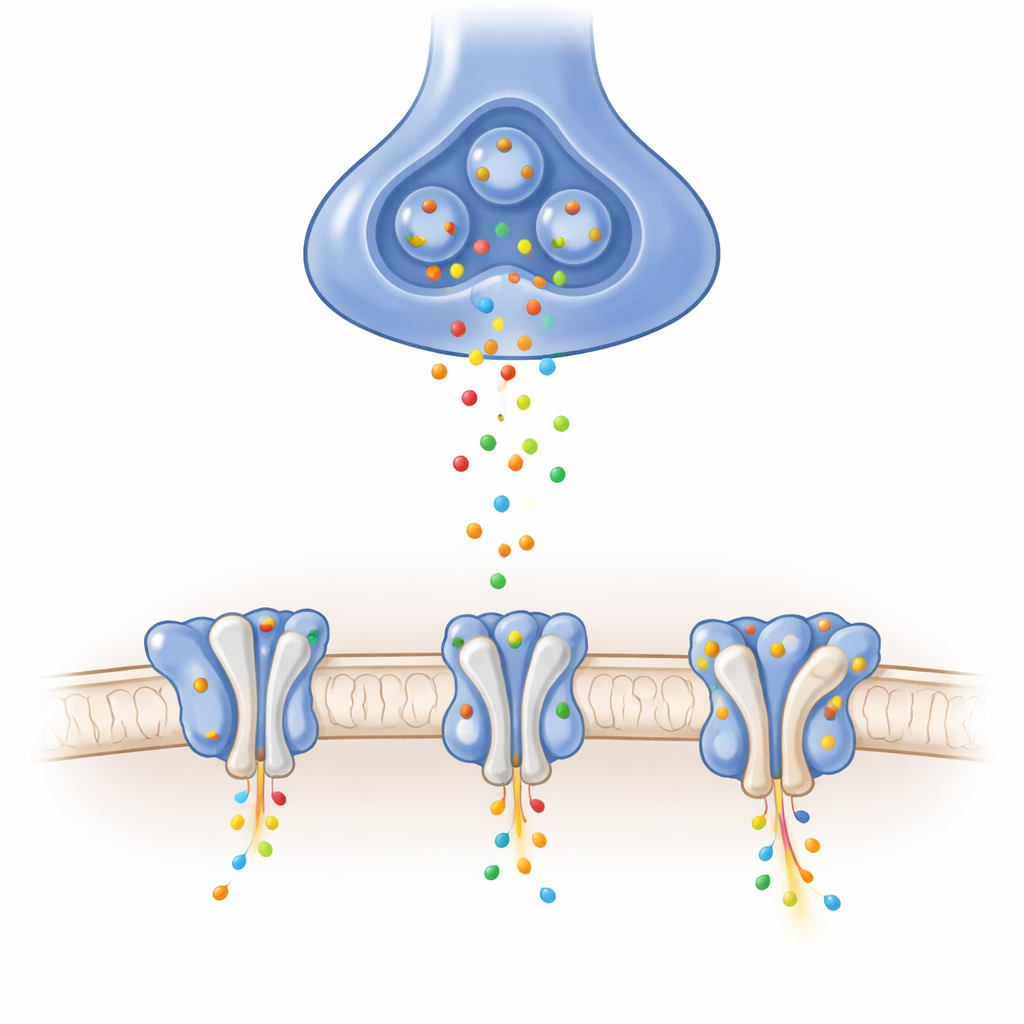
Во многих возбудительных сигналах мозга участвуют AMPA‑рецепторы, расположенные в принимающей мембране синапсов. Когда приходит химический мессенджер глутамат, эти рецепторы открывают пору, которая на доли миллисекунды пропускает положительно заряженные ионы в клетку, генерируя электрический сигнал. Точный состав каждого рецептора и набор вспомогательных белков, «прилипших» к нему, настраивают скорость открытия и закрытия, силу тока и восстановление после интенсивной работы. Одно особенно распространённое сочетание — гетеротетрамер GluA1/A2 — доминирует в ключевых центрах обучения, таких как гиппокамп, однако его подробная структура без помощников оставалась неясной.
Фиксация рецептора в трёх ключевых состояниях
С помощью высокоразрешающей крио‑электронной микроскопии авторы очистили рецепторы GluA1/A2 и запомнили их в трёх важных функциональных состояниях: закрытое, готовое к ответу; открытое, проводящее ионы; и десенситизированное — защитное, временно неответное состояние после продолжительной стимуляции. Электрические записи подтвердили, что слегка модифицированные рецепторы ведут себя похоже на природные. Снимки выявили Y‑образную архитектуру из четырёх субъединиц, организованных парами, и, что важно, отчётливо показали короткую петлю, часть фильтра селективности ионов, область, которая в ранних структурах часто была размыта. Эти базовые представления демонстрируют, как движение «раковин» связывающих лиганды доменов, вызванное глутаматом, натягивает соединительные элементы и откупоривает затвор канала в этом физиологически центральном рецепторе.
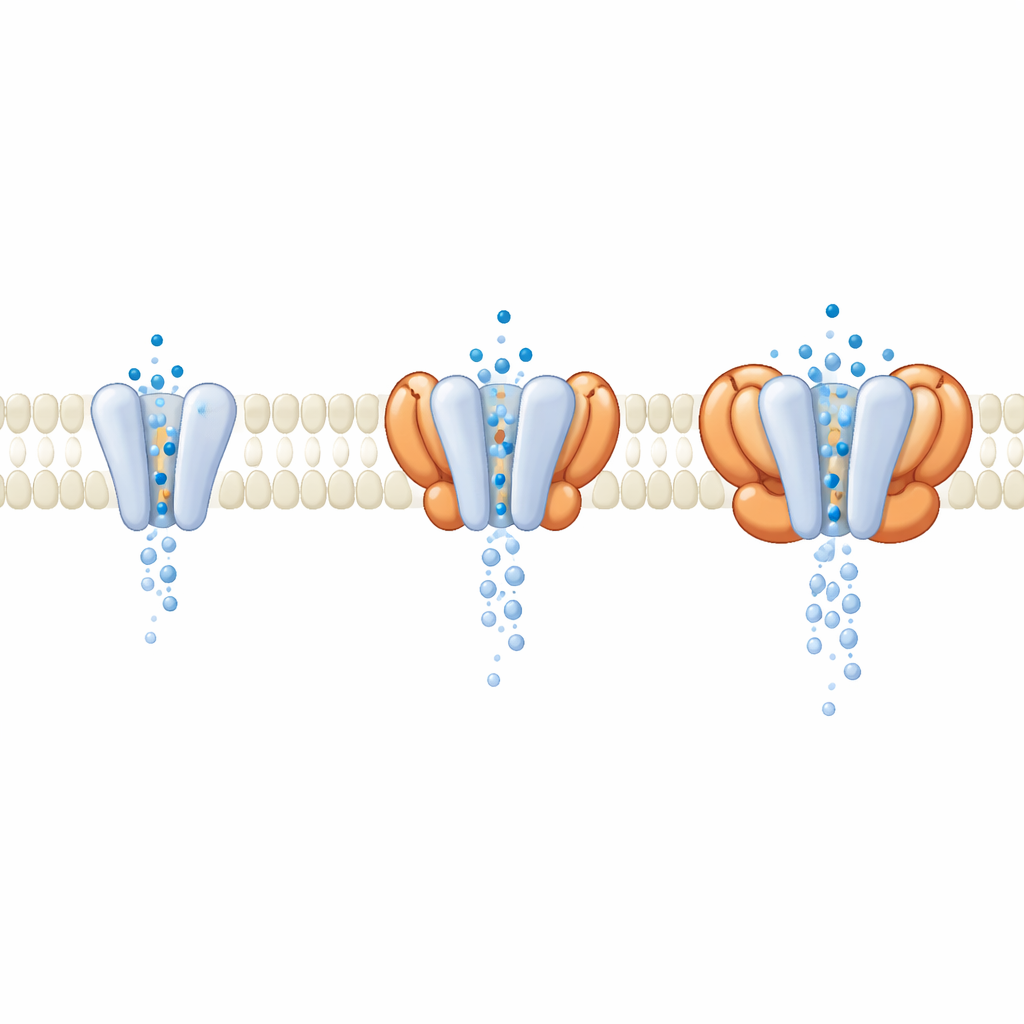
Вспомогательные белки расширяют затвор
В клетке GluA1/A2 редко работает в одиночку; обычно рядом с ним находятся вспомогательные белки, встроенные в мембрану. При обработке данных исследователи обнаружили подмножество рецепторов, естественно связанных с четырьмя единицами корнишон‑белка (CNIH), перенесёнными из клеток экспрессии. Сравнивая эти комплексы с «голым» ядром, они увидели, что внешние, детектирующие сигналы части выглядят почти одинаково в открытом состоянии. Ключевые различия проявлялись глубже в мембране, где CNIH и родственные семьи модификаторов меняли геометрию самой поры. Молекулярно‑динамические моделирования потока воды через канал показали, что комплексы с определёнными вспомогательными белками формируют более широкую, лучше гидратированную пору и повышённую смоделированную проводимость, хотя домены распознавания глутамата почти не изменялись. Это указывает на то, что многие модуляторы действуют не через изменение чувствительности к глутамату, а через перестройку затвора, по которому проходят ионы.
Асимметрия и искусство восстановления
Команда также изучила состояние десенситизации рецептора — он всё ещё связан с глутаматом, но больше не проводит ионы. В этом положении «раковины» перераспределяются так, что интерфейс, удерживающий их вместе в активном состоянии, трескается, в то время как их нижние части остаются достаточно близко, чтобы держать пору закрытой. Сравнив GluA1/A2 с рядом ранее решённых комплексов AMPA‑рецепторов с разными вспомогательными белками, авторы количественно оценили, насколько каждая пара «раковин» выкручивается из строгой двуосной симметрии. Они обнаружили сильную корреляцию: чем сильнее этот скручивание, тем медленнее рецептор восстанавливается после десенситизации и снова становится готовым откликнуться. Некоторые помощники удерживают димер почти симметричным, позволяя быстрому восстановлению, в то время как другие способствуют искажению и, следовательно, продлевают период неответности.
Последствия для настройки мозговых цепей и терапии
Вместе эти структурные и моделирующие данные показывают, что и состав основных субъединиц, и набор вспомогательных белков совместно определяют, как AMPA‑рецепторы регулируют электрические сигналы. Вспомогательные единицы могут расширять или сужать пору и контролировать длительность «молчания» рецепторов после интенсивной работы, не обязательно меняя способы распознавания глутамата. Поскольку нарушение функции AMPA‑рецепторов связано с эпилептическими припадками, последствиями инсульта и нейродегенерацией, детальные карты интерфейсов рецептор–помощник и подвижных частей затвора выделяют перспективные новые мишени для лекарств. Вместо широкого блокирования этих ключевых рецепторов будущие препараты могут тонко настраивать конкретные сборки, избирательно корректируя поток ионов и восстановление в тех цепях, которые в этом нуждаются.
Цитирование: Yen, L.Y., Newton, T.P., Yelshanskaya, M.V. et al. Auxiliary subunits reshape structural asymmetry and functional plasticity in heterotetrameric GluA1/A2 AMPA receptor core. Nat Commun 17, 4191 (2026). https://doi.org/10.1038/s41467-026-71063-1
Ключевые слова: AMPA-рецептор, синаптическая пластичность, вспомогательные субъединицы, криоэлектронная микроскопия, механизм открытия и закрытия ионного канала