Clear Sky Science · tr
Yardımcı alt birimler heterotetramerik GluA1/A2 AMPA reseptör çekirdeğinde yapısal asimetrileri ve fonksiyonel plastisiteyi yeniden şekillendiriyor
Beyin sinyali kapıları öğrenme ve hastalığı nasıl şekillendirir
Her düşünce, anı veya hareketiniz, sinir hücreleri arasında yüklü atomların akmasına izin veren küçük protein makinelerine dayanır. Bu çalışma, beynin en önemli makinelerinden biri olan GluA1/A2 AMPA reseptörüne odaklanıyor ve küçük yardımcı proteinlerin onun şeklini ve davranışını nasıl ince bir şekilde değiştirdiğini ortaya koyuyor. Bu değişiklikleri anlamak, epilepsi, inme ve Alzheimer hastalığı gibi durumlar için daha güvenli, daha hassas ilaçların geliştirilmesine kapı açabilir.
Beynin hızlı anahtarları
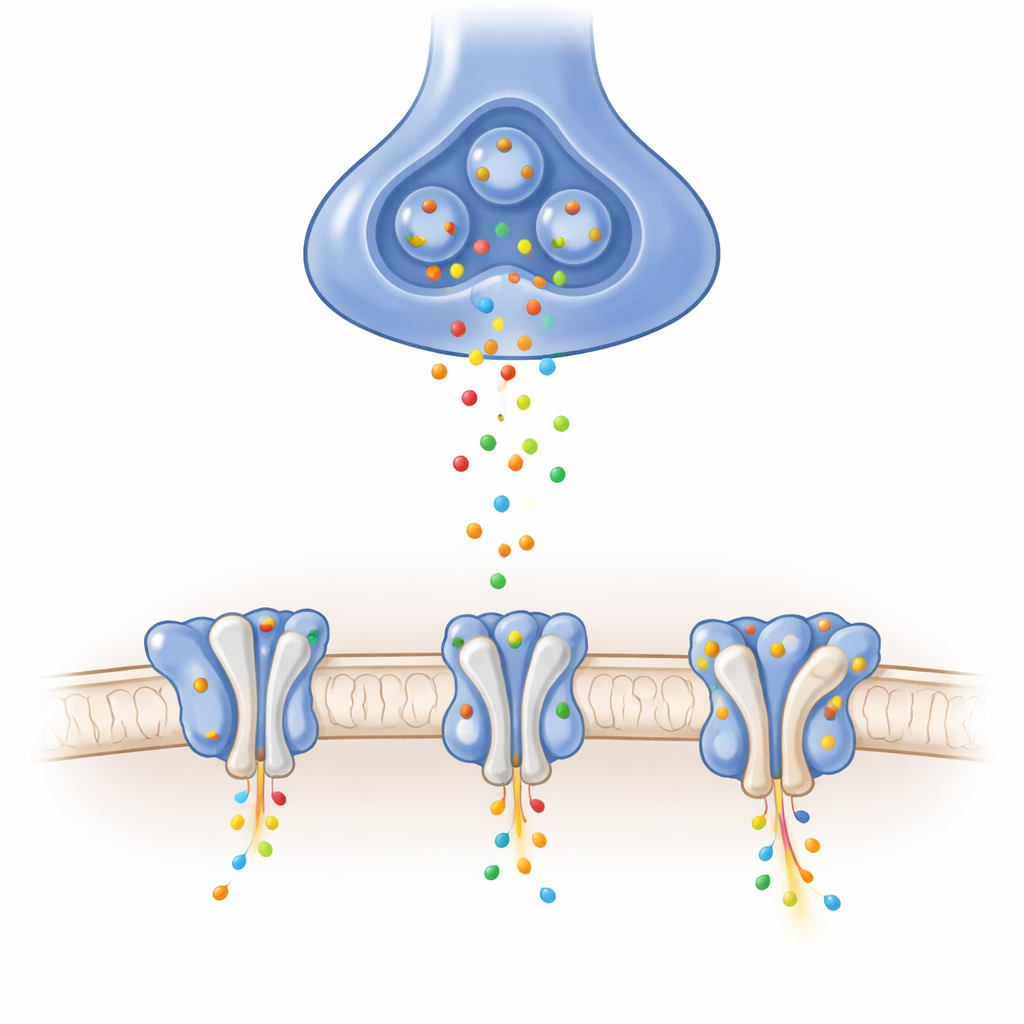
Beyinde birçok uyarıcı sinyal, sinapsların alıcı zarında bulunan AMPA reseptörleriyle iletilir. Kimyasal taşıyıcı glutamat geldiğinde, bu reseptörler kısa süreliğine pozitif yüklü iyonların hücre içine akmasına izin veren bir gözenek açar ve milisaniyeler içinde elektriksel sinyaller üretir. Her reseptörün tam bileşimi ve yanına takılan yardımcı proteinler, açılma ve kapanma hızını, geçen akımı ve yoğun kullanımdan sonra nasıl toparlandığını ayarlar. GluA1/A2 heterotetrameri olarak adlandırılan belirli bir kombinasyon, hipokampus gibi öğrenmenin kilit merkezlerinde baskın formdur, ancak yardımcılar bağlanmamış hâliyle ayrıntılı yapısı belirsiz kalmıştı.
Reseptörü üç temel pozda yakalamak
Yüksek çözünürlüklü kryo-elektron mikroskopisi kullanarak, araştırmacılar GluA1/A2 reseptörlerini saflaştırdı ve onları üç temel fonksiyonel pozda tuzağa düşürdü: kapalı ve yanıtlamaya hazır, açık ve iyon ileten, ile uzun süreli uyarımdan sonra geçici olarak iletmeyen koruyucu bir durum olan desensitize (duyarsızlaşmış). Biraz değiştirilmiş reseptörlerinin doğal olanlara çok benzediğini elektriksel kayıtlarla doğruladılar. Görüntüler, çiftler halinde düzenlenmiş dört alt birimden oluşan Y biçimli bir mimariyi ortaya koydu ve kritik olarak iyon seçicilik filtresinin bir parçasını oluşturan kısa halkayı net şekilde gösterdi; bu bölge önceki birçok yapıda bulanık kalmıştı. Bu temel görünümler, glutamatın bağlanmasıyla ligant-bağlayıcı “midyelerin” hareketlerinin bağlantı iplerini çekerek ve bu fizyolojik olarak merkezi reseptörde kanal kapısını nasıl açtığını gösteriyor.
Yardımcı proteinler kapıyı genişletiyor
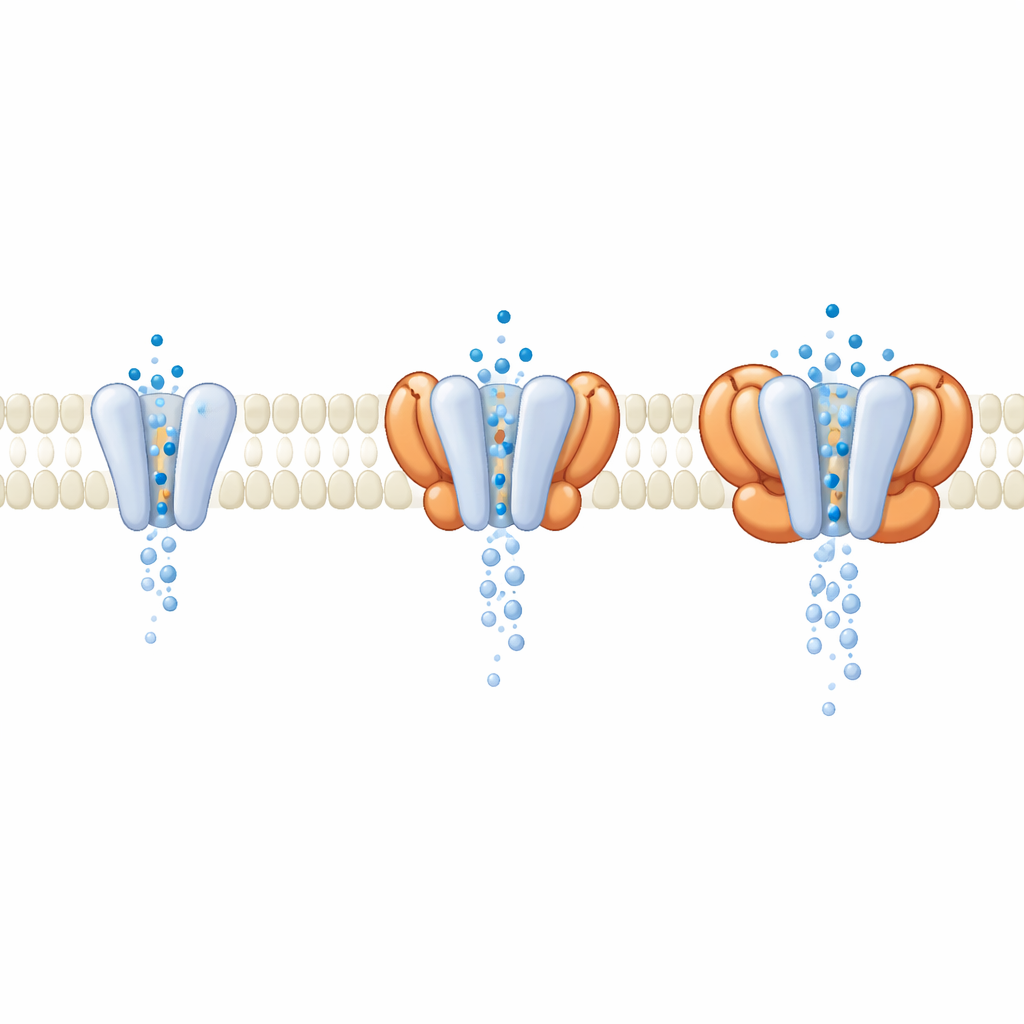
Hücrelerde GluA1/A2 nadiren tek başına hareket eder; genellikle zar boyunca yanında seyreden yardımcı proteinlerle birlikte bulunur. Veri işlem sırasında, araştırmacılar eksprese ettikleri hücrelerden taşınmış dört cornichon (CNIH) yardımcı birimi doğal olarak bağlı olan bir reseptör alt kümesi keşfettiler. Bu yardımcı yüklü reseptörleri çıplak çekirdekle karşılaştırdıklarında, kanal açıkken dıştaki, sinyal algılayan kısımların neredeyse aynı göründüğünü buldular. Anahtar farklar, CNIH ve ilişkili yardımcı ailelerin gözenek geometrisini değiştirdiği membranın daha derin bölgelerinde ortaya çıktı. Moleküler dinamik simülasyonlar, kanaldan su akışını modelleyerek, belirli yardımcıları içeren komplekslerin daha geniş, daha iyi hidrate olmuş bir gözenek ve daha yüksek simüle iletkenlik ürettiğini gösterdi; oysa glutamatı algılayan bölgeler neredeyse değişmemişti. Bu, birçok düzenleyicinin reseptörlerin glutamat algısını değiştirerek değil, iyonların geçtiği kapıyı yeniden şekillendirerek etkili olduğunu düşündürüyor.
Asimetri ve toparlanma sanatı
Araştırma ekibi ayrıca reseptör duyarsızlaştığında—hala glutamata bağlı ama artık iletken olmadığı durumda—ne olduğunu inceledi. Bu pozda, midyeler aktif durumda birbirini tutan ara yüzü çatlatacak şekilde yeniden düzenlenir, alt yarıları ise gözenek kapalı kalacak kadar yakın tutulur. Farklı yardımcı proteinler içeren daha önce çözümlenmiş çeşitli AMPA reseptör kompleksleriyle GluA1/A2’yi karşılaştırarak, yazarlar her bir midye çiftinin düzenli iki kat simetrisinden ne kadar sapma gösterdiğini nicelendirdiler. Güçlü bir korelasyon buldular: bu sapma ne kadar büyükse, reseptörün duyarsızlıktan toparlanıp tekrar yanıt vermeye hazır hâle gelmesi o kadar yavaş oluyordu. Bazı yardımcılar dimeri neredeyse simetrik tutarak hızlı toparlanmaya izin verirken, diğerleri bozulmayı teşvik ederek uzun süreli yanıtsızlığa yol açıyordu.
Beyin devrelerini ve tedavileri ayarlamak için çıkarımlar
Bu yapısal ve simülasyon sonuçları birlikte, hem çekirdek alt birimlerin kimliğinin hem de belirli yardımcı protein setinin AMPA reseptörlerinin elektrik sinyallerini nasıl kapattığını tanımlamak için birlikte çalıştığını gösteriyor. Yardımcı birimler gözenegi genişletebilir veya daraltabilir ve yoğun kullanımdan sonra reseptörlerin ne kadar süre sessiz kaldığını kontrol edebilir; bunun için glutamatın algılanma şeklini mutlaka değiştirmeleri gerekmez. AMPA reseptörünün işlev bozukluğunun nöbet bozuklukları, inme hasarı ve nörodejenerasyonla ilişkili olması nedeniyle, reseptör–yardımcı ara yüzlerinin ve kapının hareketli parçalarının ayrıntılı haritaları umut verici yeni ilaç hedeflerini öne çıkarıyor. Bu hayati reseptörleri geniş ölçüde bloke etmek yerine, gelecekteki ilaçlar belirli montajları ince ayarlayarak iyon akışını ve toparlanmayı tam olarak ihtiyaç duyulan devrelerde hassas şekilde ayarlayabilir.
Atıf: Yen, L.Y., Newton, T.P., Yelshanskaya, M.V. et al. Auxiliary subunits reshape structural asymmetry and functional plasticity in heterotetrameric GluA1/A2 AMPA receptor core. Nat Commun 17, 4191 (2026). https://doi.org/10.1038/s41467-026-71063-1
Anahtar kelimeler: AMPA reseptörü, sinaptik plastisite, yardımcı alt birimler, kryo elektron mikroskobu, iyon kanalı kapanışı