Clear Sky Science · it
Le subunità ausiliarie rimodellano l’asimmetria strutturale e la plasticità funzionale nel core eterotetramerico del recettore AMPA GluA1/A2
Come gli interruttori dei segnali cerebrali modellano apprendimento e malattia
Ogni pensiero, ricordo o movimento dipende da piccole macchine proteiche che permettono agli atomi caricati di fluire tra le cellule nervose. Questo studio esamina uno dei più importanti di questi dispositivi cerebrali — il recettore AMPA GluA1/A2 — e mostra come piccole proteine ausiliarie ne modifichino sottilmente forma e comportamento. Capire questi cambiamenti potrebbe aprire la strada a farmaci più sicuri e mirati per condizioni come epilessia, ictus e malattia di Alzheimer.
Gli interruttori rapidi del cervello
Nel cervello, molti segnali eccitatori sono mediati dai recettori AMPA, situati nella membrana ricevente delle sinapsi. Quando arriva il messaggero chimico glutammato, questi recettori aprono un poro che permette brevemente agli ioni positivi di entrare nella cellula, generando segnali elettrici in pochi millisecondi. La composizione esatta di ciascun recettore, e quali proteine ausiliarie si associano ai suoi lati, regola la velocità di apertura e chiusura, l’intensità della corrente e il recupero dopo un uso intenso. Una combinazione particolare, chiamata eterotetràmero GluA1/A2, è la forma dominante in centri chiave per l’apprendimento come l’ippocampo, ma la sua struttura dettagliata senza ausiliari rimaneva difficile da definire.
Catturare il recettore in tre pose chiave
Usando la crio‑microscopia elettronica ad alta risoluzione, gli autori hanno purificato i recettori GluA1/A2 e li hanno intrappolati in tre pose funzionali essenziali: chiuso e pronto a rispondere, aperto e conduttivo, e desensibilizzato — uno stato protettivo temporaneamente non responsivo dopo una stimolazione prolungata. Hanno verificato con registrazioni elettriche che i recettori leggermente ingegnerizzati si comportavano in modo molto simile a quelli naturali. Le immagini hanno rivelato un’architettura a Y composta da quattro subunità disposte a coppie e, cosa cruciale, hanno chiaramente risolto il breve anello che fa parte del filtro di selettività ionica, una regione spesso sfocata in strutture precedenti. Queste viste di base mostrano come i movimenti indotti dal glutammato nelle “valvole” del sito di legame tirino i collegamenti e aprano il cancello del canale in questo recettore centrale dal punto di vista fisiologico.
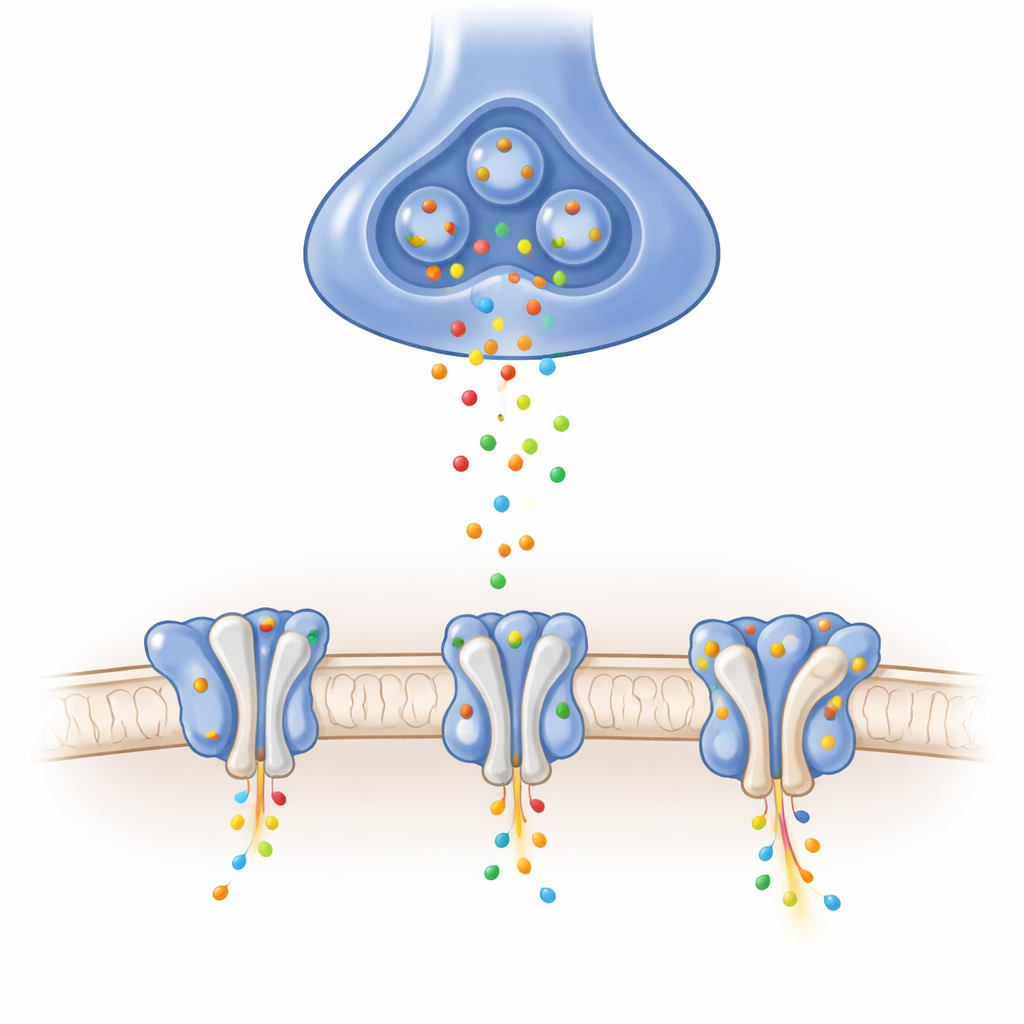
Le proteine ausiliarie allargano il cancello
In cellula, GluA1/A2 raramente agisce da solo; è di solito accompagnato da proteine ausiliarie che si affiancano nella membrana. Durante l’elaborazione dei dati, i ricercatori hanno scoperto un sottoinsieme di recettori legati naturalmente a quattro unità cornichon (CNIH) rimaste dall’espressione nelle cellule. Confrontando questi recettori con ausiliari con il core nudo, hanno osservato che le parti esterne, deputate al rilevamento del segnale, risultavano quasi identiche quando il canale era aperto. Le differenze chiave emergevano più in profondità nella membrana, dove CNIH e famiglie di ausiliari correlate alteravano la geometria del poro stesso. Le simulazioni di dinamica molecolare del flusso d’acqua attraverso il canale hanno mostrato che i complessi contenenti certi ausiliari generavano un poro più ampio, meglio idratato e con una conduttanza simulata maggiore, pur mantenendo quasi invariati i domini sensibili al glutammato. Ciò suggerisce che molti modulatori agiscono non cambiando il modo in cui i recettori percepiscono il glutammato, ma rimodellando il cancello attraverso cui passano gli ioni.
Asimmetria e l’arte del recupero
Il gruppo ha anche studiato cosa accade quando il recettore diventa desensibilizzato — ancora legato al glutammato ma non più conduttivo. In questa posa, le valvole si riallineano in modo che l’interfaccia che le teneva unite nello stato attivo si apra, mentre le loro metà inferiori restano abbastanza vicine da mantenere il poro chiuso. Confrontando GluA1/A2 con una varietà di complessi di recettori AMPA precedentemente risolti contenenti diversi ausiliari, gli autori hanno quantificato quanto ciascuna coppia di valvole ruoti fuori da una netta simmetria binaria. Hanno trovato una forte correlazione: maggiore è questa torsione, più lento è il recupero del recettore dalla desensibilizzazione e più tempo impiega a ritornare reattivo. Alcuni ausiliari mantengono il dimero quasi simmetrico, permettendo un recupero rapido, mentre altri favoriscono la distorsione e quindi una prolungata inattivazione.
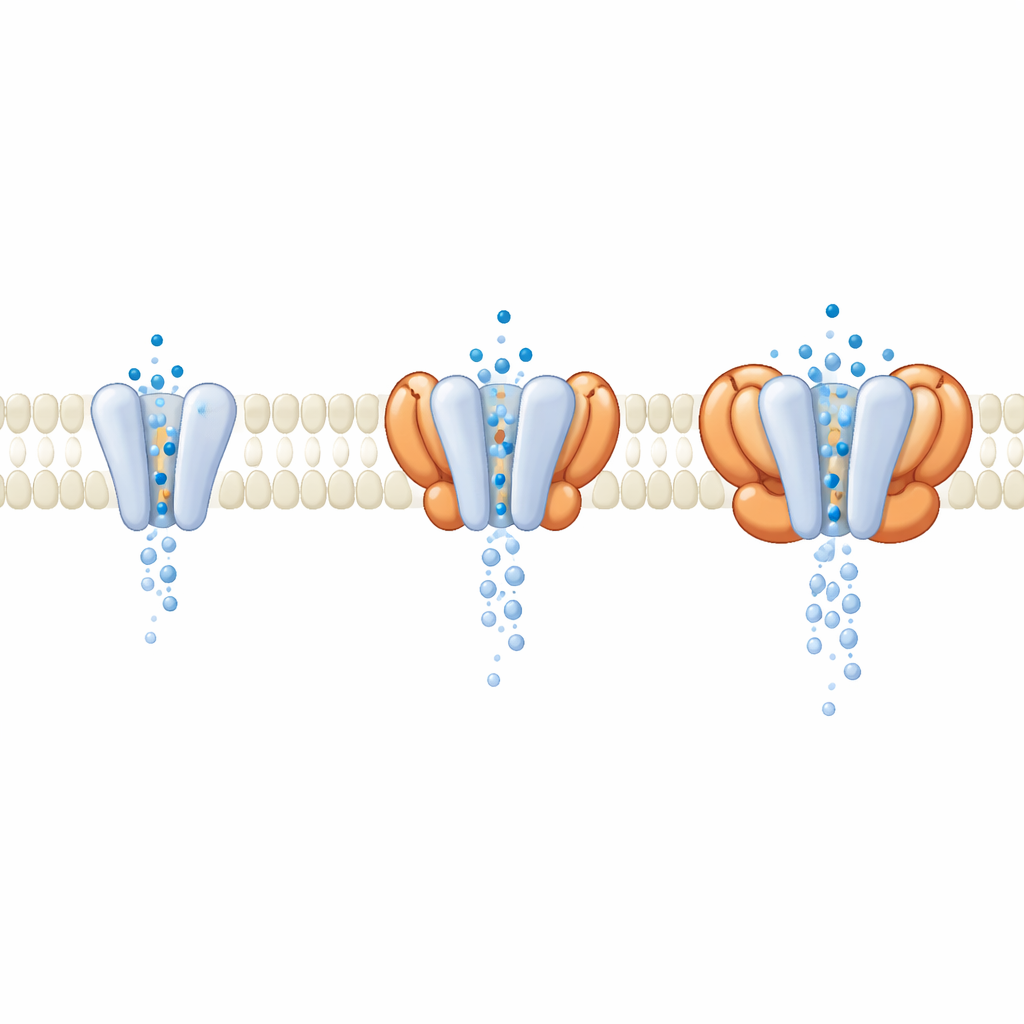
Implicazioni per la messa a punto dei circuiti cerebrali e le terapie
Nel loro insieme, questi risultati strutturali e di simulazione mostrano che sia l’identità delle subunità core sia l’insieme specifico di proteine ausiliarie definiscono come i recettori AMPA modulano i segnali elettrici. Le unità ausiliarie possono allargare o restringere il poro e controllare quanto a lungo i recettori restano silenti dopo un uso intenso, senza necessariamente alterare il modo in cui il glutammato viene percepito. Poiché il malfunzionamento dei recettori AMPA è collegato a disturbi convulsivi, danni da ictus e neurodegenerazione, le mappe dettagliate delle interfacce recettore‑ausiliare e delle parti mobili del cancello indicano nuovi bersagli farmacologici promettenti. Piuttosto che bloccare in modo esteso questi recettori cruciali, i futuri farmaci potrebbero modulare finemente specifiche assemblie, regolando con delicatezza il flusso ionico e il recupero nei circuiti che ne hanno bisogno.
Citazione: Yen, L.Y., Newton, T.P., Yelshanskaya, M.V. et al. Auxiliary subunits reshape structural asymmetry and functional plasticity in heterotetrameric GluA1/A2 AMPA receptor core. Nat Commun 17, 4191 (2026). https://doi.org/10.1038/s41467-026-71063-1
Parole chiave: recettore AMPA, plasticità sinaptica, subunità ausiliarie, crio‑microscopia elettronica, apertura del canale ionico