Clear Sky Science · fr
Les sous-unités auxiliaires reconfigurent l’asymétrie structurelle et la plasticité fonctionnelle du cœur hétérotétramérique du récepteur AMPA GluA1/A2
Comment les portes des signaux cérébraux façonnent l’apprentissage et la maladie
Chaque pensée, souvenir ou mouvement dépend de minuscules machines protéiques qui laissent passer des ions chargés entre les neurones. Cette étude se concentre sur l’une des plus importantes de ces machines — le récepteur AMPA GluA1/A2 — et montre comment de petites protéines auxiliaires modifient subtilement sa forme et son comportement. Comprendre ces modifications pourrait ouvrir la voie à des médicaments plus sûrs et plus ciblés pour des affections comme l’épilepsie, l’accident vasculaire cérébral et la maladie d’Alzheimer.
Les commutateurs rapides du cerveau
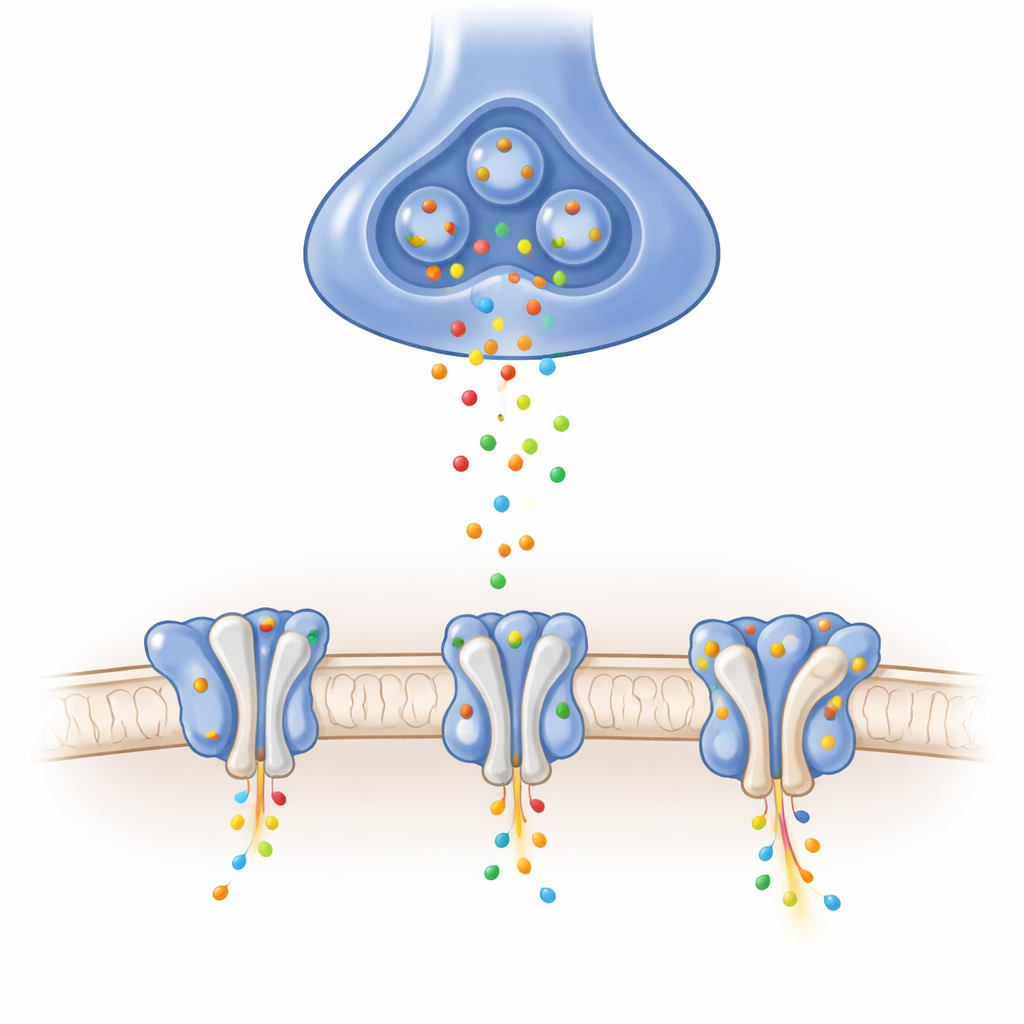
Dans le cerveau, de nombreux signaux excitateurs sont transmis par les récepteurs AMPA, situés dans la membrane postsynaptique. Lorsque le messager chimique glutamate arrive, ces récepteurs ouvrent un pore qui laisse brièvement entrer des ions positifs dans la cellule, produisant des signaux électriques en quelques millisecondes. La composition précise de chaque récepteur, et les protéines auxiliaires qui s’y associent, ajustent la vitesse d’ouverture et de fermeture, l’intensité du courant et la récupération après usage intense. Une combinaison particulière, appelée hétérotétramère GluA1/A2, est la forme dominante dans des centres d’apprentissage clés comme l’hippocampe, mais sa structure détaillée sans auxiliaires était jusque-là restée difficile à cerner.
Capturer le récepteur en trois positions clés
À l’aide d’une cryo‑microscopie électronique à haute résolution, les auteurs ont purifié les récepteurs GluA1/A2 et les ont piégés dans trois états fonctionnels essentiels : fermé et prêt à répondre, ouvert et conduisant les ions, et désensibilisé — un état protecteur temporairement non réactif après stimulation prolongée. Ils ont confirmé par des enregistrements électriques que leurs récepteurs légèrement modifiés se comportaient de manière très proche des récepteurs naturels. Les images ont révélé une architecture en Y composée de quatre sous‑unités organisées en paires et, surtout, ont clairement résolu la courte boucle qui fait partie du filtre de sélectivité ionique, une région souvent floue dans des structures antérieures. Ces vues de base montrent comment les mouvements induits par le glutamate des « coquilles » de liaison au ligand tirent sur des liaisons et ouvrent la porte du canal dans ce récepteur central sur le plan physiologique.
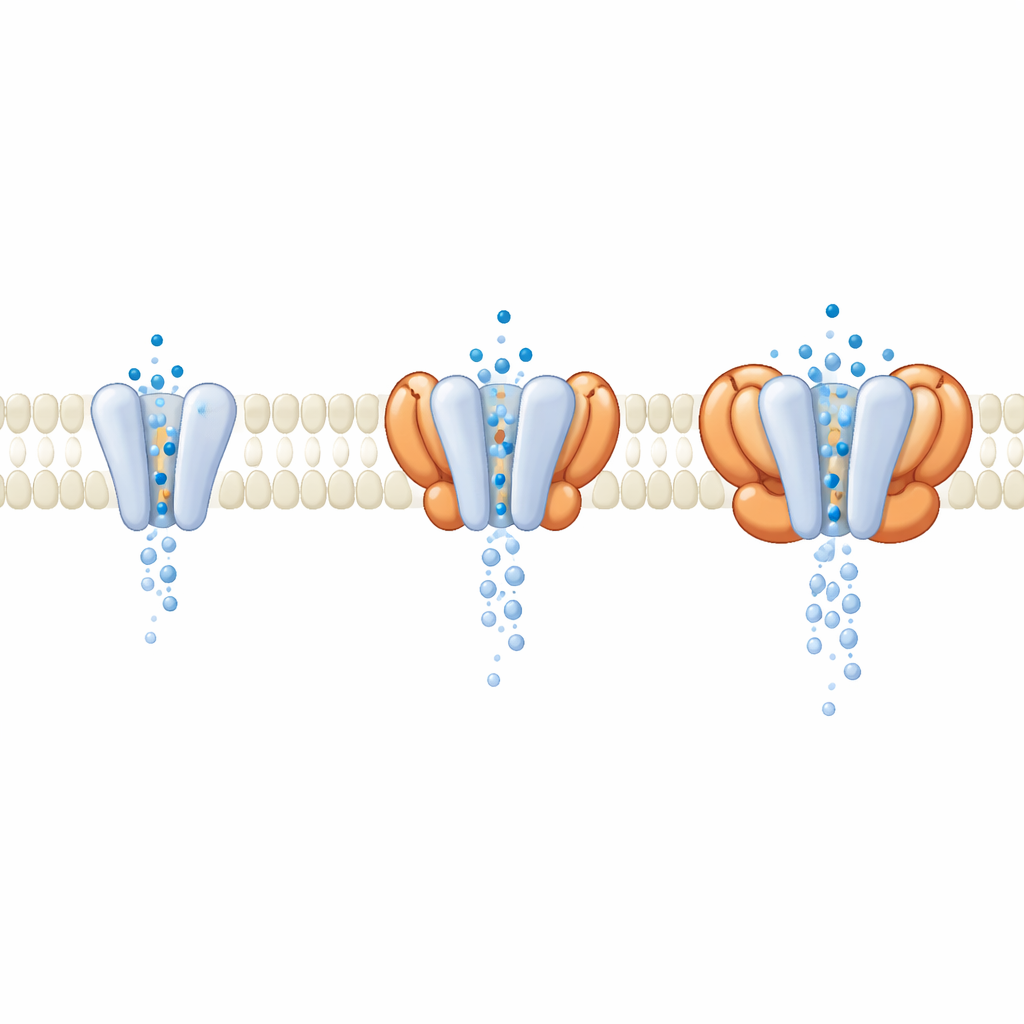
Les protéines auxiliaires élargissent la porte
Dans les cellules, GluA1/A2 agit rarement seul ; il est généralement accompagné de protéines auxiliaires qui résident dans la membrane à ses côtés. Pendant le traitement des données, les chercheurs ont découvert une sous‑population de récepteurs naturellement liés à quatre unités cornichon (CNIH) provenant des cellules d’expression. En comparant ces récepteurs chargés d’auxiliaires au cœur dépouillé, ils ont constaté que les parties externes détectrices de signal étaient presque identiques lorsque le canal était ouvert. Les différences clés apparaissaient plus profondément dans la membrane, où les CNIH et des familles d’auxiliaires apparentées modifiaient la géométrie du pore lui‑même. Des simulations de dynamique moléculaire du flux d’eau à travers le canal ont montré que les complexes contenant certains auxiliaires produisaient un pore plus large, mieux hydraté et une conductance simulée plus élevée, même si les domaines sensibles au glutamate changeaient à peine. Cela suggère que de nombreux modulateurs agissent non pas en altérant la détection du glutamate par les récepteurs, mais en reshapant la porte par laquelle passent les ions.
Asymétrie et l’art de la récupération
L’équipe a également examiné ce qui se passe lorsque le récepteur devient désensibilisé — toujours lié au glutamate mais ne conduisant plus. Dans cet état, les coquilles se réarrangent de sorte que l’interface qui les maintient ensemble à l’état actif se fissure, tandis que leurs moitiés inférieures restent suffisamment proches pour garder le pore fermé. En comparant GluA1/A2 avec une variété de complexes de récepteurs AMPA résolus précédemment contenant différents auxiliaires, les auteurs ont quantifié le degré de torsion de chaque paire de coquilles par rapport à une symétrie bilatérale parfaite. Ils ont trouvé une corrélation forte : plus cette torsion est importante, plus la récupération du récepteur après désensibilisation est lente et plus il met du temps à redevenir réactif. Certains auxiliaires maintiennent le dimère presque symétrique, permettant une récupération rapide, tandis que d’autres favorisent la déformation et donc une non‑réactivité prolongée.
Conclusions pour le réglage des circuits cérébraux et les thérapies
Ensemble, ces résultats structuraux et de simulation montrent que l’identité des sous‑unités centrales et l’ensemble particulier de protéines auxiliaires déterminent conjointement la façon dont les récepteurs AMPA régulent les signaux électriques. Les unités auxiliaires peuvent élargir ou rétrécir le pore et contrôler la durée pendant laquelle les récepteurs restent silencieux après un usage intense, sans nécessairement modifier la détection du glutamate. Étant donné que le dysfonctionnement des récepteurs AMPA est lié aux troubles convulsifs, aux lésions liées aux AVC et à la neurodégénérescence, les cartes détaillées des interfaces récepteur‑auxiliaire et des pièces mobiles de la porte mettent en évidence de nouvelles cibles médicamenteuses prometteuses. Plutôt que de bloquer largement ces récepteurs cruciaux, de futurs médicaments pourraient affiner des assemblages spécifiques, ajustant subtilement le flux ionique et la récupération dans les circuits qui en ont besoin.
Citation: Yen, L.Y., Newton, T.P., Yelshanskaya, M.V. et al. Auxiliary subunits reshape structural asymmetry and functional plasticity in heterotetrameric GluA1/A2 AMPA receptor core. Nat Commun 17, 4191 (2026). https://doi.org/10.1038/s41467-026-71063-1
Mots-clés: récepteur AMPA, plasticité synaptique, sous-unités auxiliaires, cryo‑microscopie électronique, ouverture de canal ionique