Clear Sky Science · es
Subunidades auxiliares remodelan la asimetría estructural y la plasticidad funcional en el núcleo heterotetramérico del receptor AMPA GluA1/A2
Cómo las compuertas de la señal cerebral moldean el aprendizaje y la enfermedad
Cada pensamiento, recuerdo o movimiento depende de diminutas máquinas proteicas que permiten el flujo de átomos cargados entre las células nerviosas. Este estudio se centra en una de las máquinas más importantes del cerebro—el receptor AMPA GluA1/A2—y revela cómo pequeñas proteínas auxiliares cambian sutilmente su forma y comportamiento. Entender estos cambios puede abrir puertas a fármacos más seguros y precisos para afecciones como epilepsia, ictus y la enfermedad de Alzheimer.
Los interruptores rápidos del cerebro
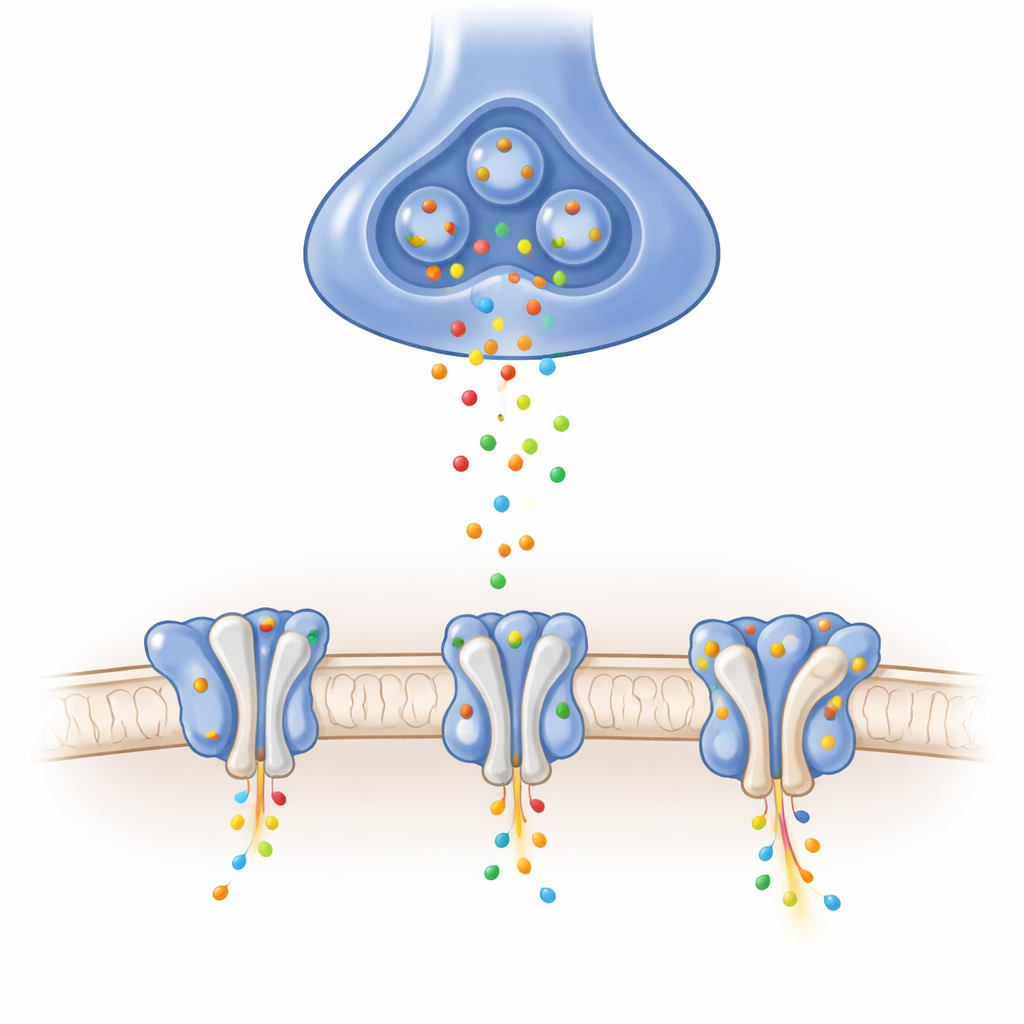
En el cerebro, muchas señales excitadoras se transmiten mediante receptores AMPA, que se sitúan en la membrana receptora de las sinapsis. Cuando llega el mensajero químico glutamato, estos receptores abren un poro que permite brevemente la entrada de iones con carga positiva en la célula, generando señales eléctricas en cuestión de milisegundos. La composición exacta de cada receptor y las proteínas auxiliares que se asocian a sus lados afinan la velocidad de apertura y cierre, la intensidad de la corriente y la recuperación tras un uso intenso. Una combinación particular, denominada heterotetrámero GluA1/A2, es la forma dominante en centros de aprendizaje clave como el hipocampo, aunque su estructura detallada sin auxiliares había permanecido esquiva.
Capturar el receptor en tres posturas clave
Empleando microscopía crioelectrónica de alta resolución, los autores purificaron receptores GluA1/A2 y los aprisionaron en tres posturas funcionales esenciales: cerrado y listo para responder, abierto y conduciendo iones, y desensibilizado—un estado protector temporalmente no receptivo tras una estimulación prolongada. Verificaron con registros eléctricos que sus receptores ligeramente modificados se comportaban de forma muy parecida a los naturales. Las imágenes revelaron una arquitectura en forma de Y construida por cuatro subunidades dispuestas en pares y, de forma crucial, resolvieron claramente el bucle corto que forma parte del filtro de selectividad iónica, una región que había aparecido borrosa en muchas estructuras anteriores. Estas vistas de referencia muestran cómo los movimientos inducidos por el glutamato en las "conchas" de unión al ligando tiran de los enlazadores y abren la compuerta del canal en este receptor central fisiológicamente.
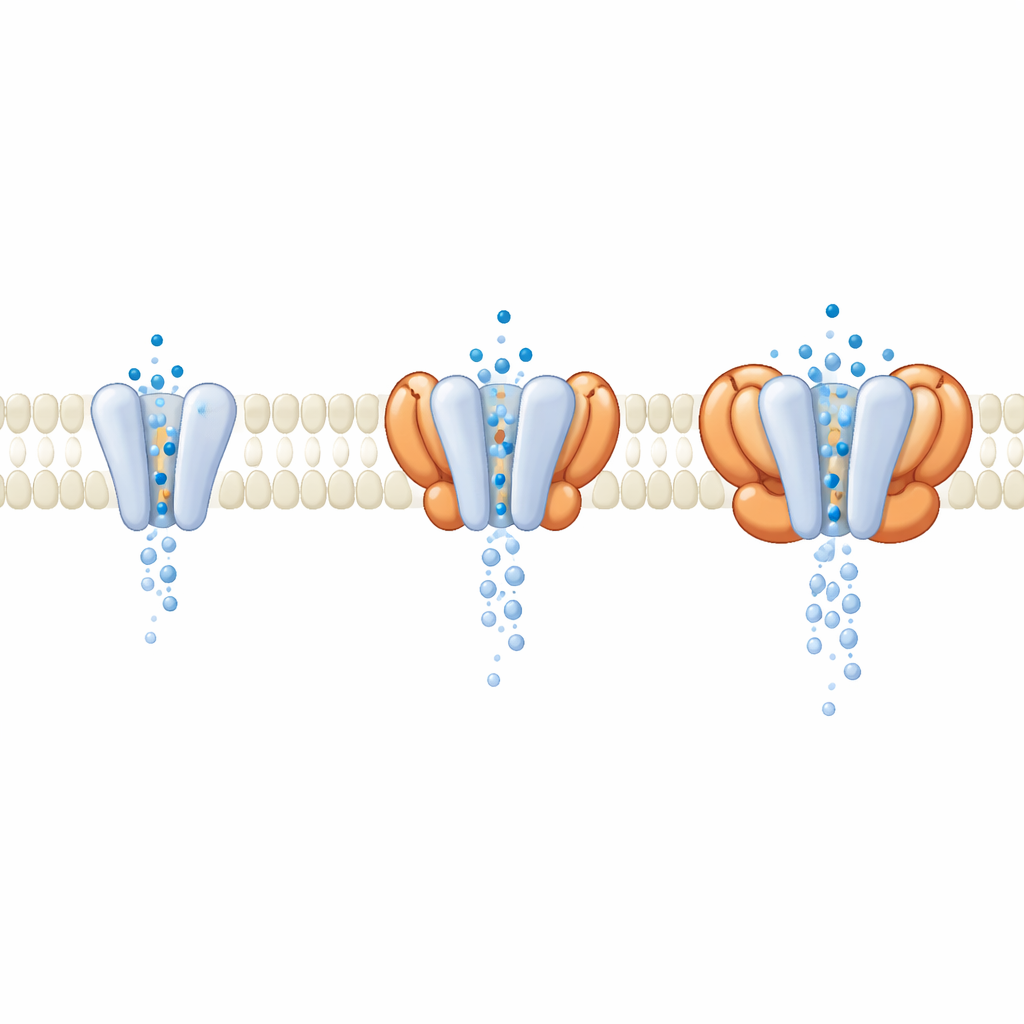
Las proteínas auxiliares ensanchan la compuerta
En las células, el GluA1/A2 rara vez actúa solo; suele ir acompañado de proteínas auxiliares que se alojan en la membrana a su lado. Durante el procesamiento de datos, los investigadores detectaron un subconjunto de receptores naturalmente unidos a cuatro unidades cornichon (CNIH) procedentes de las células de expresión. Comparando estos receptores con auxiliares con el núcleo desnudo, comprobaron que las partes externas, dedicadas a detectar señales, se veían casi idénticas cuando el canal estaba abierto. Las diferencias clave surgían más profundo en la membrana, donde CNIH y familias auxiliares relacionadas alteraban la geometría del propio poro. Simulaciones de dinámica molecular del flujo de agua a través del canal mostraron que los complejos que contenían ciertos auxiliares producían un poro más ancho, mejor hidratado y con mayor conductancia simulada, aunque los dominios detectores de glutamato apenas cambiaban. Esto sugiere que muchos moduladores actúan no cambiando cómo el receptor detecta el glutamato, sino remodelando la compuerta por la que pasan los iones.
Asimetría y el arte de la recuperación
El equipo también examinó qué ocurre cuando el receptor se desensibiliza—sigue unido al glutamato pero ya no conduce. En esta postura, las conchas se reordenan de modo que la interfaz que las mantiene juntas en el estado activo se abre, mientras que sus mitades inferiores permanecen lo bastante cercanas como para mantener el poro cerrado. Al comparar GluA1/A2 con una variedad de complejos de receptores AMPA resueltos previamente que contienen distintas proteínas auxiliares, los autores cuantificaron cuánto gira cada par de conchas fuera de una simetría axial de dos pliegues. Encontraron una correlación fuerte: cuanto mayor es este giro, más lenta es la recuperación del receptor tras la desensibilización y más tiempo tarda en volver a estar listo para responder. Algunos auxiliares mantienen al dímero casi simétrico, permitiendo una recuperación rápida, mientras que otros fomentan la distorsión y, por tanto, una inactividad prolongada.
Implicaciones para afinar circuitos cerebrales y terapias
En conjunto, estos resultados estructurales y de simulación muestran que tanto la identidad de las subunidades del núcleo como el conjunto particular de proteínas auxiliares definen cómo los receptores AMPA regulan las señales eléctricas. Las unidades auxiliares pueden ensanchar o estrechar el poro y controlar cuánto tiempo los receptores permanecen silentes tras un uso intenso, sin necesariamente alterar cómo se percibe el glutamato. Dado que el malfuncionamiento de los receptores AMPA se asocia con trastornos convulsivos, daños por ictus y neurodegeneración, los mapas detallados de las interfaces receptor‑auxiliar y de las partes móviles de la compuerta resaltan nuevas dianas farmacológicas prometedoras. En lugar de bloquear de forma general estos receptores cruciales, los futuros medicamentos podrían afinar ensamblajes específicos, ajustando sutilmente el flujo de iones y la recuperación en los circuitos que realmente lo necesitan.
Cita: Yen, L.Y., Newton, T.P., Yelshanskaya, M.V. et al. Auxiliary subunits reshape structural asymmetry and functional plasticity in heterotetrameric GluA1/A2 AMPA receptor core. Nat Commun 17, 4191 (2026). https://doi.org/10.1038/s41467-026-71063-1
Palabras clave: receptor AMPA, plasticidad sináptica, subunidades auxiliares, crioelectrónica de transmisión, apertura de canales iónicos