Clear Sky Science · sv
Hjälpande underenheter omformar strukturell asymmetri och funktionell plasticitet i heterotetramert GluA1/A2 AMPA-receptorstomme
Hur hjärnans signalgrindar formar inlärning och sjukdom
Varje tanke, minne eller rörelse du utför bygger på mikroskopiska proteinkomplex som låter laddade atomer flöda mellan nervceller. Den här studien zoomar in på en av hjärnans viktigaste sådana maskiner—GluA1/A2 AMPA-receptorn—och visar hur små hjälpproteiner subtilt ändrar dess form och beteende. Att förstå dessa förändringar kan öppna dörrar för säkrare och mer precisa läkemedel för tillstånd som epilepsi, stroke och Alzheimers sjukdom.
Hjärnans snabba brytare
I hjärnan förmedlas många excitatoriska signaler via AMPA-receptorer, som sitter i synapsens mottagande membran. När signalsubstansen glutamat anländer öppnar dessa receptorer en por som kortvarigt tillåter positiva joner att rusa in i cellen och skapa elektriska signaler på bara millisekunder. Den exakta sammansättningen av varje receptor, och vilka hjälpproteiner som håller sig vid dess sidor, ställer in hur snabbt den öppnar och stänger, hur stor ström som passerar och hur den återhämtar sig efter intensiv användning. En särskild kombination, kallad GluA1/A2-heterotetramer, är den dominerande formen i viktiga inlärningscentra som hippocampus, men dess detaljerade struktur utan hjälpande enheter hade hittills varit svårfångad.
Fånga receptorn i tre nyckelpositioner
Med högupplösande kryoelektronmikroskopi renade författarna GluA1/A2-receptorer och fångade dem i tre väsentliga funktionella tillstånd: stängd och redo att reagera, öppen och ledande joner, samt desensibiliserad—ett skyddande, tillfälligt oresponsivt tillstånd efter långvarig stimulans. De verifierade med elektriska inspelningar att deras lätt modifierade receptorer betedde sig mycket likt naturliga varianter. Bilderna avslöjade en Y-formad arkitektur byggd av fyra subenheter arrangerade i par, och, viktigt, visade tydligt den korta loopen som utgör en del av jonselektivitetsfiltret—en region som tidigare ofta varit suddig i många strukturer. Dessa grundläggande vyer visar hur glutamatinducerade rörelser i ligandbindande ”skalbössor” drar i länkarna och pryder upp kanalens grind i denna fysiologiskt centrala receptor.
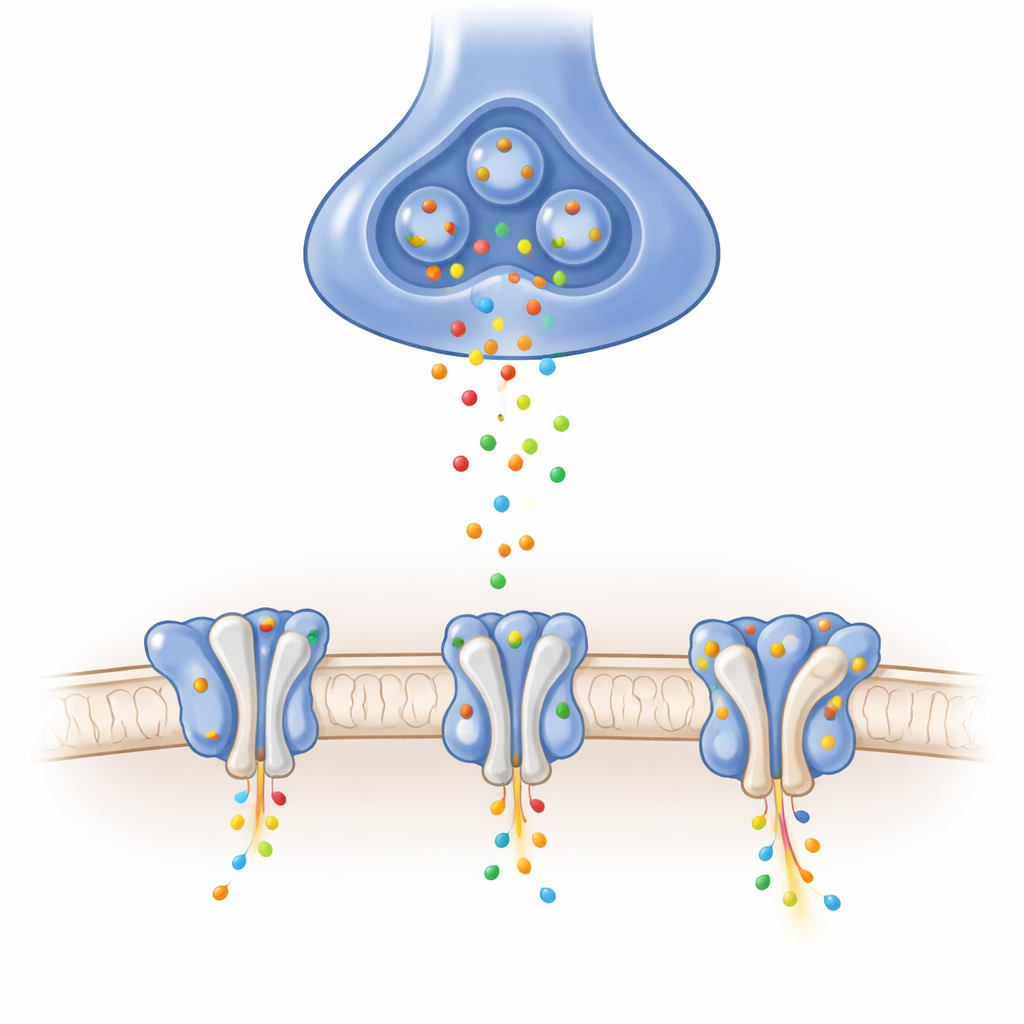
Hjälpproteiner vidgar grinden
I celler agerar GluA1/A2 sällan ensam; den följs vanligen av hjälpande proteiner som sitter i membranet vid dess sida. Under databehandlingen upptäckte forskarna en population av receptorer som naturligt var bundna till fyra cornichon (CNIH)-hjälparenheter som följt med från uttryckscellerna. När de jämförde dessa hjälpproteinladdade komplex med den nakna stommen fann de att de yttre, signalsensoriska delarna såg nästan identiska ut när kanalen var öppen. De avgörande skillnaderna framträdde djupare i membranet, där CNIH och släktingar i hjälparfamiljerna förändrade porens geometri. Molekylära dynamiksimuleringar av vattenflöde genom kanalen visade att komplex innehållande vissa hjälpare gav en bredare, bättre hydratiserad por och högre simulerad konduktans, även om glutamatsensorerna knappt förändrades. Detta tyder på att många modulatorer verkar inte genom att ändra hur receptorer känner av glutamat, utan genom att omforma den grind genom vilken joner passerar.
Asymmetri och konsten att återhämta sig
Gruppen undersökte också vad som händer när receptorn blir desensibiliserad—fortfarande bunden till glutamat men inte längre ledande. I detta tillstånd omarrangerar skalbössorna sig så att gränsytan som håller dem samman i det aktiva tillståndet spricker upp, medan deras nedre delar förblir tillräckligt nära för att hålla poren stängd. Genom att jämföra GluA1/A2 med en mängd tidigare lösta AMPA-receptorkomplex som innehöll olika hjälpande proteiner kvantifierade författarna hur mycket varje par av skalbössor vrider sig ur en prydlig tvåfaldig symmetri. De fann en stark korrelation: ju större denna vridning, desto långsammare återhämtar sig receptorn från desensibilisering och blir redo att reagera igen. Vissa hjälpare håller dimeren nära symmetrisk, vilket möjliggör snabb återhämtning, medan andra främjar distortion och därmed förlängd oresponsivitet.
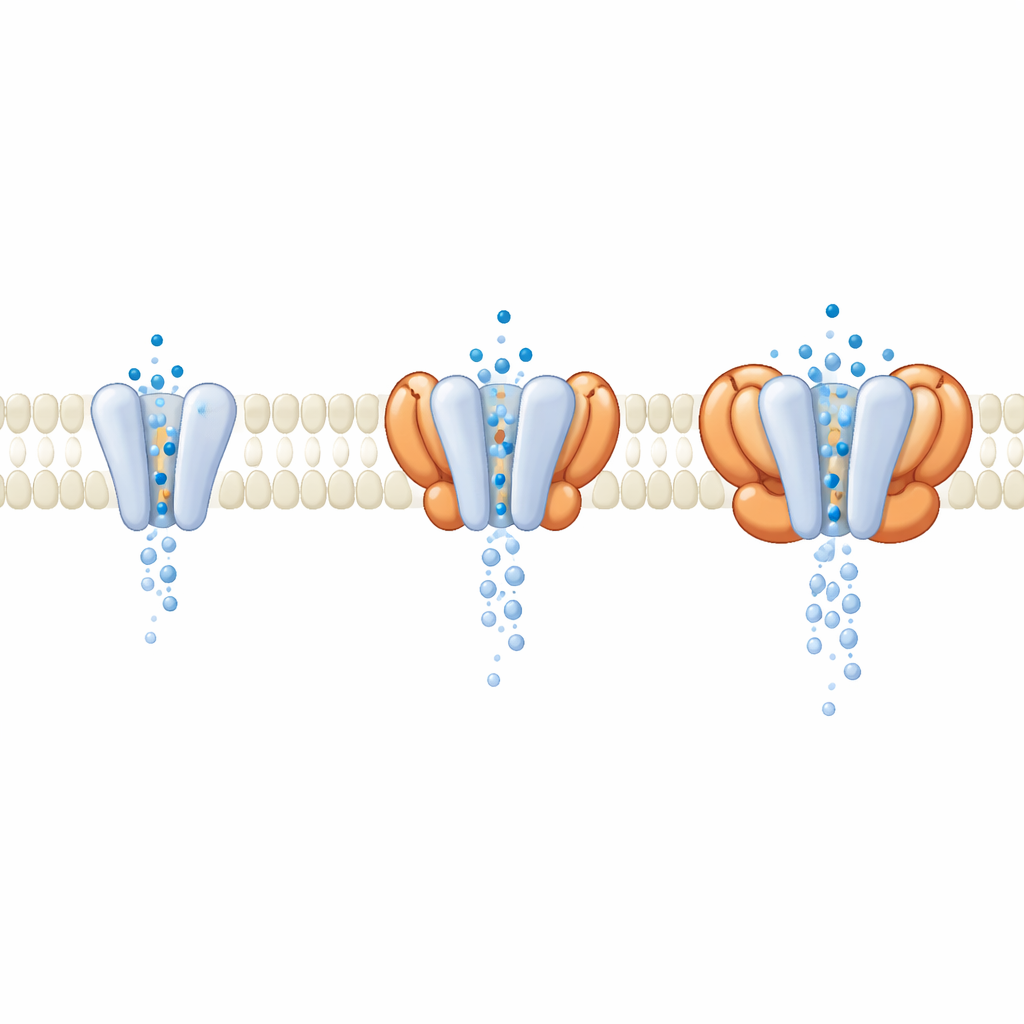
Konsekvenser för inställning av hjärnkretsar och terapier
Tillsammans visar dessa strukturella och simuleringsresultat att både identiteten hos kärnsubenheterna och den specifika uppsättningen hjälpproteiner samverkar för att bestämma hur AMPA-receptorer reglerar elektriska signaler. Hjälpenheter kan vidga eller smalna av poren och kontrollera hur länge receptorer förblir tysta efter intensiv användning, utan nödvändigtvis att förändra hur glutamat känns av. Eftersom AMPA-receptorers felaktiga funktion kopplats till anfallssyndrom, strokeskador och neurodegeneration lyfter de detaljerade kartorna över receptor–hjälpargränssnitten och grindens rörliga delar fram lovande nya läkemedelsmål. Istället för att brett blockera dessa avgörande receptorer skulle framtida läkemedel kunna finjustera specifika assembléer och subtilt justera jonflöde och återhämtning i precis de kretsar som behöver det.
Citering: Yen, L.Y., Newton, T.P., Yelshanskaya, M.V. et al. Auxiliary subunits reshape structural asymmetry and functional plasticity in heterotetrameric GluA1/A2 AMPA receptor core. Nat Commun 17, 4191 (2026). https://doi.org/10.1038/s41467-026-71063-1
Nyckelord: AMPA-receptor, synaptisk plasticitet, hjälpande underenheter, kryoelektronmikroskopi, jonkanalsgrindning