Clear Sky Science · zh
NorQD AAA+ 复合体通过扭转机制驱动金属插入
细胞如何将金属穿入关键酶体
许多维持微生物——最终维持生态系统运转的蛋白质,必须在恰当的位置携带微小的金属离子才能发挥作用。本研究揭示了由两种称为 NorQ 和 NorD 的蛋白组成的专门辅助机器,如何通过物理扭转和拉伸另一种酶,使铁原子得以嵌入到位。理解这一显微尺度的编排有助于解释细菌如何调控土壤中的温室气体化学反应,并可能启发调节含金属催化剂的新方法。
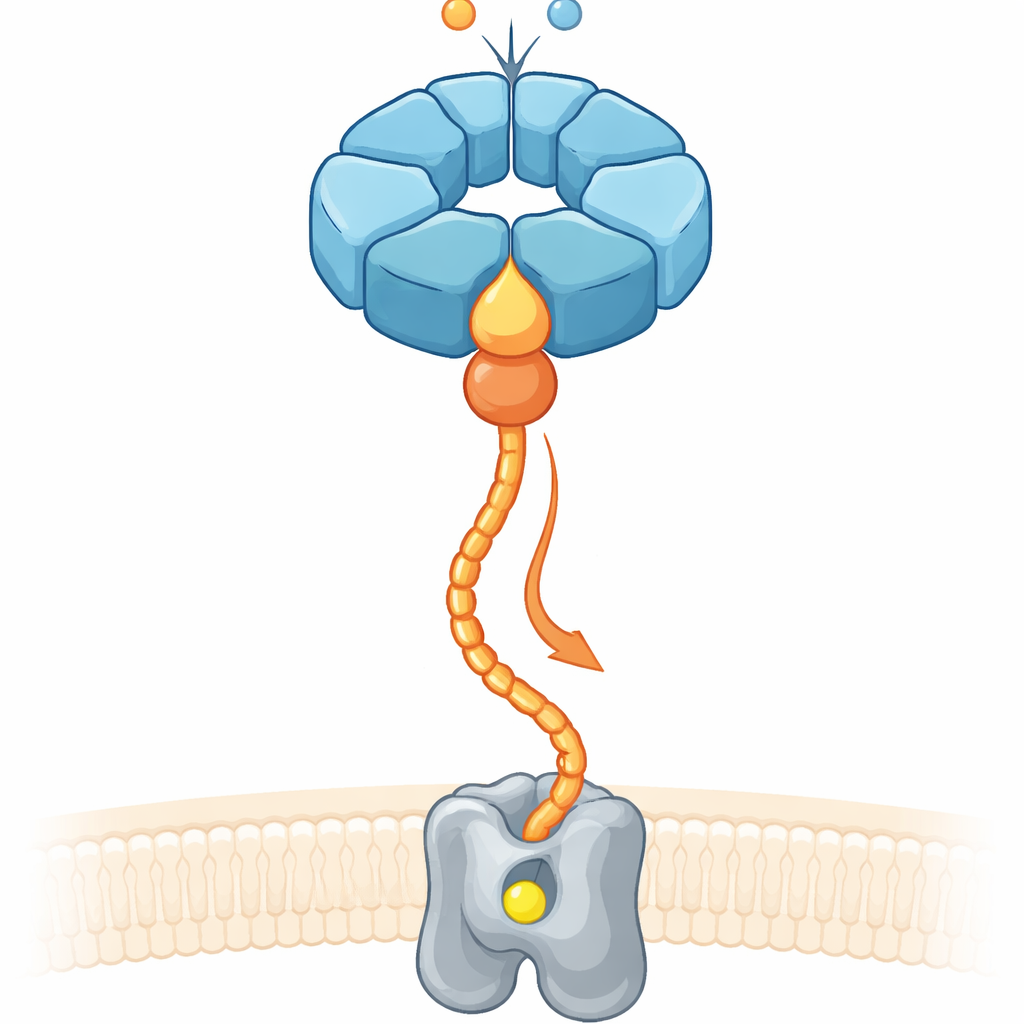
将金属放到正确位置的问题
大约三分之一的已知蛋白需要诸如铁或镁等金属才能发挥功能。然而,仅仅向细胞中大量供应金属离子并不能保证合适的金属会落入正确的口袋。因此,细胞依赖“伴侣”系统,结合未成熟的酶、重塑它们并将金属离子引导入其活性位点。在反硝化的土壤细菌中(这些细菌转化含氮化合物并影响一氧化二氮排放),一种膜酶称为一氧化氮还原酶(cNOR)需要一个非血红素铁原子(称为 FeB)才能活化。先前的工作表明,两种辅助蛋白 NorQ 和 NorD 对安装该铁是必需的,但它们如何协同并利用化学能做出机械性工作仍不清楚。
一个分子环与它的辅助伙伴
NorQ 属于一个大型家族,这类分子马达呈环形,通常形成六聚体环,水解能量丰富的分子 ATP 并拉动穿过其中央孔的蛋白链。NorD 带有一个所谓的 VWA 结构域,这是一个紧凑的搭扣模块,蛋白常通过其内的金属相关接触位点抓取其他伙伴。通过对来自两种细菌的 NorQ 和 NorD 进行高分辨率冷冻电镜研究,结合生化测试和现代结构预测,研究者发现 NorQ 与 NorD 在两个主要接触点相遇。首先,NorD 的 VWA 结构域伸出的一根指状突入深深插入 NorQ 环的中心孔,抵靠一组保守的环片。其次,NorD 的尾端侧向触及一个 NorQ 亚基上的环,正好位于 ATP 关键感知区域之后。
扭转、拉伸与一个关键的柔性连接
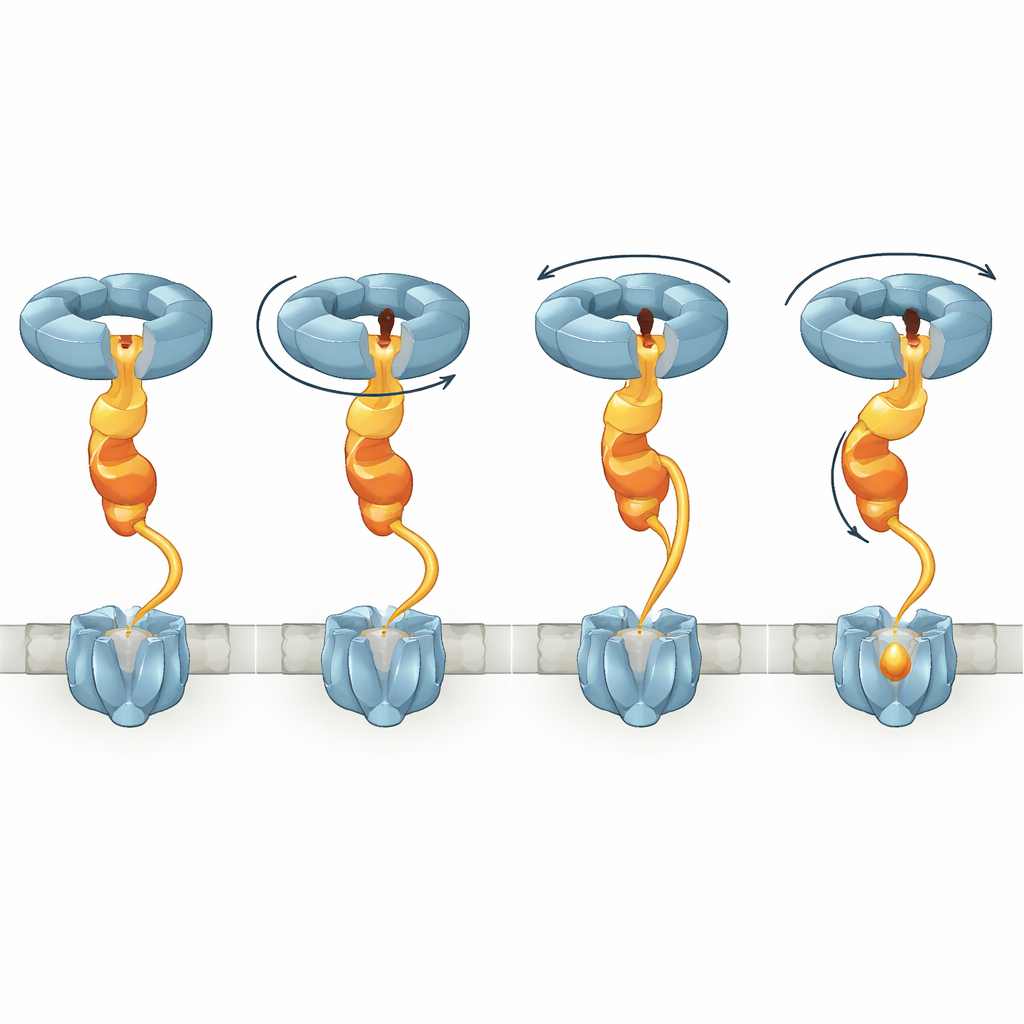
通过比较若干结构状态,研究显示当 NorD 结合时,NorQ 环从相对平坦的形状转变为螺旋楼梯状。不同亚基结合 ATP 或其水解产物 ADP,随着 ATP 结合与水解的进行,位于螺旋底部的活跃亚基向上移动,符合已知的轮换式(hand‑over‑hand)机制。由于 NorD 的指端被夹在孔内而其尾部锚定在特定环上,这些变化会旋转并牵动整个 VWA 结构域。NorD 还包含一段先前不明功能的长连接子,将其 VWA 结构域连接到可能接触 cNOR 的 N 端结构域。作者观察到多种构象,表明该连接子需跨越不同距离,暗示它可以被逐步拉伸。当他们删除该连接子的一部分时,尽管伴侣复合体仍可形成,cNOR 却完全丧失了非血红素铁和活性,这进一步强调了该区域受控拉伸在重塑过程中的核心作用。
从旋转运动到金属插入
将这些结构快照串联起来,作者提出一个模型:NorQ 像一个通过 NorD 起作用的分子绞盘。第一步,NorQ 环通过指入孔与尾对环的接触与 NorD 结合,提高其 ATP 酶活性并将 VWA 结构域锁定到位。接着,NorD 在两个“握点”上与 cNOR 结合:一个涉及其 N 端结构域,另一个涉及 VWA 区或靠近金属结合基序的连接子。随着 NorQ 在 ATP 结合与水解中循环,连续的亚基沿螺旋上攀,牵动 NorD 的指在孔内旋转。这一运动使 VWA 结构域相对于 N 端握点发生扭转,并拉紧连接子,将扭矩和张力传递到 cNOR。所致的畸变被认为会打开 cNOR 中本被屏蔽的区域,允许一个铁离子插入 FeB 位点,随后复合体释放并复位。
为何这项发现超越了单一细菌酶的重要性
对非专业读者来说,结论是 NorQ–NorD 双配对像一个纳米级的活动扳手,在两个点抓住酶并将其扭转到恰到好处,从而使一个铁原子得以就位。这项工作不仅澄清了细菌氮循环中关键步骤的发生方式,还揭示了一种普遍的“指入孔”策略,类似的马达–伙伴系统可能在生物界广泛采用。通过展示化学燃料如何被转换为对目标蛋白的精确扭转力,研究为理解——甚至将来可能改造——那些控制金属何时何地被装配进复杂分子装置的机器提供了蓝图。
引用: Kahle, M., Appelgren, S., König, F. et al. NorQD AAA+ complex drives metal insertion by a twisting mechanism. Nat Commun 17, 3032 (2026). https://doi.org/10.1038/s41467-026-71044-4
关键词: AAA+ ATP酶, 金属伴侣蛋白, 一氧化氮还原酶, 冷冻电镜结构, 金属辅因子插入