Clear Sky Science · fr
Le complexe NorQD AAA+ insère les métaux par un mécanisme de torsion
Comment les cellules fichent les métaux dans des enzymes clés
Beaucoup des protéines qui maintiennent les microbes — et, in fine, les écosystèmes — en activité doivent porter de tous petits ions métalliques au bon endroit pour fonctionner. Cette étude révèle comment une machine d’aide spécialisée, constituée de deux protéines appelées NorQ et NorD, tord et étire physiquement une autre enzyme afin qu’un atome de fer puisse être emboîté. Comprendre cette chorégraphie microscopique aide à expliquer comment les bactéries contrôlent la chimie des gaz à effet de serre dans les sols et pourrait inspirer de nouvelles manières d’ajuster des catalyseurs contenant des métaux.
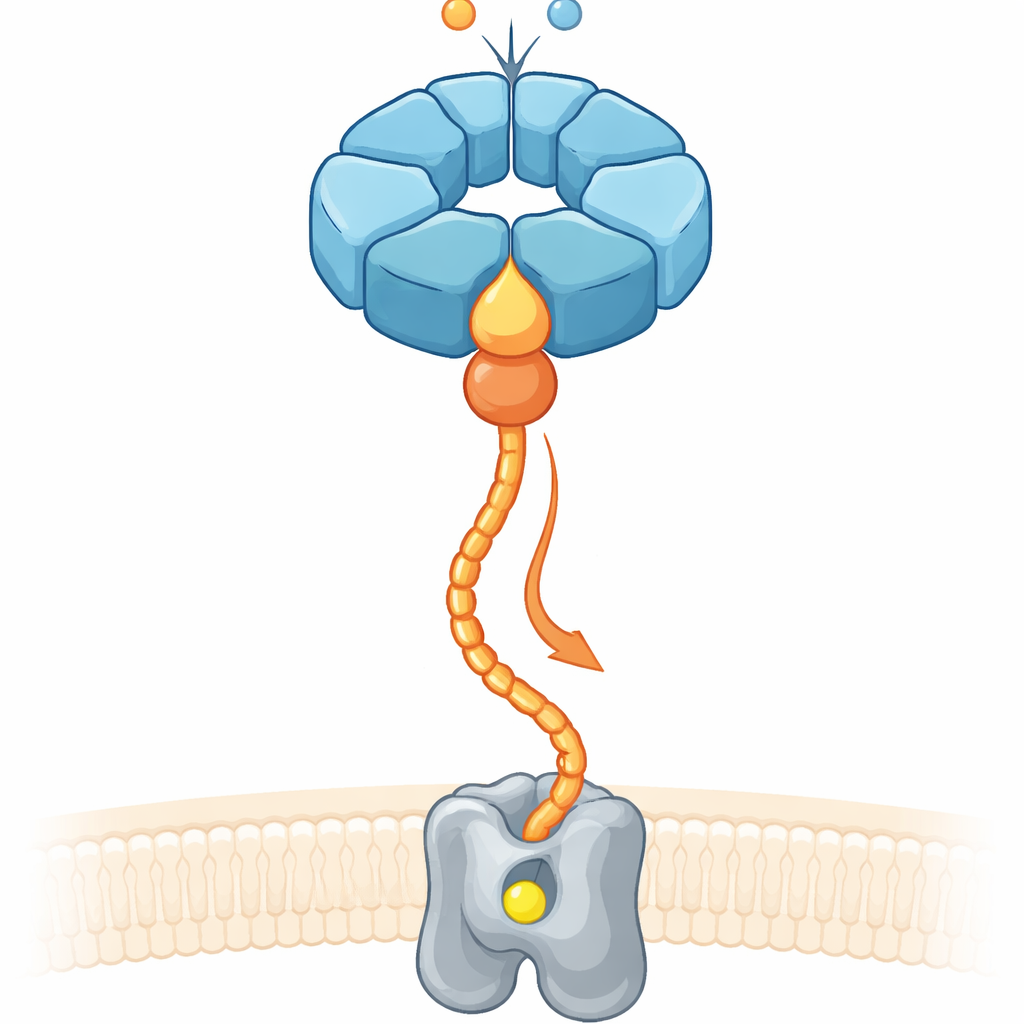
Le problème de placer les métaux au bon endroit
Environ un tiers de toutes les protéines connues nécessitent des métaux tels que le fer ou le magnésium pour fonctionner. Pourtant, inonder une cellule d’ions métalliques ne garantit pas que le bon métal ira se loger dans le bon creux. Les cellules s’appuient donc sur des systèmes « chaperons » qui se lient aux enzymes inachevées, les remodelent et guident les ions métalliques vers leurs sites actifs. Chez les bactéries dénitrifiantes du sol, qui transforment des composés azotés et influencent les émissions de protoxyde d’azote, une enzyme membranaire appelée réductase de l’oxyde nitrique (cNOR) nécessite un atome de fer non‑héminique (appelé FeB) pour devenir active. Des travaux antérieurs avaient montré que deux protéines accessoires, NorQ et NorD, sont essentielles pour installer ce fer, mais la façon dont elles coopéraient et utilisaient l’énergie chimique pour produire un travail mécanique restait floue.
Une bague moléculaire et son partenaire d’aide
NorQ appartient à une grande famille de moteurs moléculaires en forme d’anneau, connus pour former des anneaux à six sous‑unités qui consument la molécule riche en énergie ATP et tirent sur des chaînes protéiques passant dans leur pore central. NorD porte un domaine dit VWA, un module compact d’accrochage souvent utilisé par les protéines pour saisir d’autres partenaires via un site de contact dépendant d’un métal. En combinant la cryo‑microscopie électronique haute résolution sur NorQ et NorD issus de deux espèces bactériennes, des essais biochimiques et des prédictions de structure modernes, les auteurs ont constaté que NorQ et NorD se rencontrent en deux points de contact principaux. D’une part, une projection en forme de doigt provenant du domaine VWA de NorD s’insère profondément dans le pore central de l’anneau NorQ, venant se nicher contre un ensemble de boucles conservées. D’autre part, l’extrémité C‑terminale de NorD atteint latéralement une boucle d’une sous‑unité de NorQ située juste après une région clé détectrice d’ATP.
Torsion, étirement et un lien flexible critique
En comparant plusieurs états structuraux, l’étude montre que lorsque NorD se lie, l’anneau NorQ passe d’une forme relativement plate à une configuration en escalier en spirale. Différentes sous‑unités portent de l’ATP ou sa forme consommée, l’ADP, et à mesure que la liaison et l’hydrolyse de l’ATP progressent, la sous‑unité active en bas de la spirale monte d’un cran, conformément à un mécanisme connu de type « passage de main en main ». Parce que le doigt de NorD est verrouillé à l’intérieur du pore tandis que sa queue est ancrée sur une boucle spécifique, ces changements font tourner et tirer l’ensemble du domaine VWA. NorD contient aussi un long linker jusqu’ici mystérieux reliant son domaine VWA à un domaine N‑terminal qui contacte probablement la cNOR. Les auteurs observent plusieurs conformations dans lesquelles ce linker doit couvrir des distances différentes, ce qui implique qu’il peut être étiré progressivement. Quand ils ont supprimé des portions de ce linker, la cNOR a perdu complètement son fer non‑héminique et son activité, même si le complexe chaperon pouvait encore se former, ce qui souligne que l’étirement contrôlé de cette région est central pour le travail de remodelage.
De la rotation à l’insertion du métal
En reliant les clichés structuraux, les auteurs proposent un modèle dans lequel NorQ se comporte comme un treuil moléculaire agissant via NorD. Dans un premier temps, l’anneau NorQ s’associe à NorD via le doigt‑dans‑le‑pore et le contact queue‑vers‑boucle, augmentant son activité ATPasique et verrouillant le domaine VWA en position. Ensuite, NorD engage la cNOR à deux « points de prise » : l’un impliquant son domaine N‑terminal et l’autre impliquant la région VWA ou le linker proche d’un motif de liaison au métal. À mesure que NorQ cycle entre liaison et hydrolyse de l’ATP, des sous‑unités successives gravissent la spirale, entraînant le doigt de NorD autour du pore. Ce mouvement torsionne le domaine VWA par rapport à la prise N‑terminale et tend le linker, transmettant couple et tension à la cNOR. La distorsion résultante ouvrirait une région autrement protégée de la cNOR, permettant l’insertion d’un ion fer dans le site FeB, après quoi le complexe peut se libérer et se réinitialiser.
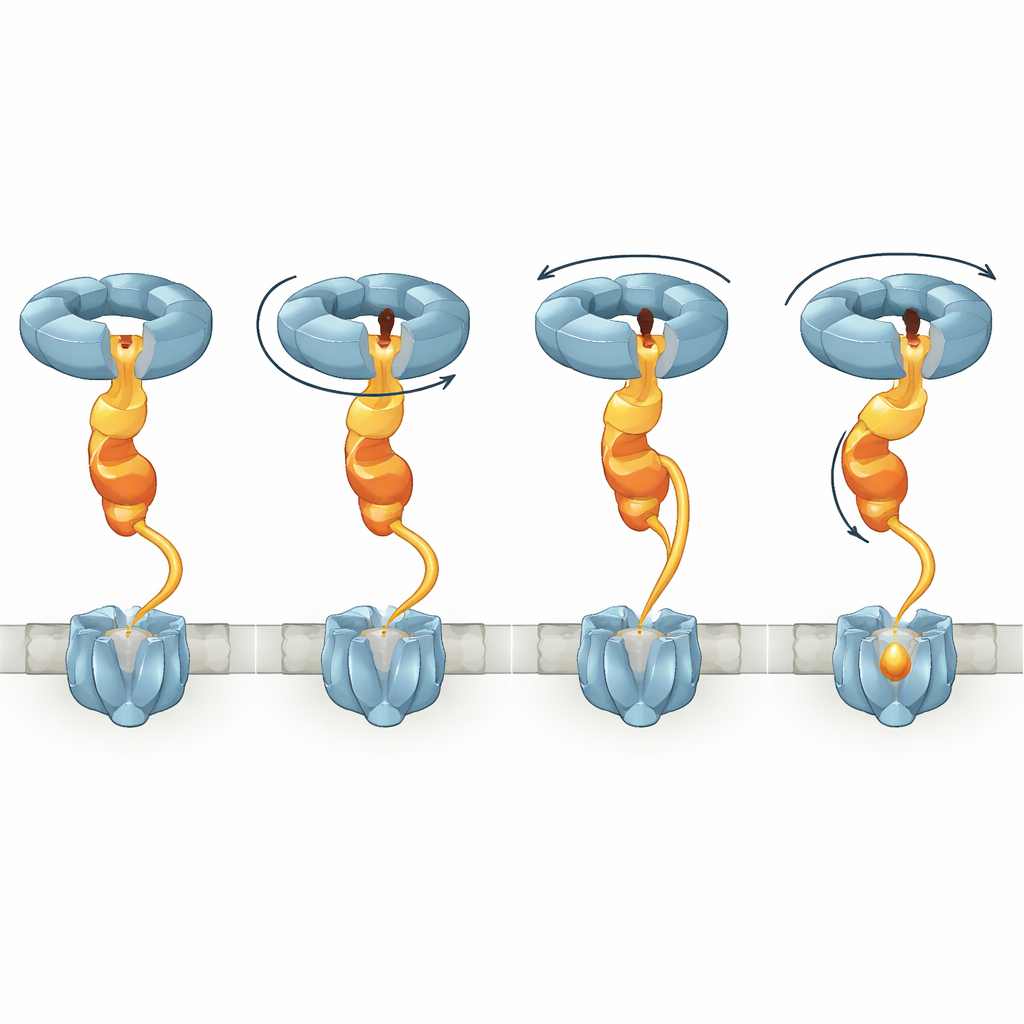
Pourquoi cela compte au‑delà d’une enzyme bactérienne
Pour un non‑spécialiste, l’idée principale est que la paire NorQ–NorD agit comme une clé anglaise nanoscopique, saisissant une enzyme en deux points et la tordant juste assez pour faire glisser un atome de fer en place. Ce travail clarifie non seulement comment se déroule une étape clé de la chimie de l’azote bactérienne, mais révèle aussi une stratégie générale « doigt‑dans‑le‑pore » que des systèmes moteur‑partenaire similaires pourraient utiliser à travers la biologie. En montrant comment le carburant chimique est converti en une force de torsion précise sur une protéine cible, l’étude fournit une feuille de route pour comprendre — et peut‑être un jour concevoir — des machines qui contrôlent où et quand les métaux sont intégrés dans des dispositifs moléculaires complexes.
Citation: Kahle, M., Appelgren, S., König, F. et al. NorQD AAA+ complex drives metal insertion by a twisting mechanism. Nat Commun 17, 3032 (2026). https://doi.org/10.1038/s41467-026-71044-4
Mots-clés: ATPase AAA+, métallochaperon, réductase de l’oxyde nitrique, structure cryo‑EM, insertion de cofacteur métallique