Clear Sky Science · es
El complejo NorQD AAA+ impulsa la inserción de metales mediante un mecanismo de torsión
Cómo las células enhebran metales en enzimas clave
Muchas de las proteínas que mantienen a los microbios —y en última instancia a los ecosistemas— funcionando deben llevar pequeños iones metálicos en el lugar exacto para ser activas. Este estudio desvela cómo una máquina ayudante especializada, formada por dos proteínas llamadas NorQ y NorD, torsiona y estira físicamente a otra enzima para que un átomo de hierro pueda encajarse en su sitio. Comprender esta coreografía microscópica ayuda a explicar cómo las bacterias controlan la química de los gases de efecto invernadero en los suelos y podría inspirar nuevas maneras de ajustar catalizadores que contienen metales.
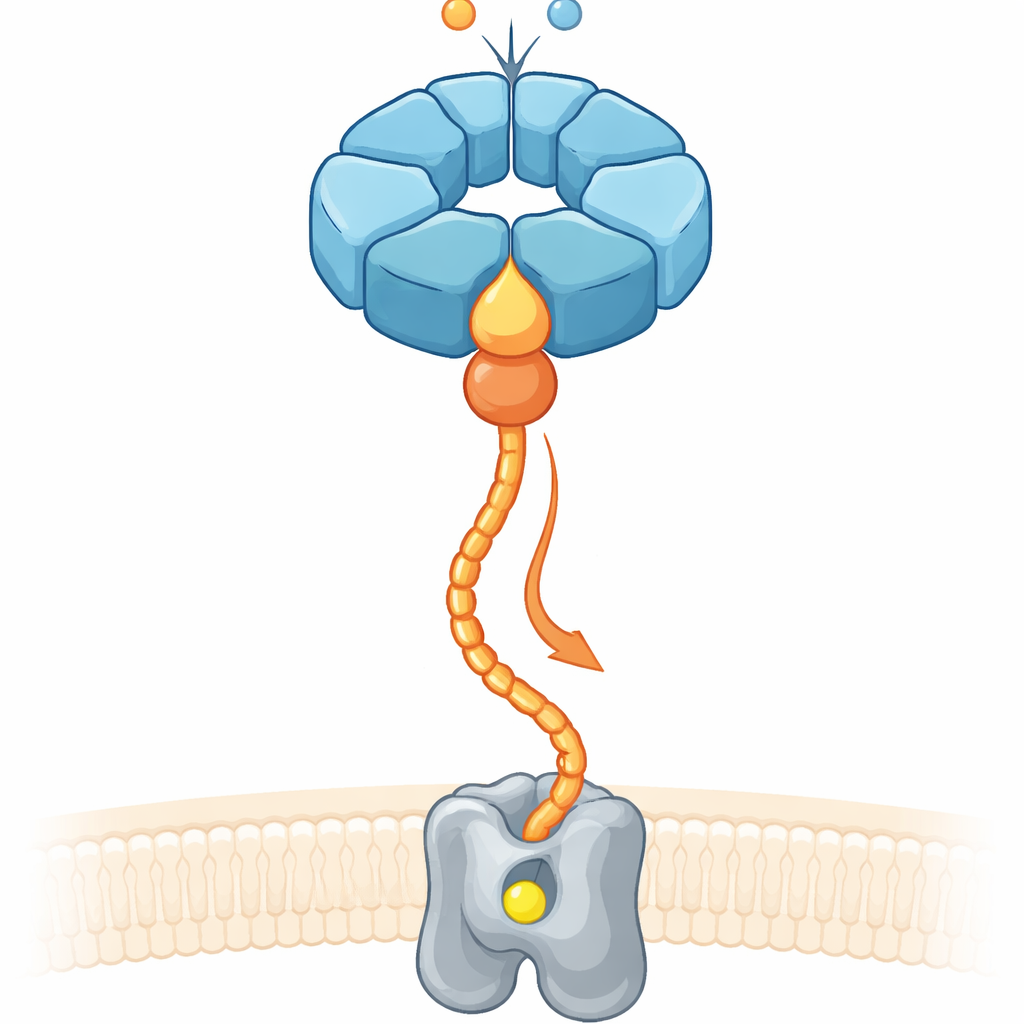
El problema de colocar los metales en el sitio correcto
Aproximadamente un tercio de todas las proteínas conocidas necesitan metales como hierro o magnesio para funcionar. Sin embargo, simplemente saturar la célula con iones metálicos no garantiza que el metal correcto ocupe el bolsillo adecuado. Por ello, las células dependen de sistemas «chaperona» que se unen a enzimas en formación, las remodelan y guían los iones metálicos hacia sus sitios activos. En bacterias desnitrificantes del suelo, que transforman compuestos de nitrógeno e influyen en las emisiones de óxido nitroso, una enzima de membrana llamada reductasa de óxido nítrico (cNOR) requiere un átomo de hierro no ‑ hemo (denominado FeB) para activarse. Trabajos previos mostraron que dos proteínas accesorias, NorQ y NorD, son esenciales para instalar este hierro, pero no quedaba claro cómo cooperaban y cómo usaban energía química para realizar trabajo mecánico.
Un anillo molecular y su socio ayudante
NorQ pertenece a una gran familia de motores moleculares en forma de anillo, conocidos por formar anillos de seis subunidades que consumen la molécula energética ATP y tiran de cadenas proteicas enhebradas por sus poros centrales. NorD porta un dominio VWA, un módulo compacto de anclaje que con frecuencia emplean las proteínas para capturar a otras mediante un sitio de contacto dependiente de metal. Usando microscopía crioelectrónica de alta resolución sobre NorQ y NorD procedentes de dos especies bacterianas, junto con ensayos bioquímicos y predicción estructural moderna, los autores encontraron que NorQ y NorD se encuentran en dos puntos de contacto principales. Primero, una proyección en forma de dedo del dominio VWA de NorD se inserta profundamente en el poro central del anillo de NorQ, acomodándose contra un conjunto de bucles conservados. Segundo, el extremo distal de NorD alcanza lateralmente para tocar un bucle de una subunidad de NorQ que se sitúa justo después de una región sensora clave para el ATP.
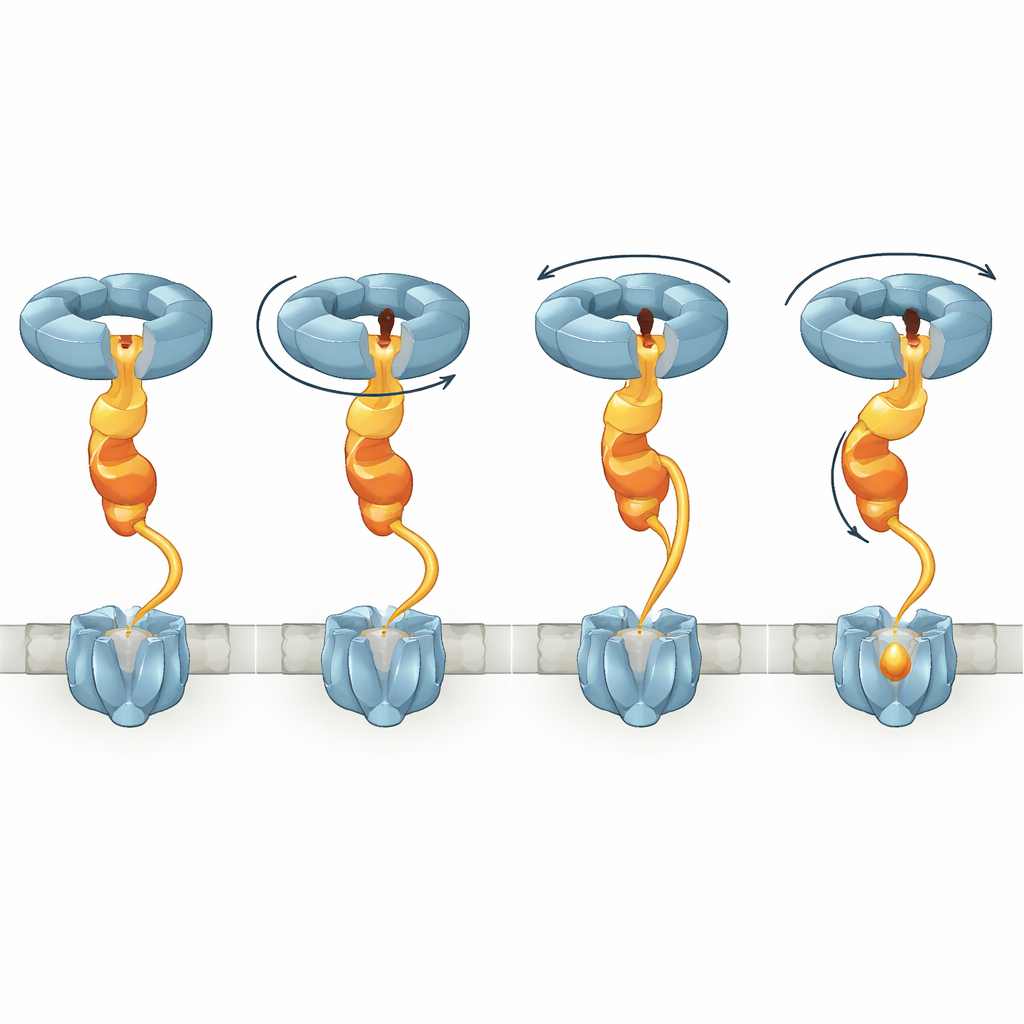
Torsión, estiramiento y un enlace flexible crucial
Al comparar varios estados estructurales, el estudio muestra que cuando NorD se une, el anillo de NorQ cambia de una forma relativamente plana a una disposición en escalera helicoidal. Diferentes subunidades contienen ATP o su forma gastada, ADP, y a medida que la unión y la hidrólisis de ATP progresan, la subunidad activa en la base de la espiral asciende, coherente con un mecanismo conocido de paso de mano a mano. Dado que el «dedo» de NorD queda fijado dentro del poro mientras su cola está anclada a un bucle concreto, estos cambios rotan y tiran de todo el dominio VWA. NorD también contiene un enlazador largo y hasta ahora enigmático que conecta su dominio VWA con un dominio N‑terminal que probablemente contacta cNOR. Los autores observan múltiples conformaciones en las que este enlazador debe abarcar distancias distintas, lo que implica que puede estirarse de manera progresiva. Cuando eliminaron partes de este enlazador, cNOR perdió por completo su hierro no‑hemo y su actividad, pese a que el complejo chaperona podía seguir formándose, subrayando que el estiramiento controlado de esta región es central para la remodelación.
De un movimiento rotatorio a la inserción del metal
Uniendo las instantáneas estructurales, los autores proponen un modelo en el que NorQ actúa como un cabrestante molecular que opera a través de NorD. En el primer paso, el anillo de NorQ se asocia con NorD mediante los contactos dedo‑en‑poro y cola‑a‑bucle, aumentando su actividad ATPasa y bloqueando el dominio VWA en posición. A continuación, NorD se engancha a cNOR en dos «puntos de agarre»: uno que implica su dominio N‑terminal y otro que implica la región VWA o el enlazador cerca de un motivo de unión al metal. A medida que NorQ cicla la unión y la hidrólisis de ATP, subunidades sucesivas trepan por la espiral, arrastrando el dedo de NorD alrededor dentro del poro. Este movimiento tuerce el dominio VWA con respecto al agarre N‑terminal y tensa el enlazador, transmitiendo par y tensión a cNOR. Se propone que la distorsión resultante abre una región de cNOR que de otro modo estaría protegida, permitiendo que un ion de hierro se inserte en el sitio FeB, tras lo cual el complejo puede liberarse y reiniciarse.
Por qué esto importa más allá de una enzima bacteriana
Para un no especialista, la conclusión es que el par NorQ–NorD actúa como una llave de tubo a nanoescala, agarrando una enzima en dos puntos y torsionándola lo justo para deslizar un átomo de hierro en su sitio. Este trabajo no solo aclara cómo ocurre un paso clave en la química bacteriana del nitrógeno, sino que también revela una estrategia general de «dedo‑en‑el‑poro» que sistemas motor‑socio similares podrían emplear a lo largo de la biología. Al mostrar cómo el combustible químico se convierte en una fuerza de torsión precisa sobre una proteína objetivo, el estudio ofrece un plano para entender —y quizás algún día diseñar— máquinas que controlen dónde y cuándo se incorporan metales en complejos dispositivos moleculares.
Cita: Kahle, M., Appelgren, S., König, F. et al. NorQD AAA+ complex drives metal insertion by a twisting mechanism. Nat Commun 17, 3032 (2026). https://doi.org/10.1038/s41467-026-71044-4
Palabras clave: AAA+ ATPasa, metalochaperona, reductasa de óxido nítrico, estructura por crio‑EM, inserción de cofactor metálico