Clear Sky Science · tr
NorQD AAA+ kompleksi bükülme mekanizmasıyla metal yerleştirmeyi sağlar
Hücreler Metalleri Anahtar Enzimlere Nasıl İplikler
Mikropları — ve nihayetinde ekosistemleri — işleyen birçok protein, işleyebilmek için küçük metal iyonlarını tam doğru noktada taşımak zorundadır. Bu çalışma, NorQ ve NorD adındaki iki proteinden oluşan özel bir yardımcı makinenin, bir diğer enzimi fiziksel olarak büküp gererek bir demir atomunun yerleştirilmesini nasıl sağladığını ortaya koyuyor. Bu mikroskobik koreografiyi anlamak, bakterilerin topraktaki sera gazı kimyasını nasıl kontrol ettiğini açıklamaya yardımcı olur ve metal içeren katalizörleri ayarlamak için yeni yaklaşımlara ilham verebilir.
Metalleri Doğru Yere Koyma Sorunu
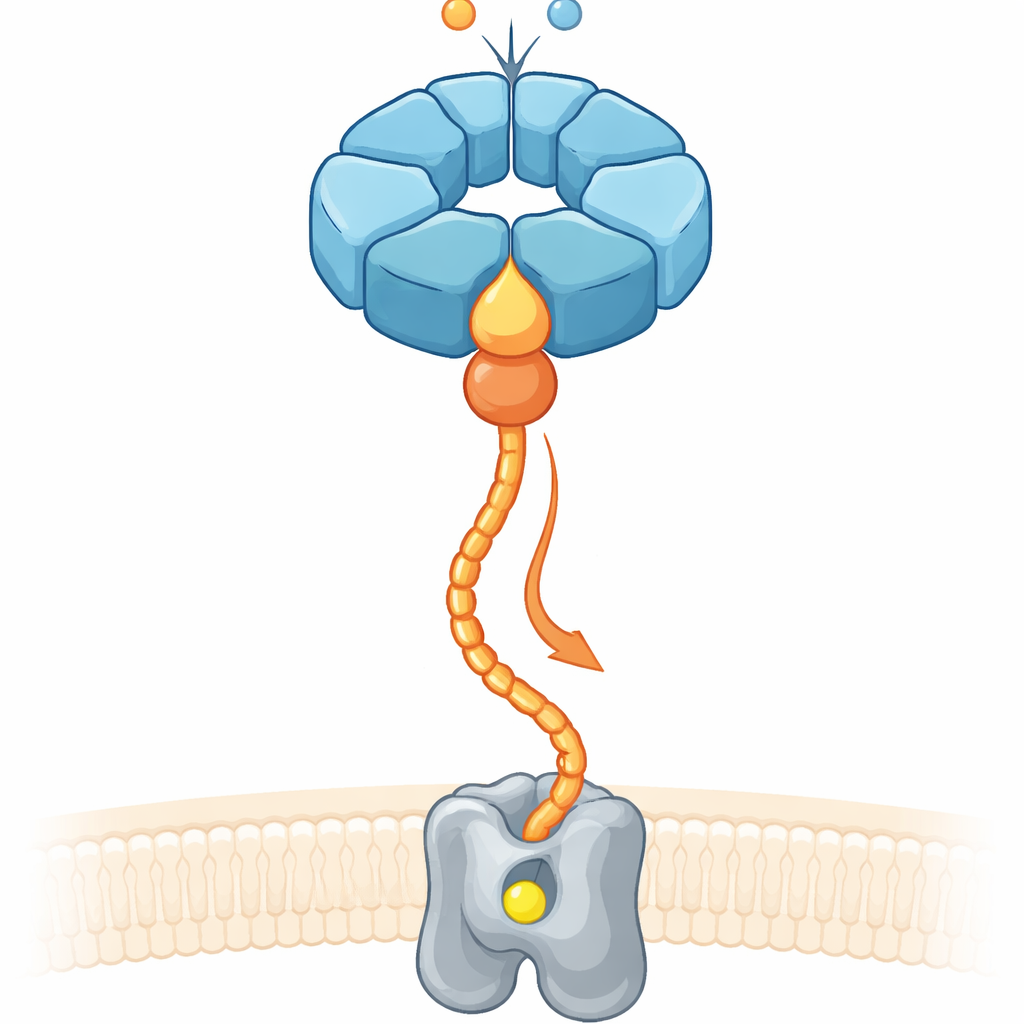
Tüm bilinen proteinlerin yaklaşık üçte biri işlemek için demir veya magnezyum gibi metallere ihtiyaç duyar. Ancak hücreyi metal iyonlarıyla doldurmak, doğru metalin doğru cepte yerleşeceğini garanti etmez. Bu nedenle hücreler, tamamlanmamış enzimlere bağlanan, onları yeniden şekillendiren ve metal iyonlarını aktif bölgelerine yönlendiren “kaperon” sistemlerine güvenir. Azot bileşiklerini dönüştüren ve azot oksit emisyonlarını etkileyen denitrifiye toprak bakterilerinde, membrana bağlı bir enzim olan nitrik oksit redüktaz (cNOR) aktif hale gelmek için non‑hem bir demir atomu (FeB olarak adlandırılır) gerektirir. Önceki çalışmalar, NorQ ve NorD adlı iki yardımcı proteinin bu demiri takmak için gerekli olduğunu göstermişti, ancak bunların nasıl işbirliği yaptığı ve kimyasal enerjiyi mekanik işe nasıl dönüştürdüğü belirsizdi.
Moleküler Bir Halka ve Yardımcı Ortağı
NorQ, altı altbirimli halkalar oluşturarak ATP adlı enerji açısından zengin molekülü harcayan ve merkezi gözeneklerinden geçirilen protein zincirlerini çeken halka biçimli moleküler motorlardan oluşan büyük bir aileye aittir. NorD ise genellikle bir metal‑temelli temas bölgesi aracılığıyla diğer partnerleri tutmak için kullanılan kompakt bir kilit modülü olan VWA (Von Willebrand A) domeni taşır. İki bakteri türünden NorQ ve NorD üzerinde yüksek çözünürlüklü kryo‑elektron mikroskopisi, biyokimyasal testler ve modern yapı tahmini kullanan yazarlar, NorQ ve NorD’nin iki ana temas noktasında buluştuğunu saptadılar. Birincisi, NorD’nin VWA domeninden çıkan parmak biçimli bir çıkıntı NorQ halkasının merkezi gözeneklerine derinlemesine girer ve korunmuş bir dizi döngüye yaslanır. İkincisi, NorD’nin kuyruk ucu yana doğru uzanıp ATP için anahtar bir sensör bölgesinin hemen ötesindeki bir NorQ altbiriminin bir döngüsüne dokunur.
Bükülme, Gerilme ve Kritik Esnek Bağlantı
Birkaç yapısal durumu karşılaştırarak, çalışma NorD bağlandığında NorQ halkasının nispeten düz bir yapıdan spiral merdivene dönüştüğünü gösteriyor. Farklı altbirimler ATP veya onun harcanmış biçimi ADP tutar ve ATP bağlanması ile hidrolizi ilerledikçe, spiralın altındaki aktif altbirim yukarı doğru adım atar; bu bilinen el‑üstüne‑el mekanizmasıyla uyumludur. NorD’nin parmağı gözenek içinde sıkıca sabitlenmişken kuyruğu belirli bir döngüye ankrajlandığı için bu değişimler tüm VWA domenini döndürür ve çeker. NorD ayrıca VWA domenini cNOR ile temas etme olası N‑terminus domenine bağlayan daha önce gizemli olan uzun bir bağlantı ipine sahiptir. Yazarlar, bu bağlantının farklı mesafeleri kapsaması gereken birden çok konformasyon gözlemlediler; bu da bağlantının kademeli olarak gerilebileceğini gösterir. Bu bağlantının parçalarını sildiklerinde, kaperon kompleksi oluşabilmesine rağmen cNOR tümüyle non‑hem demirini ve aktivitesini kaybetti; bu durum, bu bölgenin kontrollü gerilmesinin yeniden şekillendirme işinin merkezinde olduğunu vurgular.
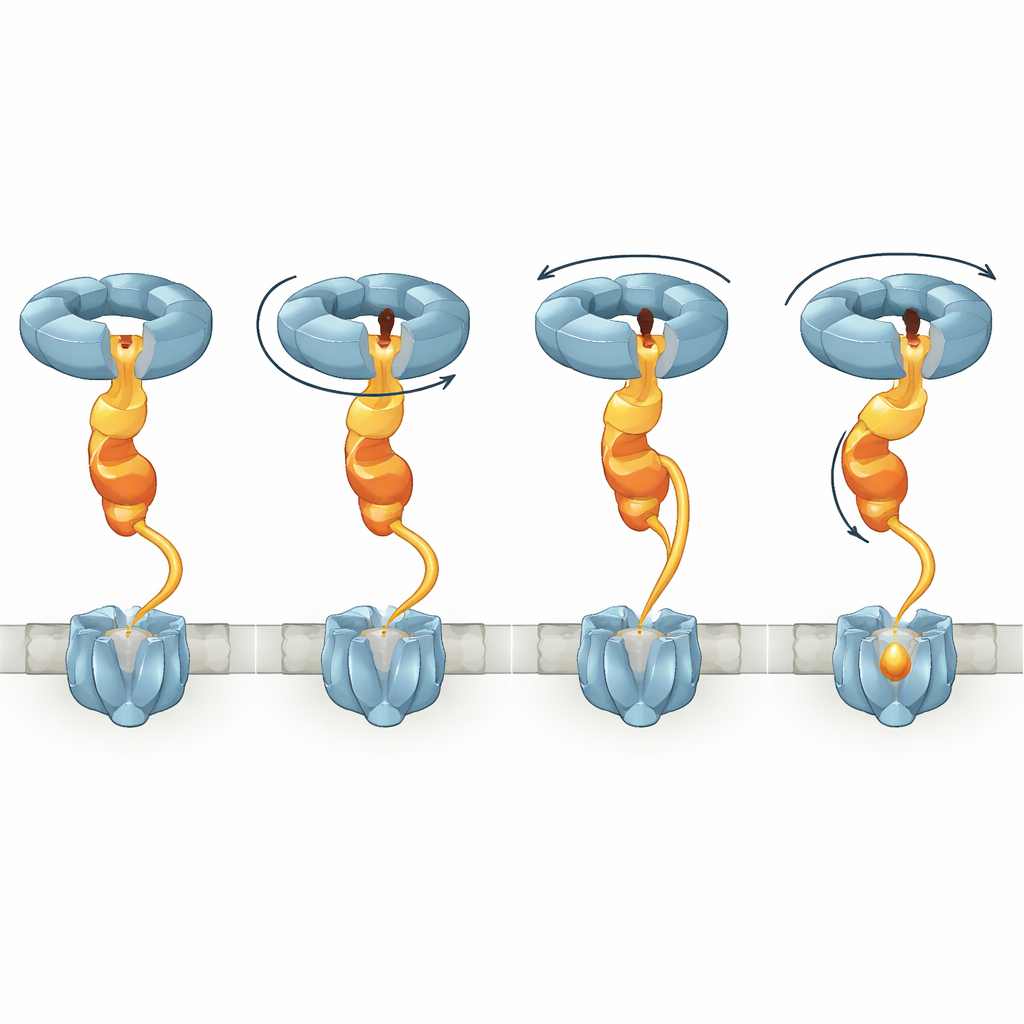
Döner Hareketten Metal Yerleştirmeye
Yapısal anlık görüntüleri birleştirerek yazarlar, NorQ’nin NorD aracılığıyla çalışan moleküler bir vinç gibi davrandığı bir model öneriyor. İlk adımda, NorQ halkası parmak‑gözenek ve kuyruk‑döngü temasları yoluyla NorD ile birleşir; bu, ATPaz aktivitesini artırır ve VWA domenini kilitler. Sonra NorD, cNOR ile iki “tutma noktası” üzerinde etkileşir: biri N‑terminal domeniyle ilgili, diğeri ise VWA bölgesi veya metal bağlayan motifin yakınındaki bağlantı ile ilgilidir. NorQ ATP bağlanması ve hidrolizi döngüsünü sürdürürken ardışık altbirimler spirali tırmanır ve NorD parmağını gözenek içinde döndürür. Bu hareket VWA domenini N‑terminus tutamağına göre çevirir ve bağlantıyı gerginleştirir; böylece tork ve gerilim cNOR’a iletilir. Ortaya çıkan bozulmanın cNOR’un aksi halde korunmuş bir bölgesini açtığı, böylece bir demir iyonunun FeB bölgesine yerleştirilmesine izin verdiği ve ardından kompleksin serbestleşip sıfırlanabildiği öne sürülür.
Bu Çalışmanın Bir Bakteri Enziminden Öte Önemi
Bir uzman olmayan için çıkarım şudur: NorQ–NorD çifti, bir enzimi iki noktadan kavrayıp onu bir demir atomunu yerleştirebilecek kadar döndüren nanoskala bir boru‑anahtarı gibi davranır. Bu çalışma yalnızca bakteriyel azot kimyasındaki önemli bir adımın nasıl gerçekleştiğini netleştirmekle kalmaz, aynı zamanda benzer motor‑partner sistemlerin biyolojide kullanabileceği genel bir “parmak‑gözenek” stratejisini ortaya koyar. Kimyasal yakıtın hedef bir protein üzerinde hassas bir bükme kuvvetine nasıl dönüştürüldüğünü göstermesi, metalin karmaşık moleküler aygıtlara nerede ve ne zaman yerleştirildiğini kontrol eden makinelerin anlaşılması — ve belki bir gün tasarlanması — için bir plan sunar.
Atıf: Kahle, M., Appelgren, S., König, F. et al. NorQD AAA+ complex drives metal insertion by a twisting mechanism. Nat Commun 17, 3032 (2026). https://doi.org/10.1038/s41467-026-71044-4
Anahtar kelimeler: AAA+ ATPaz, metallokaperon, nitrik oksit redüktaz, kryo-EM yapı, metal kofaktör yerleştirme