Clear Sky Science · nl
NorQD AAA+ complex drijft metaalinzet aan door een draaiend mechanisme
Hoe cellen metalen in sleutelenzymen rijgen
Veel van de eiwitten die microben — en uiteindelijk ecosystemen — laten functioneren, moeten kleine metaalionen precies op de juiste plek dragen om actief te zijn. Deze studie onthult hoe een gespecialiseerd hulpmachientje, opgebouwd uit twee eiwitten genaamd NorQ en NorD, een ander enzym fysiek draait en rekt zodat een ijzeratoom op zijn plaats kan worden geschoven. Begrijpen van dit microscopische choreografie verklaart hoe bacteriën de broeikasgaschemie in bodems beheersen en kan nieuwe ideeën opleveren om metaalhoudende katalysatoren bij te sturen.
Het probleem van metalen op de juiste plaats krijgen
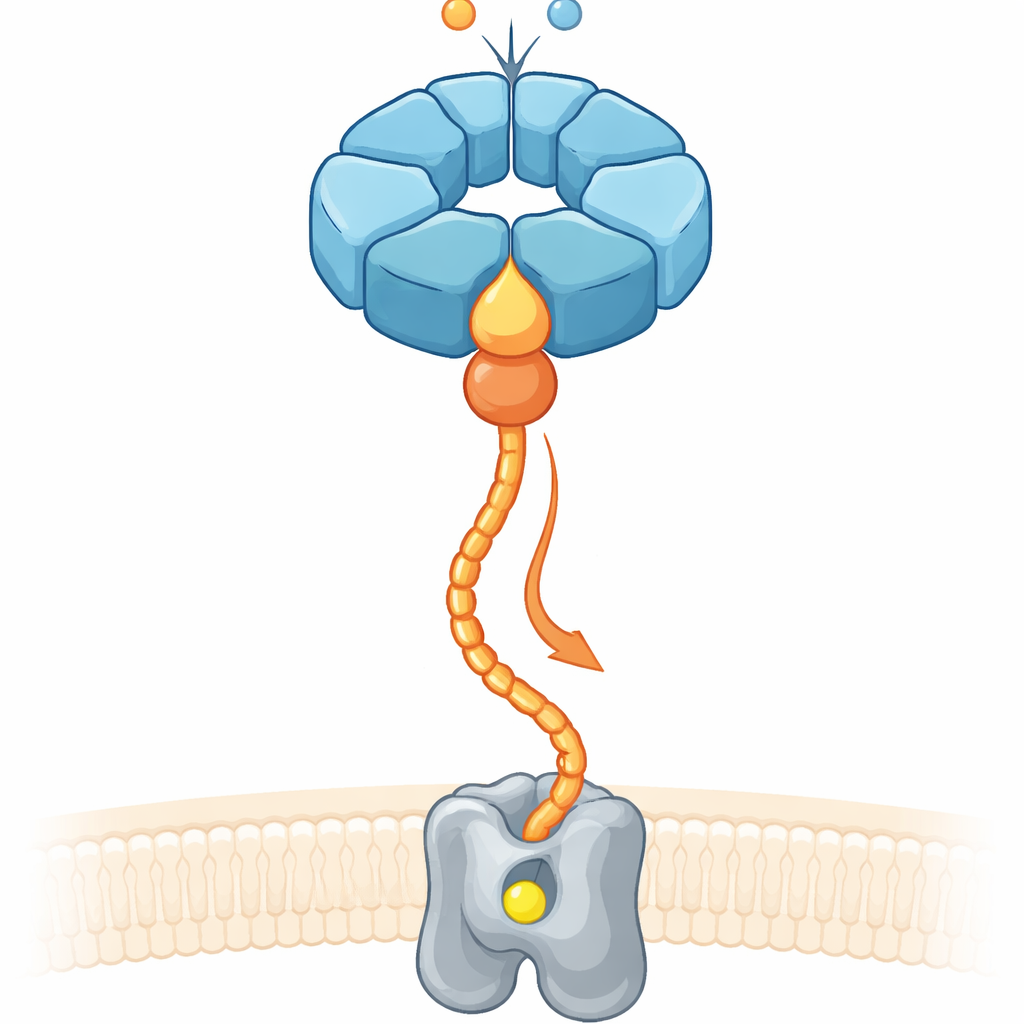
Ongeveer een derde van alle bekende eiwitten heeft metalen zoals ijzer of magnesium nodig om te functioneren. Toch betekent het simpelweg overvloedig beschikbaar stellen van metaalionen in de cel niet dat het juiste metaal in het juiste zakje belandt. Cellen vertrouwen daarom op “chaperonne”-systemen die binden aan onvoltooide enzymen, ze vervormen en metalen naar hun actieve centra leiden. Bij denitrificerende bodembacteriën, die stikstofverbindingen omzetten en de uitstoot van lachgas beïnvloeden, heeft een membraaneiwit genaamd nitric oxide reductase (cNOR) een niet‑heme ijzeratoom nodig (FeB) om actief te zijn. Eerder werk liet zien dat twee hulpverlenende eiwitten, NorQ en NorD, essentieel zijn voor het plaatsen van dit ijzer, maar hoe ze samenwerkten en chemische energie gebruikten om mechanisch werk te verrichten, bleef onduidelijk.
Een moleculaire ring en zijn hulpende partner
NorQ behoort tot een grote familie van ringvormige moleculaire motoren, bekend om het vormen van zessubeenheidsringen die de energierijke molecule ATP verbranden en aan eiwitketens trekken die door hun centrale poriën worden geregen. NorD draagt een zogenaamde VWA‑domein, een compact vergrendelingsmodule die eiwitten vaak gebruiken om andere partners vast te grijpen via een metaalgebaseerde contactplaats. Met hoogresolutie cryo‑elektronenmicroscopie van NorQ en NorD uit twee bacteriesoorten, samen met biochemische tests en moderne structurele voorspelling, vonden de auteurs dat NorQ en NorD elkaar op twee hoofdcontactpunten ontmoeten. Ten eerste steekt een vingerachtige uitstulping van het VWA‑domein van NorD diep in de centrale porie van de NorQ‑ring en nestelt zich tegen een reeks geconserveerde lussen. Ten tweede reikt het staartuiteinde van NorD zijdelings om een lus op een NorQ‑subeenheid aan te raken die net voorbij een sleutel‑sensorregio voor ATP ligt.
Draaien, rekken en een cruciale flexibele schakel
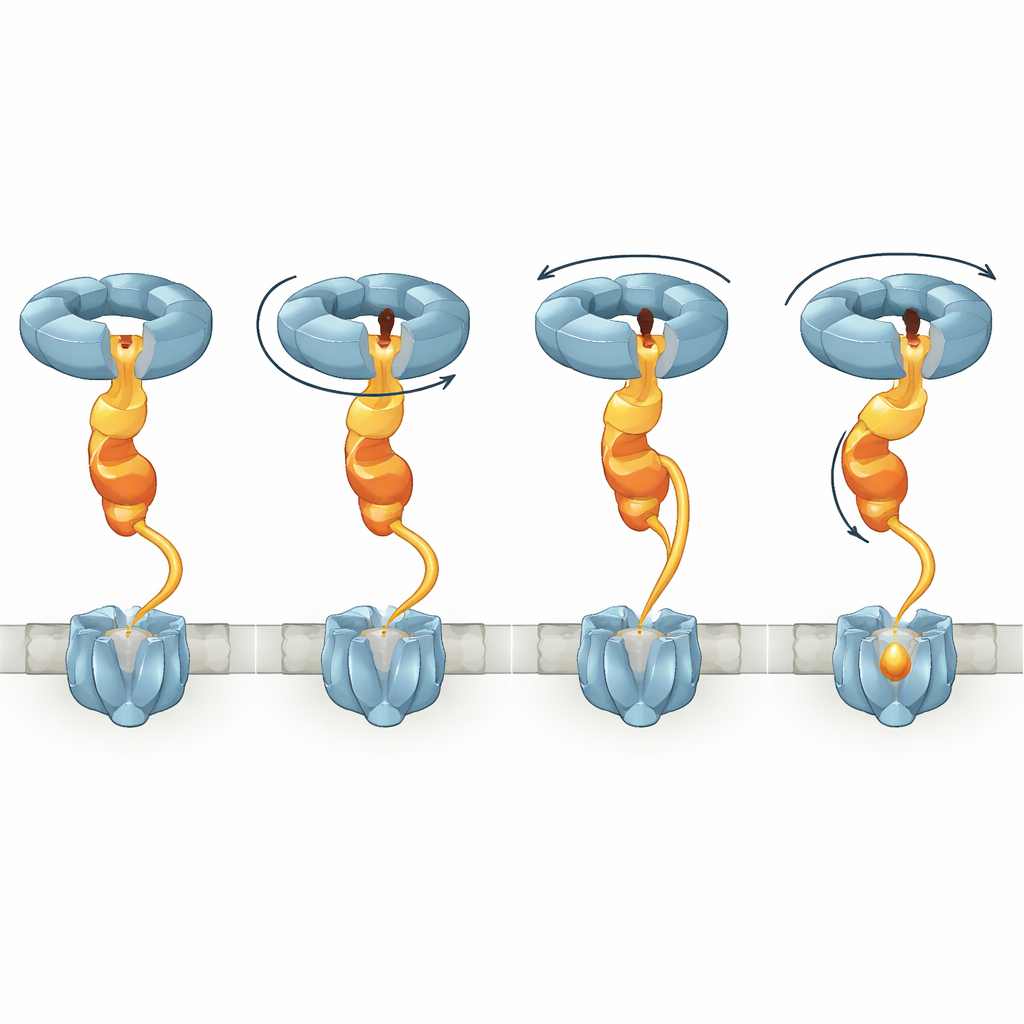
Door verschillende structurele toestanden te vergelijken, toont de studie aan dat wanneer NorD bindt, de NorQ‑ring van een relatief vlakke vorm naar een spiraaltrap verandert. Verschillende subeenheden houden ATP of de uitgeputte vorm ADP vast, en naarmate ATP‑binding en hydrolyse vorderen, stapt de actieve subeenheid onderaan de spiraal omhoog, in overeenstemming met een bekend hand‑over‑hand mechanisme. Omdat de vinger van NorD in de porie geklemd zit terwijl zijn staart is verankerd aan een specifieke lus, roteren en trekken deze veranderingen aan het hele VWA‑domein. NorD bevat ook een lange, voorheen raadselachtige schakel die zijn VWA‑domein verbindt met een N‑terminaal domein dat waarschijnlijk contact maakt met cNOR. De auteurs observeren meerdere conformaties waarin deze schakel verschillende afstanden moet overbruggen, wat impliceert dat hij progressief kan worden uitgerekt. Wanneer ze delen van deze schakel verwijderden, verloor cNOR volledig zijn niet‑heme ijzer en activiteit, hoewel het chaperoncomplex nog steeds kon vormen, wat benadrukt dat gecontroleerd uitrekken van dit gebied centraal is voor de herstructureringstaak.
Van roterende beweging naar metaalinzet
Door de structurele momentopnamen te verbinden, stellen de auteurs een model voor waarin NorQ zich gedraagt als een moleculaire lier die via NorD werkt. In de eerste stap associeert de NorQ‑ring met NorD via de vinger‑in‑pore en staart‑naar‑lus contactpunten, waardoor zijn ATPase‑activiteit stijgt en het VWA‑domein op zijn plaats wordt vergrendeld. Vervolgens pakt NorD cNOR op twee “grijppunten”: één met zijn N‑terminale domein en het andere met het VWA‑gebied of de schakel nabij een metaalbindend motief. Terwijl NorQ cycli door ATP‑binding en hydrolyse, klimmen opeenvolgende subeenheden de spiraal op en slepen de NorD‑vinger rond in de porie. Deze beweging draait het VWA‑domein ten opzichte van de N‑terminale greep en trekt de schakel strak, waardoor koppel en spanning naar cNOR worden overgebracht. De resulterende vervorming zou een anders afgeschermd gebied van cNOR openen, waardoor een ijzerion in de FeB‑plaats kan worden ingebracht, waarna het complex kan loslaten en resetten.
Waarom dit belangrijk is buiten één bacterieel enzym
Voor niet‑specialisten komt het erop neer dat het NorQ–NorD‑paar fungeert als een nanoschaal pijpsleutel, die een enzym op twee punten vastgrijpt en het net genoeg draait om een ijzeratoom op zijn plaats te schuiven. Dit werk verduidelijkt niet alleen hoe een sleutelstap in de bacteriële stikstofchemie verloopt, maar onthult ook een algemeen “vinger‑in‑pore”‑strategie die vergelijkbare motor–partner systemen mogelijk elders in de biologie gebruiken. Door te tonen hoe chemische brandstof wordt omgezet in een preciese draaiende kracht op een doelwit‑eiwit, biedt de studie een blauwdruk om te begrijpen — en misschien op een dag te ontwerpen — machines die bepalen waar en wanneer metalen in complexe moleculaire apparaten worden ingebouwd.
Bronvermelding: Kahle, M., Appelgren, S., König, F. et al. NorQD AAA+ complex drives metal insertion by a twisting mechanism. Nat Commun 17, 3032 (2026). https://doi.org/10.1038/s41467-026-71044-4
Trefwoorden: AAA+ ATPase, metallochaperon, nitric oxide reductase, cryo-EM structuur, inzet van metaalcofactor