Clear Sky Science · de
NorQD‑AAA+-Komplex treibt Metall‑Einbau durch einen Drehmechanismus an
Wie Zellen Metalle in wichtige Enzyme einführen
Viele der Proteine, die Mikroben – und letztlich ganze Ökosysteme – am Laufen halten, müssen winzige Metallionen an genau der richtigen Stelle tragen, um zu funktionieren. Diese Studie zeigt, wie eine spezialisierte Helfermaschine, bestehend aus zwei Proteinen namens NorQ und NorD, ein anderes Enzym physikalisch verdreht und dehnt, sodass ein Eisenatom eingebaut werden kann. Das Verständnis dieser mikroskopischen Choreographie erklärt, wie Bakterien die Treibhausgaschemie im Boden steuern, und könnte Ideen liefern, um metallhaltige Katalysatoren gezielt zu beeinflussen.
Das Problem: Metalle an die richtige Stelle bringen
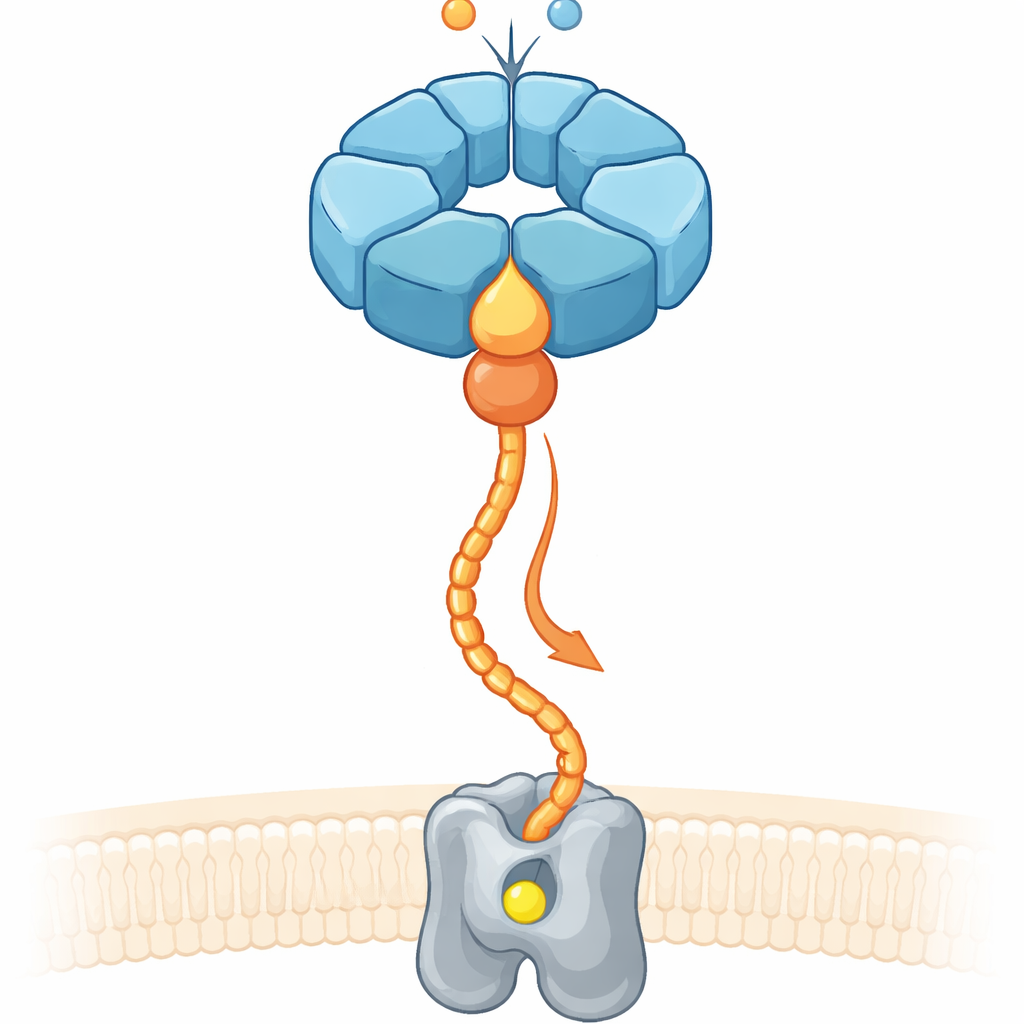
Ungefähr ein Drittel aller bekannten Proteine benötigt Metalle wie Eisen oder Magnesium, um zu funktionieren. Allein das Überschwemmen einer Zelle mit Metallionen garantiert jedoch nicht, dass das richtige Metall in die passende Tasche gelangt. Zellen verlassen sich daher auf „Chaperon“-Systeme, die an unfertige Enzyme binden, diese umformen und Metallionen in ihre aktiven Zentren leiten. In denitrifizierenden Bodenbakterien, die Stickstoffverbindungen umwandeln und N2O‑Emissionen beeinflussen, benötigt ein Membranenzym, die nitric oxide reductase (cNOR), ein nicht‑hämbasiertes Eisenatom (genannt FeB), um aktiv zu werden. Frühere Arbeiten zeigten, dass zwei Zusatzproteine, NorQ und NorD, für das Einsetzen dieses Eisens unerlässlich sind, doch wie sie zusammenarbeiteten und chemische Energie in mechanische Arbeit umsetzten, blieb unklar.
Ein molekularer Ring und sein Helferpartner
NorQ gehört zu einer großen Familie ringförmiger molekularer Motoren, die dafür bekannt sind, sechsteilige Ringe zu bilden, ATP zu verbrennen und Proteinstränge durch ihre zentralen Poren zu ziehen. NorD trägt eine sogenannte VWA‑Domäne, ein kompaktes Andockmodul, mit dem Proteine oft Partner über metallbasierte Kontaktstellen greifen. Mithilfe hochauflösender Kryo‑Elektronenmikroskopie von NorQ und NorD aus zwei Bakterienarten, zusammen mit biochemischen Tests und modernen Strukturvorhersagen, fanden die Autoren heraus, dass NorQ und NorD an zwei Hauptkontaktpunkten zusammentreffen. Erstens schiebt sich eine fingerartige Projektion der VWA‑Domäne von NorD tief in die zentrale Pore des NorQ‑Rings und liegt an einer Reihe konservierter Schleifen an. Zweitens reicht das Schwanzende von NorD seitlich, um eine Schleife eines NorQ‑Unterunits zu berühren, die kurz hinter einer Schlüsselregion zur ATP‑Erkennung liegt.
Drehen, Dehnen und eine kritische flexible Verbindung
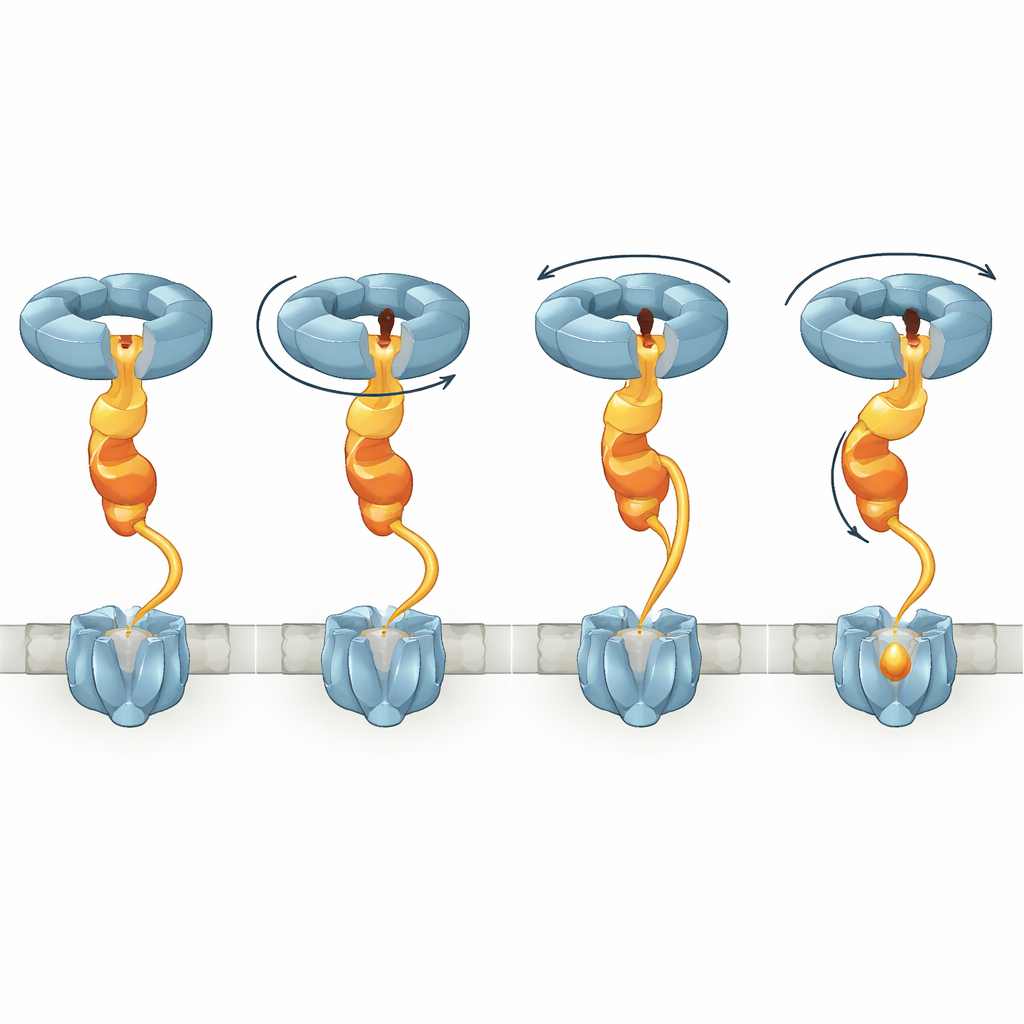
Durch den Vergleich mehrerer Strukturzustände zeigt die Studie, dass der NorQ‑Ring, wenn NorD bindet, von einer relativ flachen Form in eine spiralförmige Treppe übergeht. Verschiedene Untereinheiten halten ATP oder dessen verbrauchte Form ADP, und wenn ATP‑Bindung und ‑Hydrolyse ablaufen, steigt die aktive Untereinheit an der Unterseite der Spirale auf — entsprechend einem bekannten Hand‑über‑Hand‑Mechanismus. Da der NorD‑Finger in der Pore eingespannt ist, während sein Schwanz an einer bestimmten Schleife verankert ist, drehen und ziehen diese Veränderungen die gesamte VWA‑Domäne. NorD enthält außerdem einen langen, zuvor rätselhaften Linker, der seine VWA‑Domäne mit einer N‑terminalen Domäne verbindet, die wahrscheinlich cNOR kontaktiert. Die Autoren beobachten mehrere Konformationen, in denen dieser Linker unterschiedliche Distanzen überbrücken muss, was darauf hindeutet, dass er schrittweise gedehnt werden kann. Als sie Teile dieses Linkers entfernten, verlor cNOR vollständig sein nicht‑hämbasiertes Eisen und seine Aktivität, obwohl der Chaperon‑Komplex weiterhin gebildet werden konnte. Das unterstreicht, dass die kontrollierte Dehnung dieses Bereichs zentral für die Umformungsarbeit ist.
Von rotierender Bewegung zum Metalleinbau
Aus den strukturellen Momentaufnahmen entwickeln die Autoren ein Modell, wonach NorQ wie eine molekulare Winde wirkt, die über NorD ansetzt. Zunächst assoziiert der NorQ‑Ring mit NorD über die Finger‑in‑Pore‑ und Schwanz‑zu‑Schleife‑Kontaktstellen, was die ATPase‑Aktivität erhöht und die VWA‑Domäne verriegelt. Anschließend greift NorD cNOR an zwei „Greifpunkten“: einem über die N‑terminale Domäne und einem weiteren über die VWA‑Region oder den Linker in der Nähe eines Metallbindemotivs. Während NorQ den Zyklus aus ATP‑Bindung und ‑Hydrolyse durchläuft, klettern nacheinander Untereinheiten die Spirale hinauf und ziehen den NorD‑Finger in der Pore mit. Diese Bewegung verdreht die VWA‑Domäne relativ zum N‑terminalen Griff und spannt den Linker, wodurch Torsion und Spannung auf cNOR übertragen werden. Die resultierende Verzerrung soll eine sonst abgeschirmte Region von cNOR öffnen, sodass ein Eisenion in die FeB‑Stelle eingesetzt werden kann, wonach sich der Komplex lösen und zurücksetzen kann.
Warum das über ein einzelnes bakterielles Enzym hinaus relevant ist
Für Nicht‑Spezialisten lautet das Fazit: Das NorQ–NorD‑Paar wirkt wie ein nanoskaliger Rohrzangenschlüssel, der ein Enzym an zwei Punkten greift und es so weit verdreht, dass ein Eisenatom eingeschoben werden kann. Diese Arbeit klärt nicht nur einen Schlüsselschritt der bakteriellen Stickstoffchemie, sondern zeigt auch eine allgemeine „Finger‑in‑Pore“-Strategie, die ähnliche Motor‑Partner‑Systeme in der Biologie verwenden könnten. Indem sie zeigt, wie chemischer Brennstoff in eine präzise Drehkraft auf ein Zielprotein umgewandelt wird, liefert die Studie eine Blaupause dafür, wie Maschinen verstanden — und vielleicht eines Tages entworfen — werden können, die kontrollieren, wo und wann Metalle in komplexe molekulare Bauteile eingebaut werden.
Zitation: Kahle, M., Appelgren, S., König, F. et al. NorQD AAA+ complex drives metal insertion by a twisting mechanism. Nat Commun 17, 3032 (2026). https://doi.org/10.1038/s41467-026-71044-4
Schlüsselwörter: AAA+ ATPase, Metallochaperon, nitric oxide reductase, cryo‑EM‑Struktur, Einbau von Metall‑Cofaktoren