Clear Sky Science · it
Il complesso NorQD AAA+ guida l’inserimento del metallo mediante un meccanismo di torsione
Come le cellule inseriscono i metalli negli enzimi chiave
Molte delle proteine che mantengono in funzione i microbi – e in ultima analisi gli ecosistemi – devono ospitare minuscoli ioni metallici nel posto giusto per funzionare. Questo studio rivela come una macchina aiutante specializzata, composta da due proteine chiamate NorQ e NorD, torca e allunghi fisicamente un altro enzima affinché un atomo di ferro possa essere collocato al suo posto. Comprendere questa coreografia microscopica aiuta a spiegare come i batteri controllano la chimica dei gas serra nei suoli e potrebbe ispirare nuovi modi per regolare catalizzatori contenenti metalli.
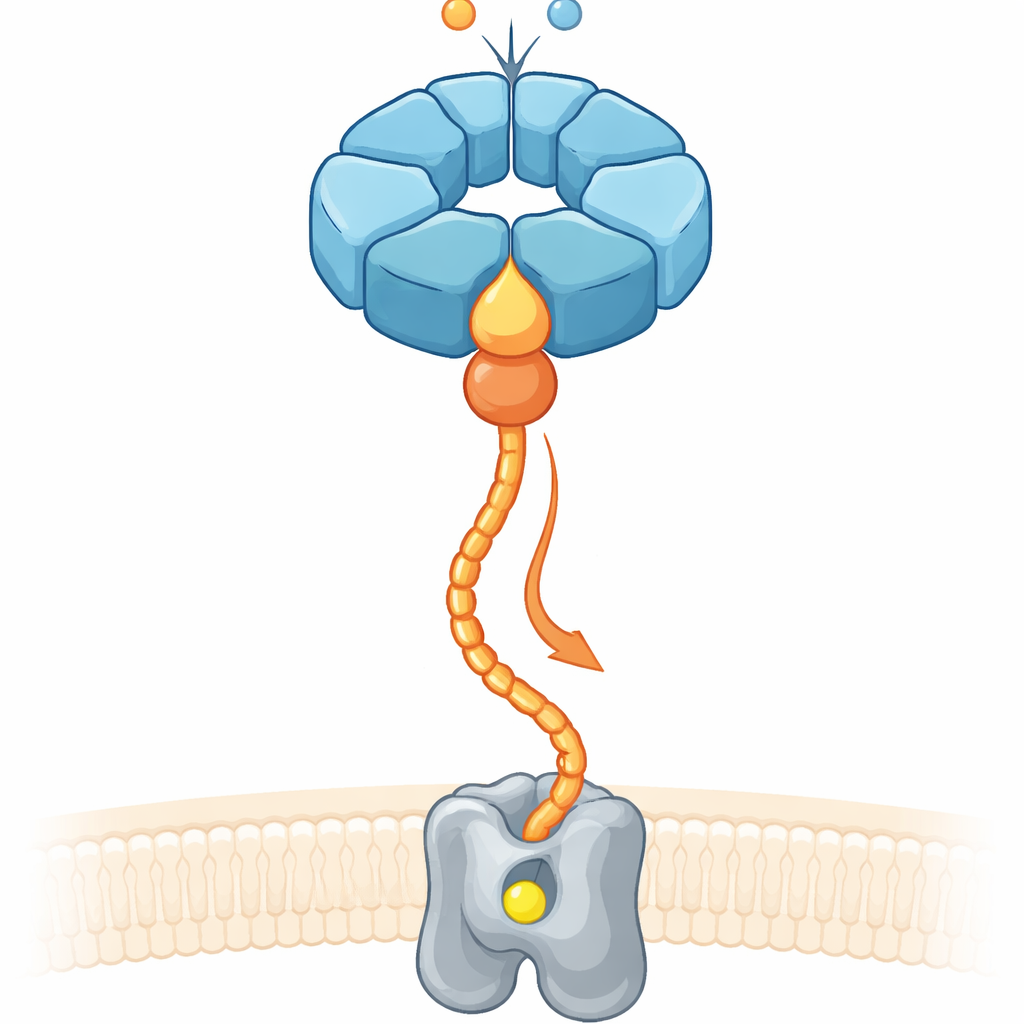
Il problema di mettere i metalli nel posto giusto
All’incirca un terzo di tutte le proteine conosciute necessita di metalli come il ferro o il magnesio per funzionare. Tuttavia, semplicemente inondare una cellula di ioni metallici non garantisce che il metallo corretto finisca nella tasca giusta. Le cellule si affidano quindi a sistemi “chaperone” che si legano agli enzimi non ancora completi, li rimodellano e guidano gli ioni metallici nei loro siti attivi. Nei batteri denitrificanti del suolo, che trasformano composti dell’azoto e influenzano le emissioni di ossido nitroso, un enzima di membrana chiamato nitric oxide reductase (cNOR) richiede un atomo di ferro non eme (chiamato FeB) per diventare attivo. Studi precedenti avevano mostrato che due proteine accessorie, NorQ e NorD, sono essenziali per l’installazione di questo ferro, ma restava poco chiaro come cooperassero e come utilizzassero energia chimica per compiere lavoro meccanico.
Un anello molecolare e il suo partner aiutante
NorQ appartiene a una grande famiglia di motori molecolari ad anello, noti per formare anelli a sei subunità che consumano la molecola ricca di energia ATP e tirano catene proteiche fatte passare attraverso i loro pori centrali. NorD possiede un cosiddetto dominio VWA, un modulo compatto di aggancio spesso usato dalle proteine per afferrare altri partner tramite un sito di contatto mediato da metallo. Utilizzando microscopia crioelettronica ad alta risoluzione su NorQ e NorD di due specie batteriche, insieme a test biochimici e predizioni strutturali moderne, gli autori hanno trovato che NorQ e NorD si incontrano in due punti di contatto principali. Primo, una proiezione a dito dal dominio VWA di NorD si inserisce profondamente nel poro centrale dell’anello di NorQ, adagiandosi contro un insieme di loop conservati. Secondo, l’estremità della coda di NorD raggiunge lateralmente per toccare un loop di una subunità di NorQ che si trova appena oltre una regione sensore chiave per l’ATP.
Torsione, allungamento e un collegamento flessibile critico
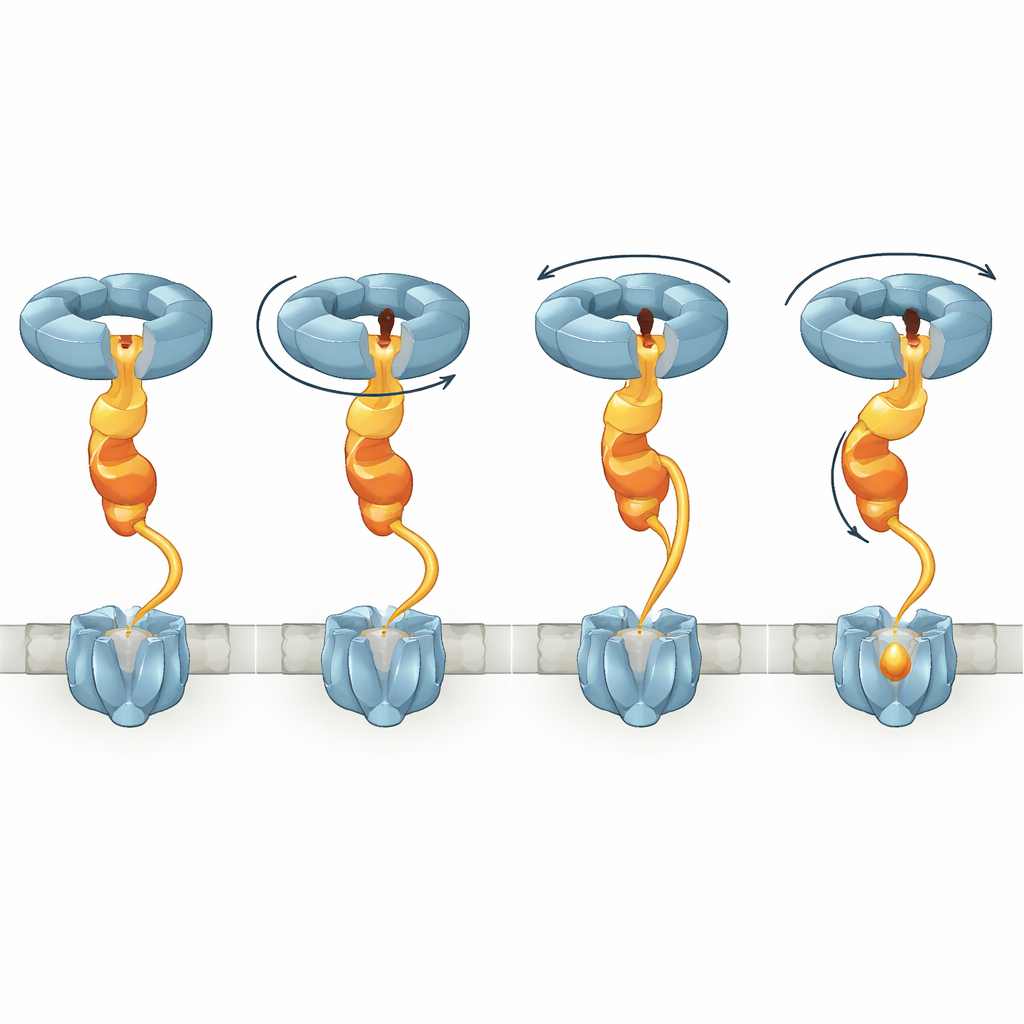
Confrontando diversi stati strutturali, lo studio mostra che quando NorD si lega, l’anello di NorQ passa da una forma relativamente piatta a una scala a chiocciola a gradini. Diverse subunità contengono ATP o la sua forma spenta, ADP, e man mano che il legame e l’idrolisi dell’ATP procedono, la subunità attiva in fondo alla spirale si solleva, in linea con un meccanismo noto come hand-over-hand. Poiché il dito di NorD è bloccato all’interno del poro mentre la sua coda è ancorata a un loop specifico, questi cambiamenti ruotano e tirano l’intero dominio VWA. NorD contiene anche un lungo collegamento, in precedenza misterioso, che connette il dominio VWA a un dominio N-terminale che probabilmente entra in contatto con cNOR. Gli autori osservano più conformazioni in cui questo collegamento deve coprire distanze diverse, implicando che può essere progressivamente esteso. Quando hanno eliminato parti di questo collegamento, cNOR ha perso completamente il suo ferro non eme e la sua attività, anche se il complesso chaperone poteva ancora formarsi, sottolineando che l’allungamento controllato di questa regione è centrale per il lavoro di rimodellamento.
Dal moto rotatorio all’inserimento del metallo
Collegando gli istantanee strutturali, gli autori propongono un modello in cui NorQ si comporta come una verricello molecolare che agisce tramite NorD. Nel primo passo, l’anello di NorQ si associa a NorD tramite i contatti dito‑nel‑poro e coda‑su‑loop, aumentando la sua attività ATPasica e bloccando il dominio VWA in posizione. Successivamente, NorD ingaggia cNOR in due “punti di presa”: uno che coinvolge il suo dominio N-terminale e l’altro che coinvolge la regione VWA o il collegamento vicino a un motivo di legame per il metallo. Mentre NorQ cicla attraverso il legame e l’idrolisi dell’ATP, subunità successive salgono la spirale, trascinando il dito di NorD in giro all’interno del poro. Questo moto torce il dominio VWA rispetto alla presa N-terminale e tende il collegamento, trasmettendo coppia e tensione a cNOR. La distorsione risultante è proposta aprire una regione altrimenti schermata di cNOR, permettendo a un ion ferro di essere inserito nel sito FeB, dopo di che il complesso può rilasciarsi e resettarsi.
Perché questo conta oltre un singolo enzima batterico
Per un non specialista, il risultato principale è che la coppia NorQ–NorD agisce come una chiave inglese a scala nanometrica, afferrando un enzima in due punti e torcendolo giusto quanto necessario per far scivolare un atomo di ferro al suo posto. Questo lavoro non solo chiarisce come avvenga un passaggio chiave nella chimica dell’azoto batterico, ma svela anche una strategia generale “dito‑nel‑poro” che sistemi motore‑partner simili potrebbero usare in tutta la biologia. Mostrando come il carburante chimico venga convertito in una forza di torsione precisa su una proteina bersaglio, lo studio offre un modello per comprendere – e forse un giorno progettare – macchine che controllano dove e quando i metalli vengono incorporati in dispositivi molecolari complessi.
Citazione: Kahle, M., Appelgren, S., König, F. et al. NorQD AAA+ complex drives metal insertion by a twisting mechanism. Nat Commun 17, 3032 (2026). https://doi.org/10.1038/s41467-026-71044-4
Parole chiave: ATPasi AAA+, metallocarica, nitric oxide reductase, struttura cryo-EM, inserimento del cofattore metallico