Clear Sky Science · pt
Complexo NorQD AAA+ dirige inserção de metal por um mecanismo de torção
Como as Células Encaixam Metais em Enzimas-Chave
Muitas das proteínas que mantêm micróbios — e, em última instância, ecossistemas — funcionando precisam carregar íons metálicos minúsculos exatamente no lugar certo para atuar. Este estudo revela como uma máquina auxiliar especializada, formada por duas proteínas chamadas NorQ e NorD, torce e estica fisicamente outra enzima para que um átomo de ferro possa ser encaixado. Entender essa coreografia microscópica ajuda a explicar como bactérias controlam a química dos gases de efeito estufa no solo e pode inspirar novas maneiras de ajustar catalisadores que contêm metais.
O Problema de Colocar Metais no Lugar Certo
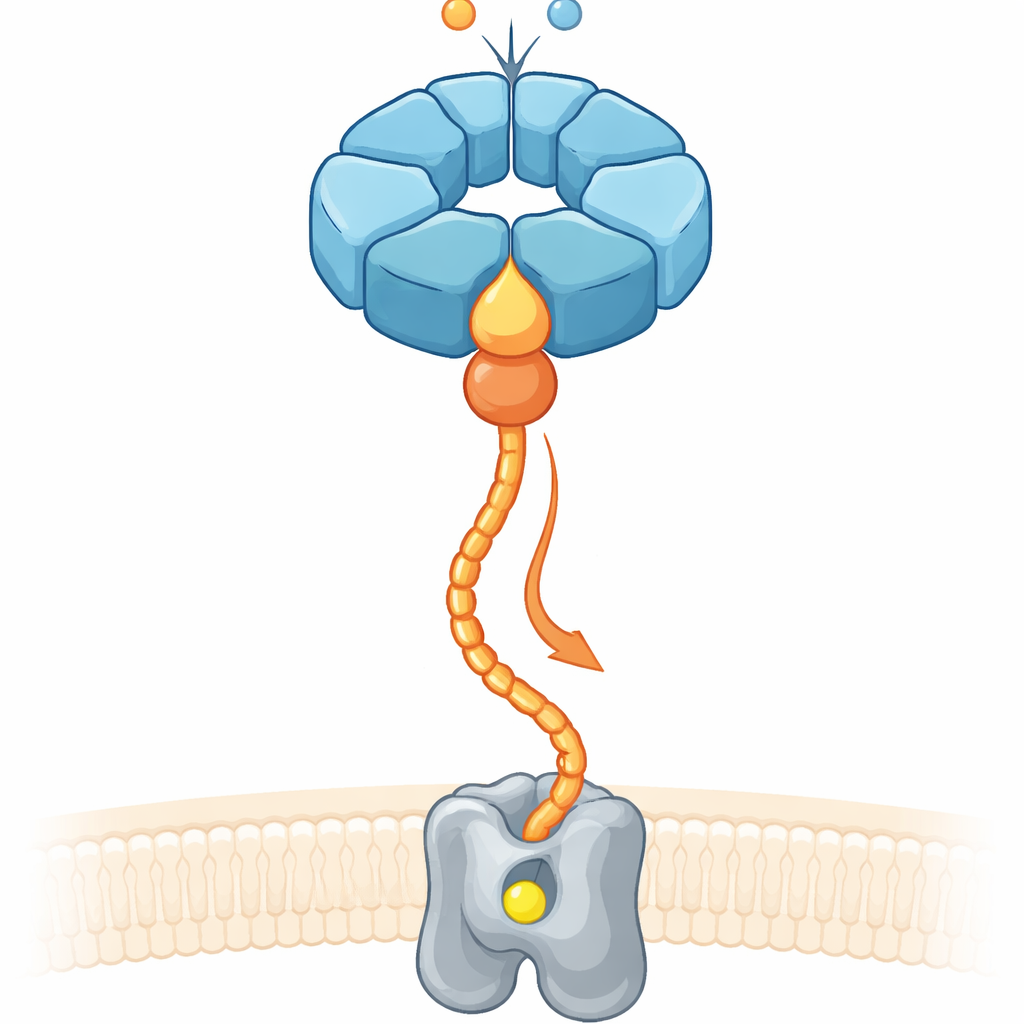
Cerca de um terço de todas as proteínas conhecidas precisam de metais como ferro ou magnésio para funcionar. Ainda assim, simplesmente inundar uma célula com íons metálicos não garante que o metal correto vá ao encaixe certo. As células, portanto, dependem de sistemas “chaperona” que se ligam a enzimas em maturação, as remodelam e guiam os íons metálicos até seus sítios ativos. Em bactérias desnitrificantes do solo, que transformam compostos de nitrogênio e influenciam as emissões de óxido nitroso, uma enzima de membrana chamada redutase de óxido nítrico (cNOR) requer um átomo de ferro não‑heme (chamado FeB) para ficar ativa. Trabalhos anteriores mostraram que duas proteínas acessórias, NorQ e NorD, são essenciais para instalar esse ferro, mas como elas cooperavam e usavam energia química para realizar trabalho mecânico permanecia obscuro.
Um Anel Molecular e Seu Parceiro Auxiliar
NorQ pertence a uma grande família de motores moleculares em forma de anel, conhecidos por formar anéis de seis subunidades que queimam a molécula energética ATP e puxam cadeias proteicas atravessadas por seus poros centrais. NorD carrega um chamado domínio VWA, um módulo compacto de encaixe frequentemente usado por proteínas para agarrar parceiros via um sítio de contato mediado por metal. Usando crio‑microscopia eletrônica em alta resolução nas proteínas NorQ e NorD de duas espécies bacterianas, juntamente com testes bioquímicos e predição estrutural moderna, os autores descobriram que NorQ e NorD se encontram em dois pontos de contato principais. Primeiro, uma projeção em forma de dedo do domínio VWA de NorD insere‑se profundamente no poro central do anel de NorQ, aninhando‑se contra um conjunto de alças conservadas. Em segundo lugar, a extremidade da cauda de NorD alcança lateralmente para tocar uma alça em uma subunidade de NorQ que fica logo após uma região sensora chave para ATP.
Torção, Alongamento e um Elo Flexível Crítico
Ao comparar vários estados estruturais, o estudo mostra que quando NorD se liga, o anel de NorQ muda de uma forma relativamente plana para uma escada em espiral. Diferentes subunidades contêm ATP ou sua forma gasta, ADP, e à medida que a ligação e a hidrólise do ATP prosseguem, a subunidade ativa na base da espiral sobe, conforme um mecanismo conhecido de “mão sobre mão”. Porque o dedo de NorD está preso dentro do poro enquanto sua cauda está ancorada a uma alça específica, essas mudanças rotacionam e puxam todo o domínio VWA. NorD também contém um longo conector, até então enigmático, que liga seu domínio VWA a um domínio N‑terminal que provavelmente faz contato com a cNOR. Os autores observam múltiplas conformações nas quais esse conector precisa cobrir diferentes distâncias, o que implica que ele pode ser progressivamente esticado. Quando deletaram partes desse conector, a cNOR perdeu completamente seu ferro não‑heme e atividade, embora o complexo chaperona ainda pudesse se formar, destacando que o alongamento controlado dessa região é central para a tarefa de remodelação.
Do Movimento Rotativo à Inserção do Metal
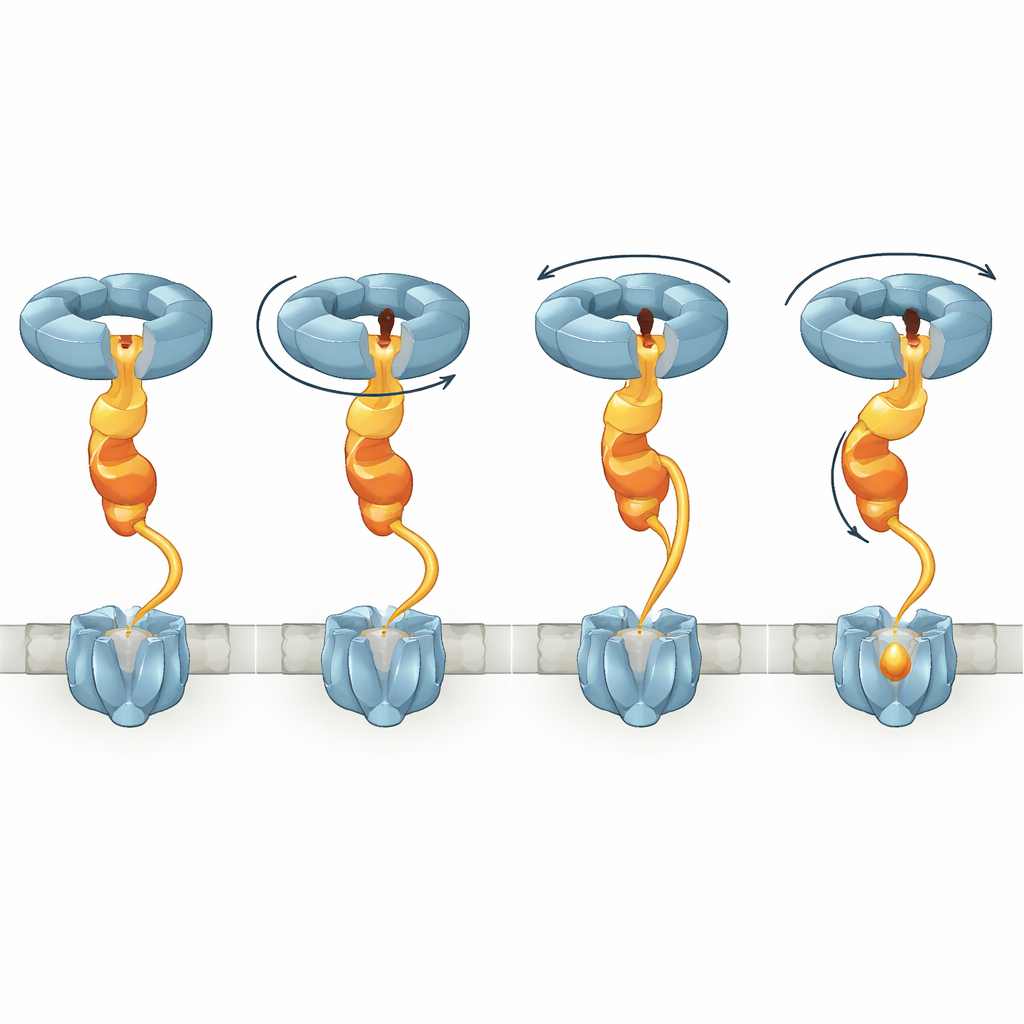
Amarrando os instantâneos estruturais, os autores propõem um modelo em que NorQ se comporta como um guincho molecular atuando por meio de NorD. No primeiro passo, o anel NorQ associa‑se a NorD via os contatos dedo‑no‑poro e cauda‑à‑alça, aumentando sua atividade ATPase e travando o domínio VWA na posição. Em seguida, NorD interage com a cNOR em dois “pontos de apreensão”: um envolvendo seu domínio N‑terminal e o outro envolvendo a região VWA ou o conector próximo a um motivo de ligação de metal. À medida que NorQ percorre ciclos de ligação e hidrólise de ATP, subunidades sucessivas sobem pela espiral, arrastando o dedo de NorD ao redor dentro do poro. Esse movimento torce o domínio VWA em relação à apreensão N‑terminal e estica o conector, transmitindo torque e tensão para a cNOR. A distorção resultante é proposta para abrir uma região normalmente protegida da cNOR, permitindo que um íon de ferro seja inserido no sítio FeB, após o qual o complexo pode se soltar e resetar.
Por Que Isso Importa Além de Uma Enzima Bacteriana
Para um não‑especialista, a conclusão é que o par NorQ–NorD age como um grifo em escala nanométrica, agarrando uma enzima em dois pontos e torcendo‑a o suficiente para encaixar um átomo de ferro. Este trabalho não apenas esclarece como ocorre uma etapa chave na química do nitrogênio bacteriano, mas também revela uma estratégia geral de “dedo‑no‑poro” que sistemas motor–parceiro semelhantes podem usar na biologia. Ao mostrar como combustível químico é convertido em uma força de torção precisa sobre uma proteína alvo, o estudo oferece um roteiro para entender — e talvez um dia projetar — máquinas que controlam onde e quando metais são incorporados em dispositivos moleculares complexos.
Citação: Kahle, M., Appelgren, S., König, F. et al. NorQD AAA+ complex drives metal insertion by a twisting mechanism. Nat Commun 17, 3032 (2026). https://doi.org/10.1038/s41467-026-71044-4
Palavras-chave: AAA+ ATPase, metalochaperona, redutase de óxido nítrico, estrutura por crio‑EM, inserção de cofator metálico