Clear Sky Science · ru
Комплекс NorQD AAA+ обеспечивает вставку металла посредством закручивающего механизма
Как клетки проталкивают металлы в ключевые ферменты
Многие белки, которые поддерживают работу микробов — а в конечном счёте и экосистем — должны иметь в определённой точке крошечный ион металла, чтобы функционировать. В этом исследовании раскрывается, как специализированный вспомогательный механизм, состоящий из двух белков — NorQ и NorD, физически скручивает и растягивает другой фермент, чтобы туда можно было установить атом железа. Понимание этой микроскопической хореографии помогает объяснить, как бактерии контролируют газовые процессы в почвах, влияющие на климат, и может вдохновить новые подходы к настройке металло-содержащих катализаторов.
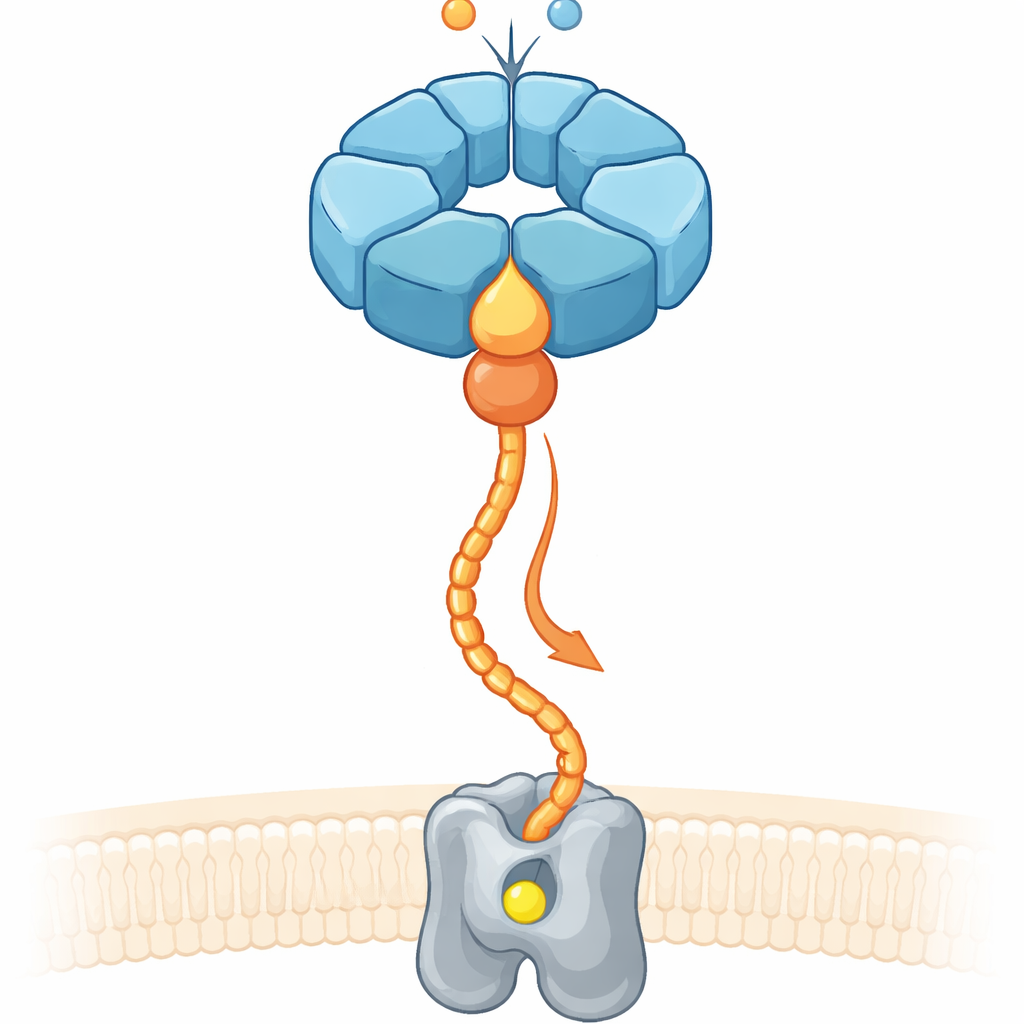
Проблема размещения металлов в нужном месте
Примерно треть известных белков нуждается в металлах, таких как железо или магний, чтобы функционировать. Однако простое насыщение клетки ионами металла не гарантирует, что нужный металл попадёт в нужный карман. Поэтому клетки полагаются на «чейперонные» системы, которые связываются с недооформленными ферментами, перестраивают их и направляют ионы металлов в их активные центры. У денитрифицирующих почвенных бактерий, которые преобразуют азотсодержащие соединения и влияют на выбросы закиси азота, мембранный фермент нитрическая оксид-редуктаза (cNOR) требует не‑гемного атома железа (обозначаемого FeB) для активации. Ранее было показано, что два вспомогательных белка, NorQ и NorD, необходимы для установки этого железа, но оставалось неясным, как они взаимодействуют и используют химическую энергию для выполнения механической работы.
Молекулярное кольцо и его помощник
NorQ принадлежит большой семье кольцеобразных молекулярных моторов, известных тем, что формируют шестисубъединичные кольца, гидролизуют энергичный молекул ATP и тянут белковые цепи, пропуская их через центральное отверстие. NorD содержит так называемый VWA-домен — компактный защёлкивающий модуль, который часто используют белки для захвата партнёров через металло-опосредованную контактную точку. С помощью высокоразрешающей крио-электронной микроскопии NorQ и NorD из двух видов бактерий, в сочетании с биохимическими тестами и современным предсказанием структуры, авторы обнаружили, что NorQ и NorD соединяются в двух основных контактных местах. Во-первых, пальцеобразный выступ VWA-домена NorD глубоко проникает в центральное отверстие кольца NorQ, прилегая к набору консервативных петель. Во-вторых, хвостовой конец NorD тянется вбок и касается петли одной из субъединиц NorQ, расположенной сразу за ключевой сенсорной областью для ATP.
Закручивание, растяжение и критическая гибкая связь
Сравнивая несколько структурных состояний, исследование показывает, что при связывании NorD кольцо NorQ переходит от относительно плоской формы в форму спиральной лестницы. Разные субъединицы содержат ATP или его истощённую форму ADP, и по мере связывания и гидролиза ATP активная субъединица внизу спирали поднимается вверх — в духе известного механизма «рука за рукой». Поскольку «палец» NorD зажат внутри отверстия, а его хвост закреплён за конкретную петлю, эти перемещения вращают и тянут весь VWA-домен. NorD также содержит длинный, ранее неясный линкер, соединяющий его VWA-домен с N‑терминальным доменом, который, вероятно, контактирует с cNOR. Авторы наблюдают несколько конформаций, в которых этот линкер должен покрывать разные расстояния, что указывает на его способность к постепенному растяжению. Когда они удаляли части этого линкера, cNOR полностью терял свой не‑гемный атом железа и активность, хотя чейперонный комплекс всё ещё мог образовываться, подчёркивая, что контролируемое растяжение этой области является ключевым для реструктуризации.
От вращательного движения к вставке металла
Сводя структурные снимки воедино, авторы предлагают модель, в которой NorQ действует как молекулярная лебёдка, действующая через NorD. На первом шаге кольцо NorQ связывается с NorD через контакты «палец-в-отверстии» и «хвост-к-петле», повышая свою ATPазную активность и фиксируя VWA-домен в положении. Затем NorD захватывает cNOR в двух «точках захвата»: одна включает его N‑терминальный домен, другая — VWA‑область или линкер возле мотива, связывающего металл. По мере того как NorQ циклично связывает и гидролизует ATP, последующие субъединицы поднимаются по спирали, протаскивая палец NorD внутри отверстия. Это движение скручивает VWA‑домен относительно N‑терминального захвата и натягивает линкер, передавая крутящий момент и напряжение на cNOR. Получающаяся деформация, как полагают, открывает в противном случае защищённую область cNOR, позволяя иону железа войти в сайт FeB, после чего комплекс может освободиться и вернуться в исходное состояние.
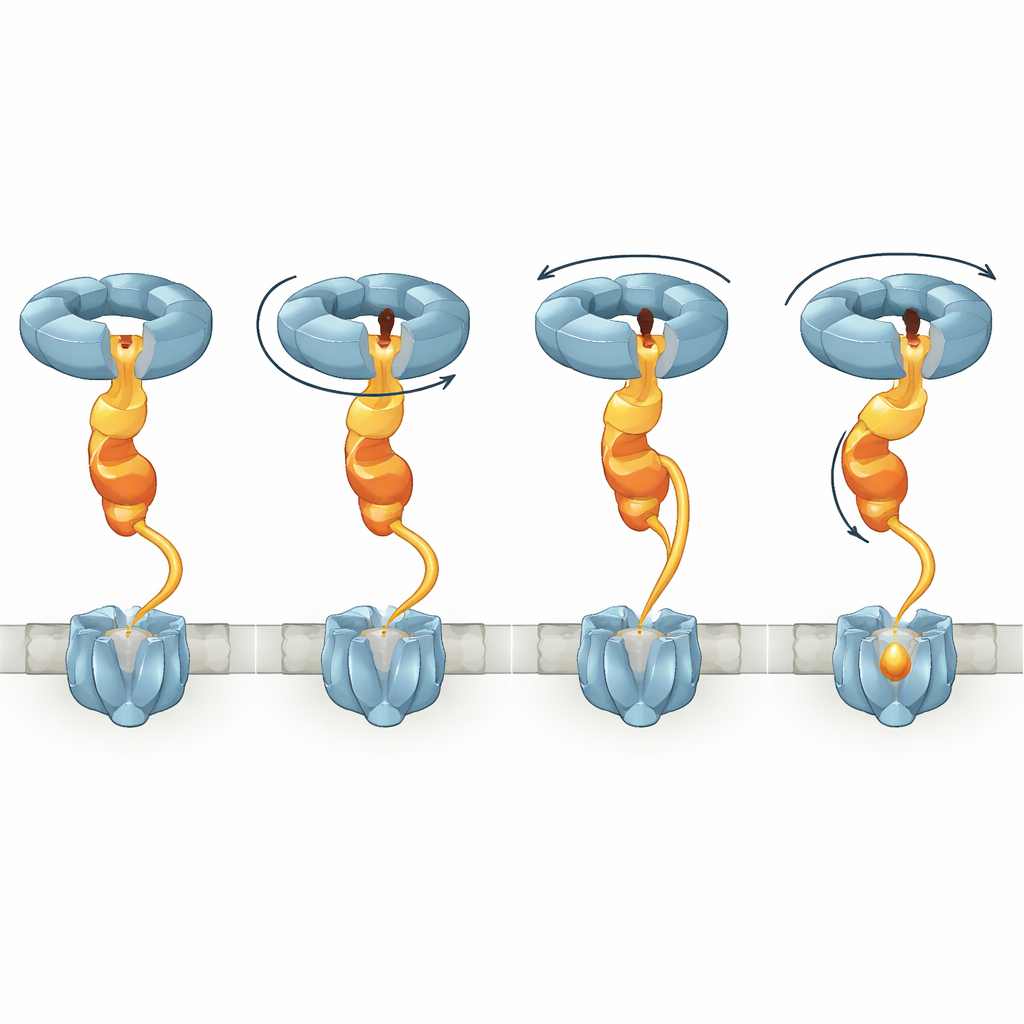
Почему это важно помимо одного бактериального фермента
Для неспециалиста суть в том, что пара NorQ–NorD действует как наноразмерный разводной ключ: захватывает фермент в двух точках и закручивает его ровно настолько, чтобы вставить атом железа. Эта работа не только проясняет ключевой шаг в бактериальной азотной химии, но и выявляет общую стратегию «палец-в-отверстии», которую сходные мотор‑партнёр системы могут использовать по всему живому миру. Показав, как химическое топливо превращается в точную скручивающую силу на целевом белке, исследование предлагает схему для понимания — и, возможно, в будущем для проектирования — машин, контролирующих, где и когда металлы встраиваются в сложные молекулярные устройства.
Цитирование: Kahle, M., Appelgren, S., König, F. et al. NorQD AAA+ complex drives metal insertion by a twisting mechanism. Nat Commun 17, 3032 (2026). https://doi.org/10.1038/s41467-026-71044-4
Ключевые слова: AAA+ ATPase, металлочейперон, нитрический оксид-редуктаза, крио-ЭМ структура, вставка металлического кофактора