Clear Sky Science · sv
NorQD AAA+‑komplex driver metallinsättning genom en vridmekanism
Hur celler träder in metaller i viktiga enzymer
Många av de proteiner som håller mikrober – och i förlängningen ekosystem – igång måste bära små metalljoner på precis rätt plats för att fungera. Denna studie avslöjar hur en specialiserad hjälpmaskin, uppbyggd av två proteiner kallade NorQ och NorD, fysiskt vrider och sträcker ett annat enzym så att en järnatom kan skjutas på plats. Att förstå denna mikroskopiska koreografi hjälper till att förklara hur bakterier styr växthusgaskemi i marken och kan inspirera nya sätt att stämma metallinnehållande katalysatorer.
Problemet med att få metallerna på rätt ställe
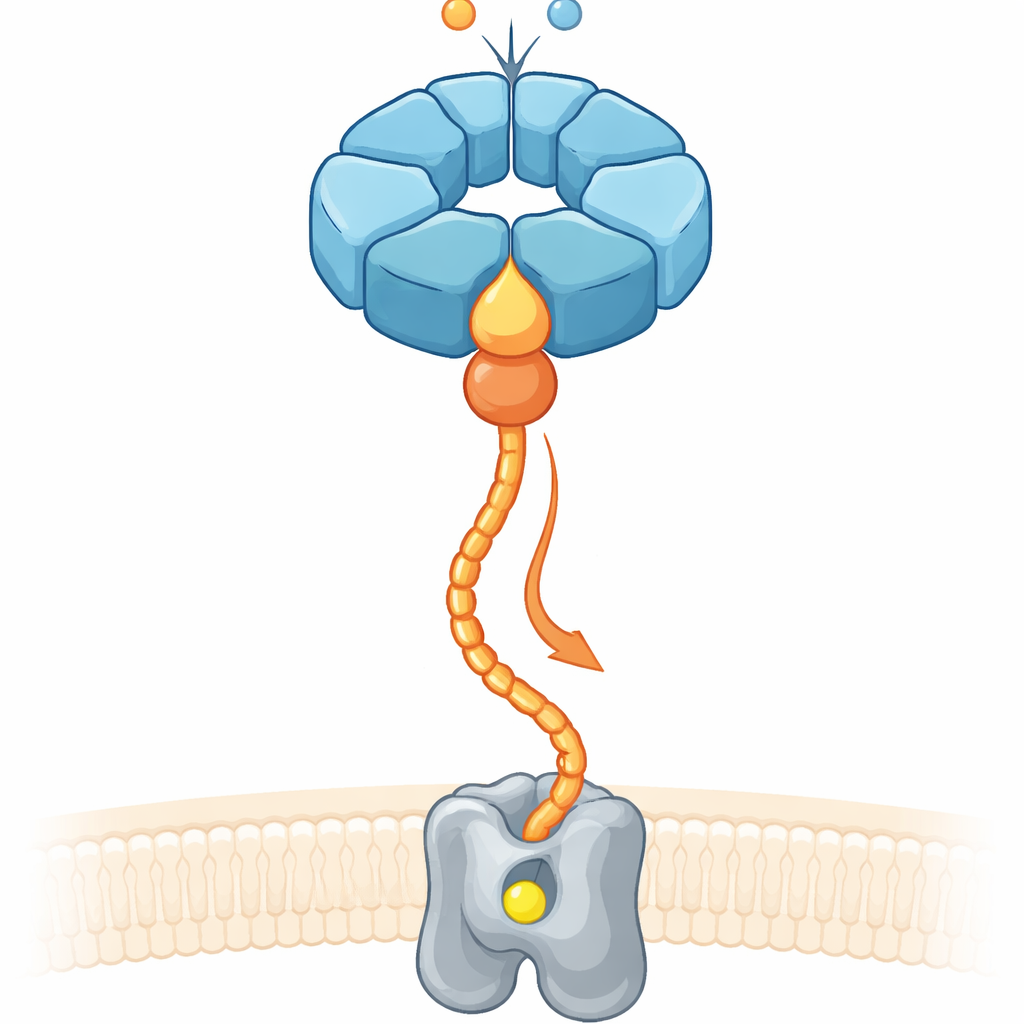
Cirka en tredjedel av alla kända proteiner behöver metaller som järn eller magnesium för att fungera. Att bara översvämma en cell med metalljoner garanterar inte att rätt metall hamnar i rätt ficka. Celler förlitar sig därför på ”chaperon”-system som binder till ofärdiga enzymer, formar om dem och vägleder metalljoner in i deras aktiva säten. I denitrifierande markbakterier, som omvandlar kväveföreningar och påverkar lustgasutsläpp, kräver ett membranbundet enzym kallat nitric oxide reductase (cNOR) en icke‑hem‑järnatom (kallad FeB) för att bli aktivt. Tidigare arbete visade att två accessoriska proteiner, NorQ och NorD, är nödvändiga för att installera detta järn, men hur de samarbetade och använde kemisk energi för att utföra mekaniskt arbete var oklart.
En molekylär ring och dess hjälppartner
NorQ hör till en stor familj av ringformade molekylära motorer, kända för att bilda sexsubenhetsringar som förbrukar energirika ATP‑molekyler och drar i proteinkedjor som träs genom deras centrala porer. NorD bär en så kallad VWA‑domän, en kompakt låsmodul som ofta används av proteiner för att greppa andra partner via en metallbaserad kontaktpunkt. Genom högupplöst kryoelektronmikroskopi på NorQ och NorD från två bakteriearter, tillsammans med biokemiska tester och moderna strukturförutsägelser, fann författarna att NorQ och NorD möts vid två huvudsakliga kontaktpunkter. För det första tränger en fingerlik projektion från NorD:s VWA‑domän djupt in i NorQ‑ringens centrala por och ligger intill en uppsättning konserverade slingor. För det andra når NorD:s svansända åt sidan för att röra vid en slinga på en NorQ‑subenhet som sitter precis förbi en nyckelregion som känner av ATP.
Vridning, töjning och en kritisk flexibel länk
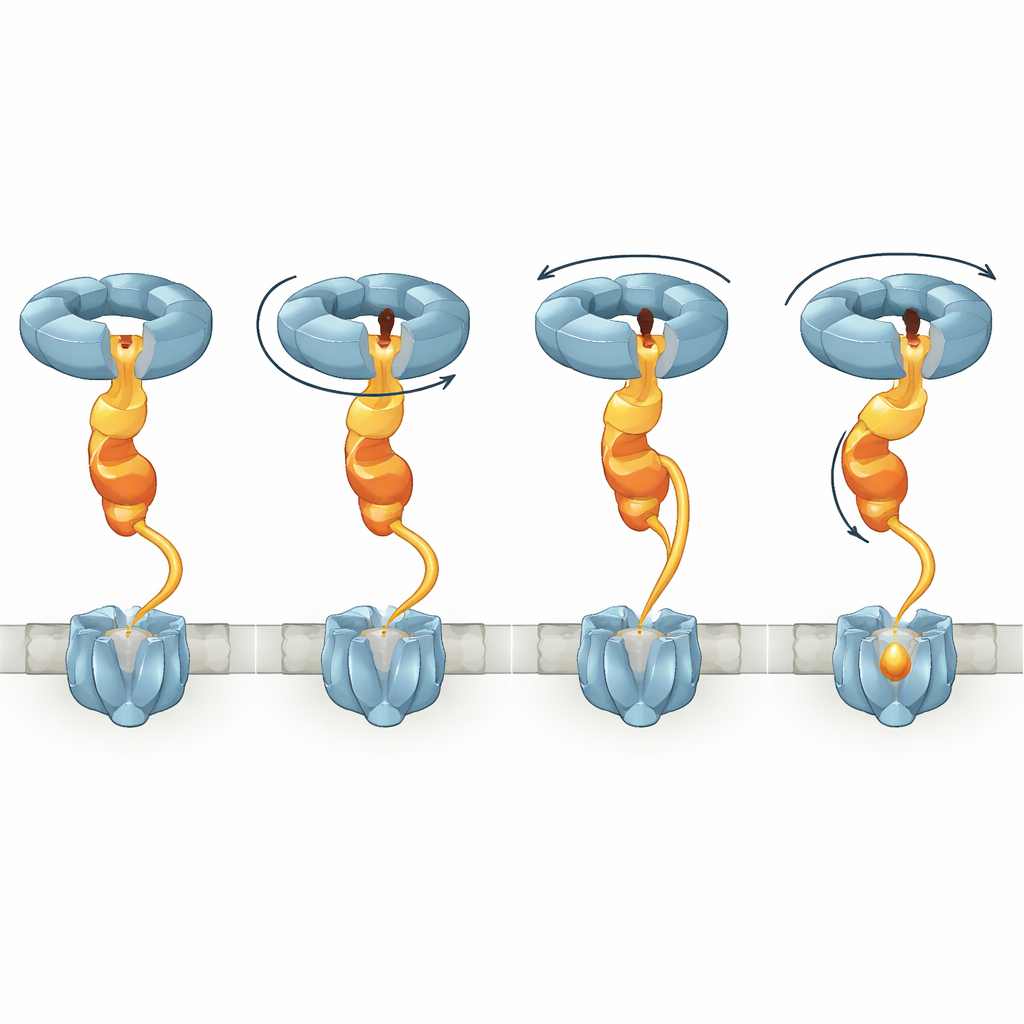
Genom att jämföra flera strukturella tillstånd visar studien att när NorD binder, skiftar NorQ‑ringen från en relativt platt form till en spiraltrappa. Olika subenheter håller ATP eller dess utmattade form, ADP, och när ATP‑bindning och hydrolys fortskrider, kliver den aktiva subenheten längst ner i spiralen uppåt, i linje med en känd hand‑över‑hand‑mekanism. Eftersom NorD:s finger kläms inne i poren medan dess svans är förankrad vid en specifik slinga, roterar och drar dessa förändringar i hela VWA‑domänen. NorD innehåller också en lång, tidigare mystisk länk som förbinder dess VWA‑domän med en N‑terminal domän som sannolikt kontaktar cNOR. Författarna observerar flera konformationer där denna länk måste sträcka över olika avstånd, vilket antyder att den kan töjas gradvis. När de tog bort delar av denna länk förlorade cNOR helt sitt icke‑hem‑järn och sin aktivitet, även om chaperonkomplexet fortfarande kunde bildas, vilket understryker att kontrollerad töjning av detta område är central för omformningsjobbet.
Från roterande rörelse till metallinsättning
Genom att binda samman de strukturella ögonblicksbilderna föreslår författarna en modell där NorQ beter sig som en molekylär vinsch som verkar genom NorD. I ett första steg associerar NorQ‑ringen med NorD via finger‑i‑pore‑ och svans‑till‑slinga‑kontakterna, vilket höjer dess ATPas‑aktivitet och låser VWA‑domänen i position. Därefter engagerar NorD cNOR vid två ”greppunkter”: en som involverar dess N‑terminala domän och den andra som involverar VWA‑regionen eller länken nära ett metallbindande motiv. När NorQ cyklar genom ATP‑bindning och hydrolys klättrar successiva subenheter uppför spiralen och drar NorD‑fingret runt inne i poren. Denna rörelse vrider VWA‑domänen relativt det N‑terminala greppet och spänner länken, vilket överför vridmoment och spänning till cNOR. Den resulterande deformationen antas öppna ett i annat fall skyddat område av cNOR, vilket tillåter att en järnjon sätts in i FeB‑sätet, varefter komplexet kan släppa och återställa sig.
Varför detta är viktigt bortom ett bakterieenzym
För en icke‑specialist är slutsatsen att NorQ–NorD‑paret fungerar som en nanoskala rörtång, som greppar ett enzym på två punkter och vrider det precis så mycket att en järnatom kan glida på plats. Detta arbete klargör inte bara hur ett nyckelsteg i bakteriell kvävkemi sker, utan avslöjar också en generell ”finger‑i‑pore”‑strategi som liknande motor–partner‑system kan använda inom biologin. Genom att visa hur kemiskt bränsle omvandlas till en precis vridkraft på ett målprotein erbjuder studien en ritning för att förstå – och kanske en dag konstruera – maskiner som styr var och när metaller byggs in i komplexa molekylära enheter.
Citering: Kahle, M., Appelgren, S., König, F. et al. NorQD AAA+ complex drives metal insertion by a twisting mechanism. Nat Commun 17, 3032 (2026). https://doi.org/10.1038/s41467-026-71044-4
Nyckelord: AAA+ ATPas, metallokampar, nitric oxide reductase, kryo‑EM‑struktur, insättning av metalldelar