Clear Sky Science · pl
Kompleks NorQD AAA+ wprowadza metal przez mechanizm skręcania
Jak komórki wprowadzają metale do kluczowych enzymów
Wiele białek, które utrzymują mikroorganizmy — a w konsekwencji całe ekosystemy — w działaniu, musi przenosić maleńkie jony metali dokładnie w odpowiednie miejsce, by działać. W tym badaniu odkryto, jak specjalistyczna maszyna pomocnicza, złożona z dwóch białek zwanych NorQ i NorD, fizycznie skręca i rozciąga inny enzym, tak aby atom żelaza mógł zostać umieszczony na swoim miejscu. Zrozumienie tej mikroskopowej choreografii pomaga wyjaśnić, jak bakterie kontrolują chemię gazów cieplarnianych w glebach i może zainspirować nowe sposoby modyfikowania katalizatorów zawierających metale.
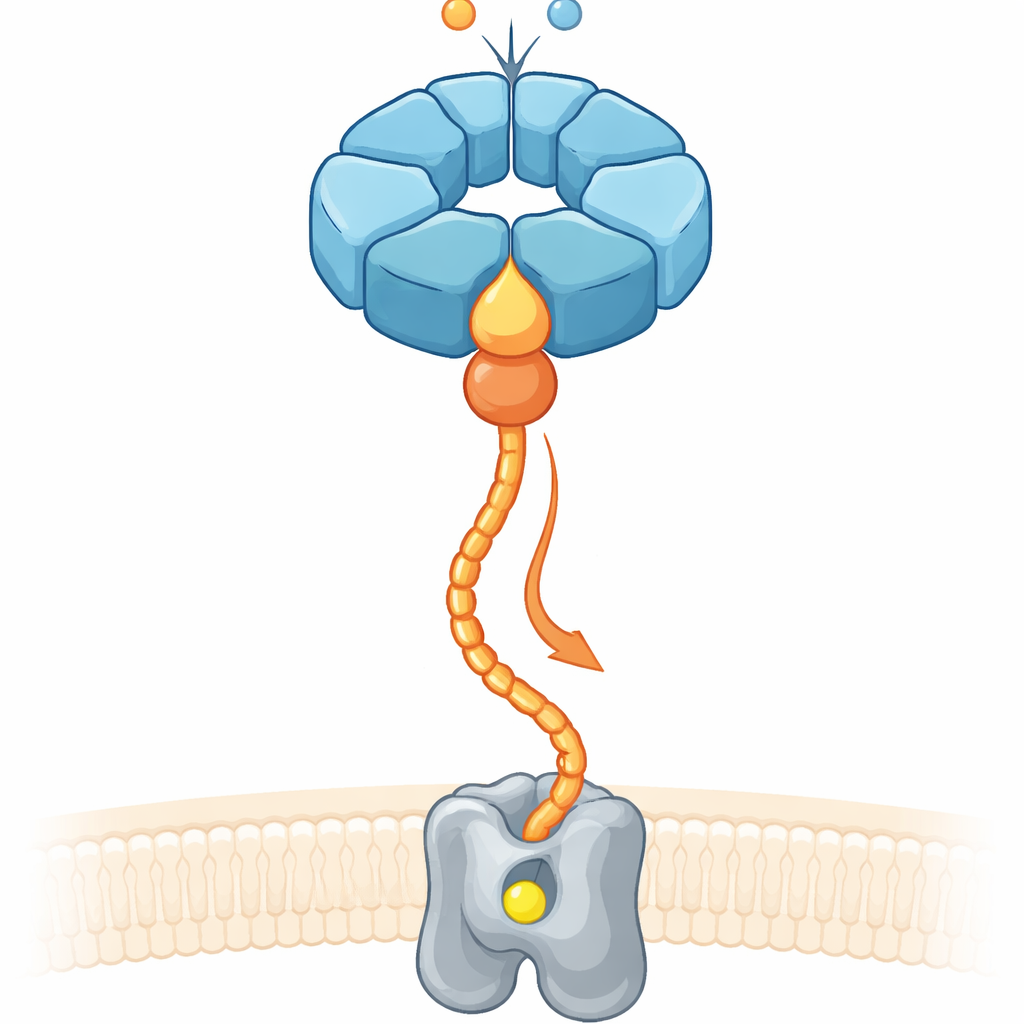
Problem umieszczania metali we właściwym miejscu
Około jedna trzecia znanych białek potrzebuje metali, takich jak żelazo czy magnez, aby funkcjonować. Jednak samo zalanie komórki jonami metali nie gwarantuje, że właściwy metal trafi do właściwej kieszeni. Komórki polegają więc na systemach „chaperonowych”, które wiążą niedokończone enzymy, przekształcają je i prowadzą jony metali do ich miejsc aktywnych. W bakteriach denitryfikujących glebę, które przekształcają związki azotu i wpływają na emisje podtlenku azotu, enzym błonowy zwany reduktazą tlenku azotu (cNOR) wymaga niehemowego atomu żelaza (nazwanego FeB), aby stać się aktywny. Wcześniejsze prace wykazały, że dwa białka pomocnicze, NorQ i NorD, są niezbędne do wkładania tego żelaza, ale to, jak współdziałały i wykorzystywały energię chemiczną do wykonania pracy mechanicznej, pozostawało niejasne.
Pierścień molekularny i jego partner pomocniczy
NorQ należy do dużej rodziny pierścieniowych silników molekularnych, znanych z tworzenia sześciocukłowych pierścieni, które rozkładają wysokoenergetyczną cząsteczkę ATP i przyciągają łańcuchy białkowe przeciągane przez ich centralne pory. NorD zawiera tzw. domenę VWA, zwarty moduł zapadkowy często wykorzystywany przez białka do chwytania partnerów poprzez metalowo zależne miejsce kontaktu. Korzystając z wysokorozdzielczej krio‑elektronowej mikroskopii NorQ i NorD z dwóch gatunków bakterii, wraz z testami biochemicznymi i współczesnym przewidywaniem struktur, autorzy odkryli, że NorQ i NorD stykają się w dwóch głównych punktach kontaktu. Po pierwsze, palcowaty wyrostek domeny VWA NorD wciska się głęboko w centralną porę pierścienia NorQ, opierając się o zestaw konserwowanych pętli. Po drugie, koniec ogonowy NorD sięga bokiem, aby dotknąć pętli jednej podjednostki NorQ, która znajduje się tuż za kluczowym regionem sensorycznym dla ATP.
Skręcanie, rozciąganie i krytyczne elastyczne łącze
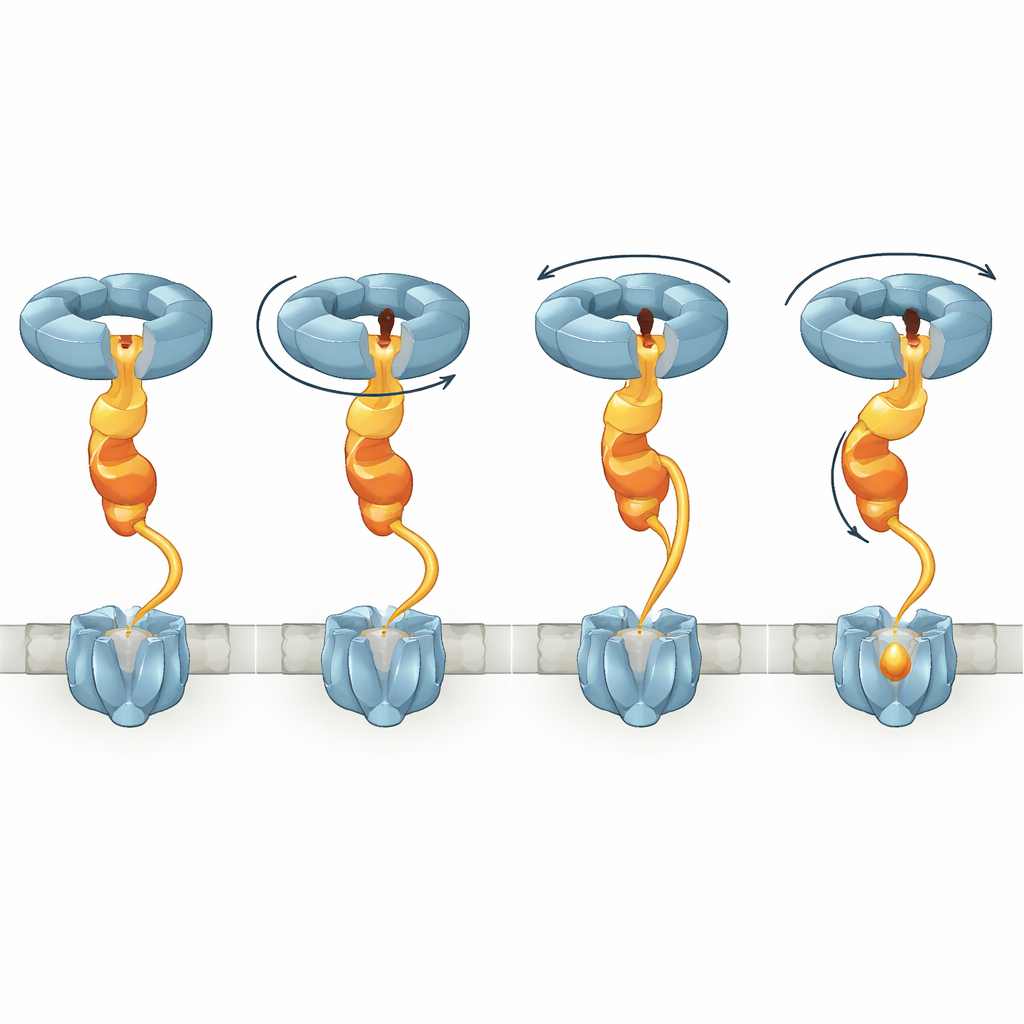
Porównując kilka stanów strukturalnych, badanie pokazuje, że gdy NorD się wiąże, pierścień NorQ przekształca się z relatywnie płaskiego kształtu w spiralne schodki. Różne podjednostki trzymają ATP lub jego zużytą formę, ADP, a wraz z wiązaniem ATP i jego hydrolizą aktywna podjednostka u dołu spirali przesuwa się w górę, zgodnie z znanym mechanizmem „ręka‑nad‑ręką”. Ponieważ palec NorD jest zaciśnięty wewnątrz poru, podczas gdy jego ogon jest zakotwiczony do konkretnej pętli, te zmiany obracają i ciągną całą domenę VWA. NorD zawiera także długi, wcześniej tajemniczy łącznik łączący jego domenę VWA z domeną N‑terminalną, która prawdopodobnie kontaktuje się z cNOR. Autorzy obserwują wiele konformacji, w których ten łącznik musi pokrywać różne odległości, co sugeruje, że może być stopniowo rozciągany. Gdy usunęli części tego łącznika, cNOR całkowicie stracił swoje niehemowe żelazo i aktywność, mimo że kompleks chaperonowy mógł się nadal formować, podkreślając, że kontrolowane rozciąganie tej części jest kluczowe dla zadania przebudowy.
Z ruchu obrotowego do wstawiania metalu
Składając ze sobą migawki strukturalne, autorzy proponują model, w którym NorQ zachowuje się jak molekularna wciągarka działająca przez NorD. W pierwszym kroku pierścień NorQ łączy się z NorD poprzez kontakt palca w porze i ogona z pętlą, podnosząc swoją aktywność ATPazową i blokując domenę VWA na miejscu. Następnie NorD angażuje cNOR w dwóch „punktach chwytu”: jeden obejmuje jego domenę N‑terminalną, a drugi odnosi się do regionu VWA lub łącznika w pobliżu motywu wiążącego metal. W miarę jak NorQ cykluje przez wiązanie i hydrolizę ATP, kolejne podjednostki wspinają się po spirali, przeciągając palec NorD wzdłuż wewnątrz poru. Ten ruch skręca domenę VWA względem chwytu N‑terminalnego i napina łącznik, przekazując moment obrotowy i napięcie do cNOR. Powstałe zniekształcenie ma otworzyć inaczej osłonięty obszar cNOR, pozwalając jonowi żelaza wstawić się do miejsca FeB, po czym kompleks może się uwolnić i zresetować.
Dlaczego to ma znaczenie poza jednym bakteryjnym enzymem
Dla osoby niezajmującej się specjalnie tematem wniosek jest taki, że para NorQ–NorD działa jak nanoskala klucz do rur, chwytając enzym w dwóch punktach i skręcając go wystarczająco, by włożyć atom żelaza na miejsce. Ta praca nie tylko wyjaśnia, jak zachodzi kluczowy krok w bakteryjnej chemii azotu, ale także ujawnia ogólną strategię „palec‑w‑porze”, której podobne systemy silnik‑partner mogą używać w całej biologii. Pokazując, jak paliwo chemiczne zostaje przekształcone w precyzyjną siłę skrętną działającą na docelowe białko, badanie dostarcza planu zrozumienia — i być może któregoś dnia inżynierii — maszyn kontrolujących gdzie i kiedy metale są wbudowywane w złożone urządzenia molekularne.
Cytowanie: Kahle, M., Appelgren, S., König, F. et al. NorQD AAA+ complex drives metal insertion by a twisting mechanism. Nat Commun 17, 3032 (2026). https://doi.org/10.1038/s41467-026-71044-4
Słowa kluczowe: ATPaza AAA+, metalochaperon, reduktaza tlenku azotu, struktura cryo-EM, wstawianie kofaktora metalowego