Clear Sky Science · zh
人源牛磺酸转运蛋白底物结合与抑制的结构机制
这个微小营养泵为何重要
牛磺酸是一种分布于人体各处的小分子,有助于维持心脏、大脑、眼睛和肌肉的正常功能。细胞不能仅靠被动扩散获得足够的牛磺酸;相反,它们借助位于细胞膜上的专门门控装置——牛磺酸转运蛋白。当该转运蛋白功能异常时,与心脏疾病、神经障碍、视力丧失和癌症有关。本研究以原子级细节揭示了人源牛磺酸转运蛋白如何抓取牛磺酸、将其运入细胞,以及如何被类药物分子阻断或劫持,为未来治疗提供线索。
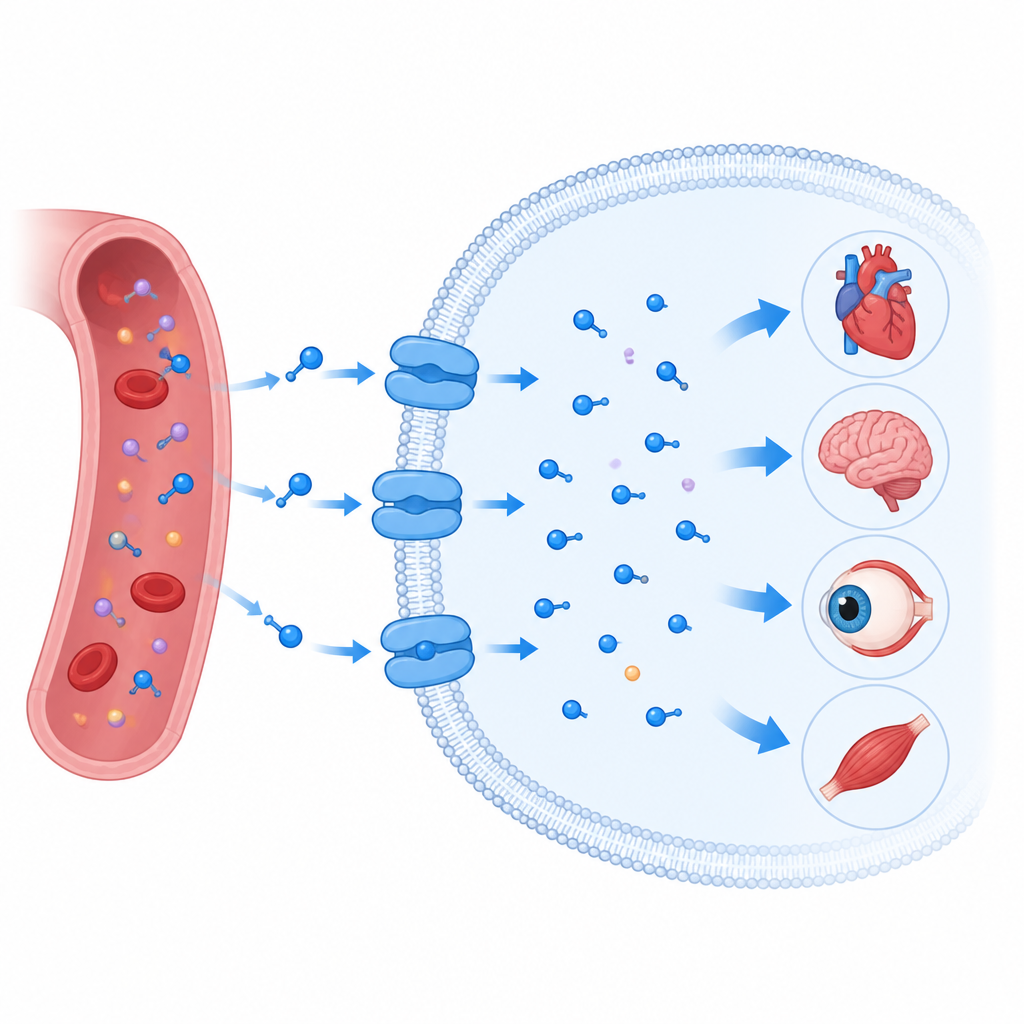
将牛磺酸拉入细胞的门
牛磺酸转运蛋白位于包裹每个细胞的疏油性膜中,属于一个大型转运蛋白家族,该家族还负责运输诸如血清素和多巴胺等脑内信号分子。与其同源蛋白类似,它并不是简单形成一个开放的通道,而更像一个旋转门:先向膜的一侧打开,围住货物后关闭,然后向另一侧打开。研究者使用冷冻电子显微镜确定了人源牛磺酸转运蛋白在工作时的多个三维快照。他们捕获了空载态、与牛磺酸结合态、与一种名为β-丙氨酸的相关分子结合态,以及与一种环状牛磺酸模拟物P4S结合的态,包含部分闭合和较为开放的向内朝向构象。
牛磺酸如何契合其专属口袋
结构显示牛磺酸停靠在转运蛋白深处的中央口袋内,该口袋由若干穿膜螺旋环绕。牛磺酸一端有带负电的磺酸基,另一端有带正电的氨基,两端由一段短碳链相连。转运蛋白提供了一个富含甘氨酸的小型凹槽来托举较为笨重的磺酸基,并通过氢键网络和一个配位的钠离子将其锚定。碳链嵌入一处疏水斑块,而氨基端则伸向一个带负电的残基,形成稳定的盐桥。这种精细调校的排列解释了为什么转运蛋白对牛磺酸具有很强的特异性,以及关键残基的微小变化如何削弱转运功能。
冒名顶替的分子及它们如何阻断或搭乘泵
β-丙氨酸是一种天然化合物,其羧基代替了牛磺酸的磺酸,几乎以相同方式结合,利用相同的口袋、钠离子和接触点。然而,它形成的氢键较少,这与其相对较弱的亲和力一致。P4S是一种合成的环状牛磺酸类似物,也将其磺酸基推入同一凹槽并占据牛磺酸位点,但其刚性的环状结构未能使氨基与关键酸性残基正确对齐。这种不匹配破坏了最强的相互作用之一,使P4S成为亲和力较低的阻断剂。由于这三种分子竞争同一位点,当β-丙氨酸或P4S浓度较高时,牛磺酸的摄取速度会减慢。
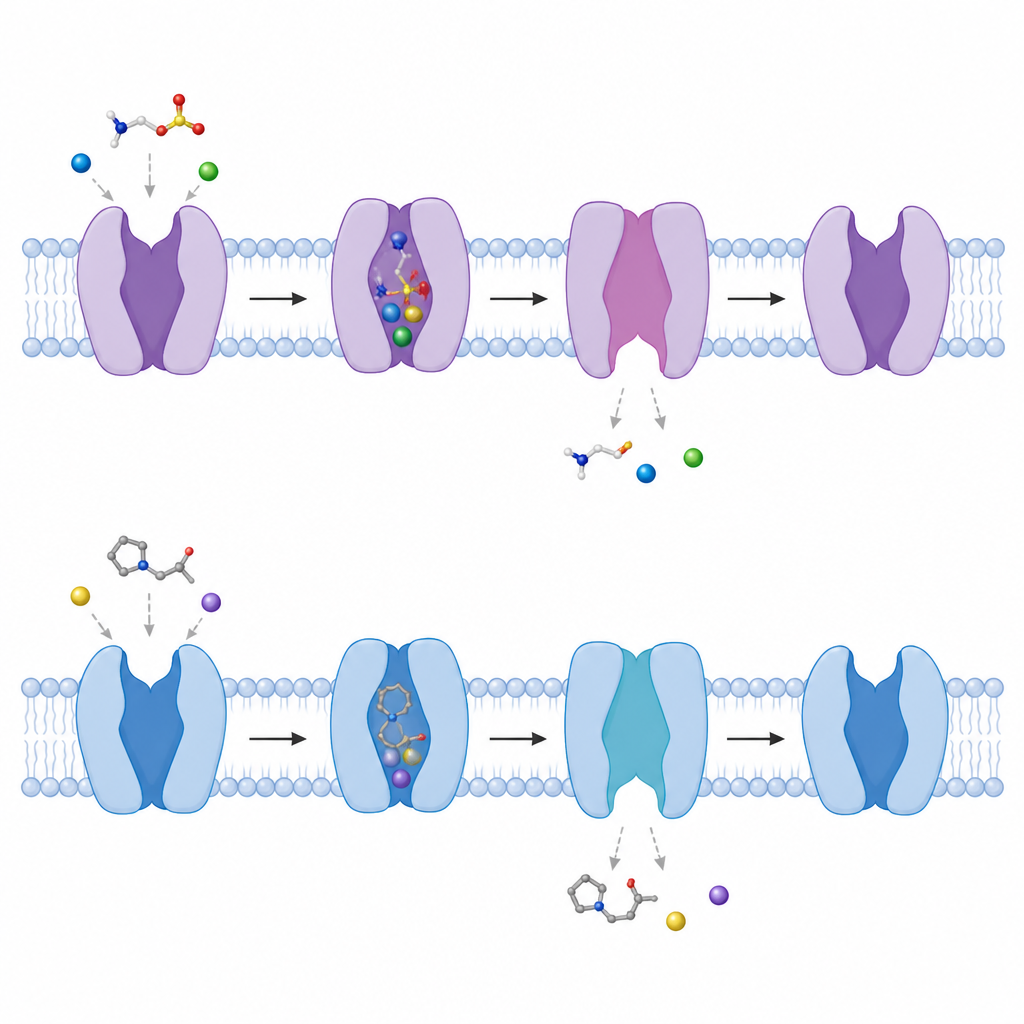
观察门在细胞内侧打开的过程
通过比较有无结合分子的结构,作者追踪了转运蛋白在不同构象间的切换。膜内侧附近的一段短螺旋向外弯曲约50度,另一段螺旋部分解旋,形成从中央口袋通往细胞内的通道。随着这些变化,精心排列的钠离子结合位点解体,使钠离子随后是牛磺酸更容易释放到细胞内部。研究团队还显示,在没有任何结合分子的情况下,转运蛋白会在更闭合和更开放的向内朝向形态之间自然翻转,暗示其构象能谱不断变化,使其在牛磺酸出现时能迅速响应。
重新定义一种抑制剂并展望药物
令人惊讶的是,功能测试表明P4S并非仅仅是将门卡住的简单塞子。相反,它可以像牛磺酸本身一样被转运,通过相同的钠梯度移动,甚至触发细胞内预装牛磺酸的释放。换句话说,P4S表现为一种可被运输的底物类似物,同时又与牛磺酸竞争位点。结构快照与转运测量共同勾勒出牛磺酸转运蛋白的完整工作循环,并明确指出控制每一步的特定口袋和运动。对非专业读者而言,这意味着研究者现在拥有一份详细的蓝图,可用于设计既能更有效补充牛磺酸又能在如癌症等依赖过度牛磺酸转运的疾病中选择性减缓其摄取的新分子。
引用: Qi, Y., Zhang, Y., Wang, D. et al. Structural mechanism of substrate binding and inhibition of human taurine transporter. Nat Commun 17, 4257 (2026). https://doi.org/10.1038/s41467-026-70772-x
关键词: 牛磺酸转运蛋白, 膜转运, 冷冻电子显微镜, 神经心脏健康, 药物设计