Clear Sky Science · fr
Mécanisme structural de la liaison du substrat et de l’inhibition du transporteur humain de la taurine
Pourquoi cette petite pompe nutritive compte
La taurine est une petite molécule présente dans tout le corps humain, où elle contribue au bon fonctionnement du cœur, du cerveau, des yeux et des muscles. Les cellules ne peuvent pas compter sur la diffusion passive pour obtenir suffisamment de taurine ; elles utilisent plutôt une porte spécialisée dans la membrane cellulaire appelée transporteur de la taurine. Lorsque ce transporteur dysfonctionne, il est associé à des maladies cardiaques, des troubles nerveux, une perte de vision et au cancer. Cette étude révèle, à l’échelle atomique, comment le transporteur humain de la taurine saisit la taurine, la transfère dans les cellules, et peut être bloqué ou détourné par des molécules de type médicament, fournissant des pistes pour de futures thérapies.
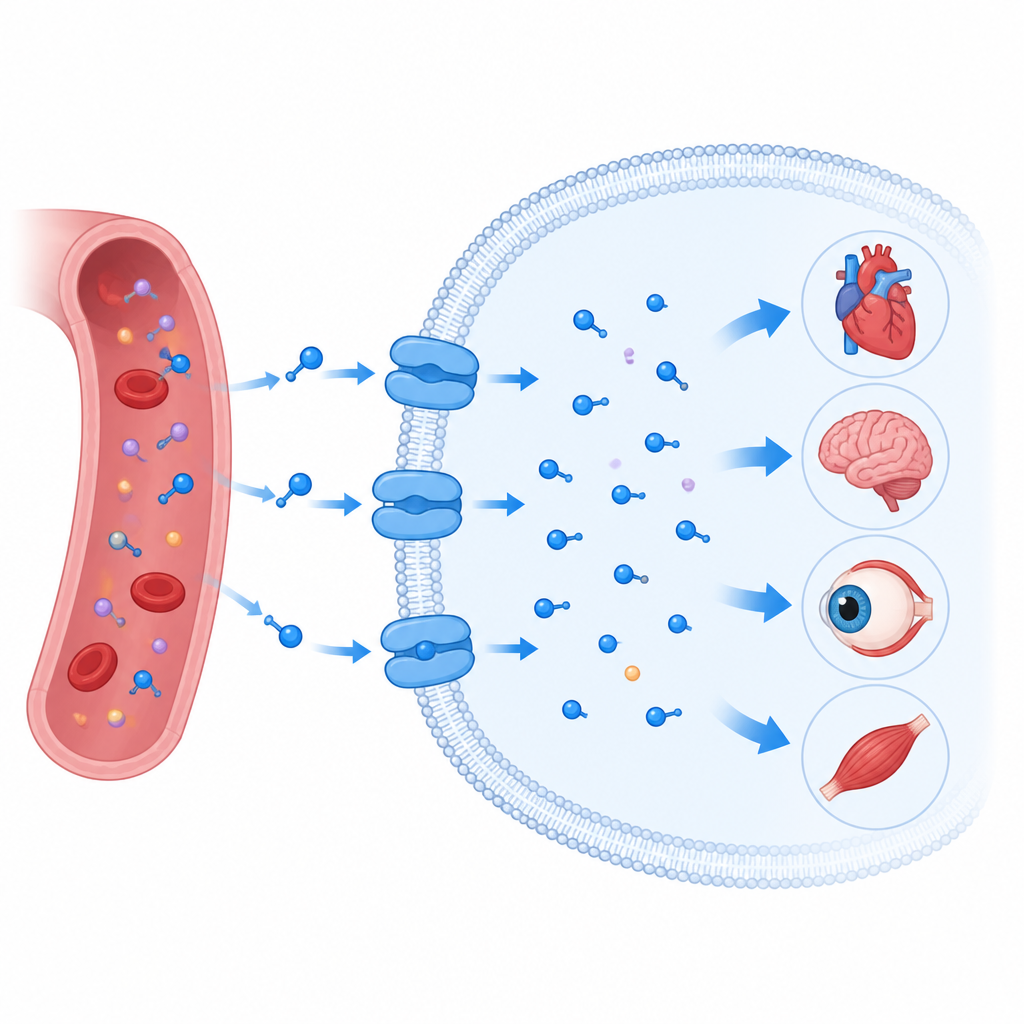
Une porte qui attire la taurine dans les cellules
Le transporteur de la taurine est inséré dans la membrane huileuse qui entoure chaque cellule et appartient à une grande famille de protéines de transport qui déplacent aussi des messagers cérébraux comme la sérotonine et la dopamine. Comme ses apparentés, il ne forme pas simplement un canal ouvert. Il fonctionne plutôt comme une porte tournante : il s’ouvre d’un côté de la membrane, se referme autour de sa cargaison, puis s’ouvre de l’autre côté. Les chercheurs ont utilisé la cryo‑microscopie électronique pour déterminer plusieurs instantanés tridimensionnels du transporteur humain de la taurine en action. Ils l’ont capturé vide, lié à la taurine, lié à une molécule apparentée appelée bêta‑alanine, et lié à un mimétique annulé de la taurine connu sous le nom de P4S, dans des formes partiellement fermées et plus ouvertes dirigées vers l’intérieur.
Comment la taurine s’insère dans sa poche sur mesure
Les structures montrent que la taurine se loge dans une poche centrale profonde à l’intérieur du transporteur, entourée par plusieurs hélices traversant la membrane. La taurine porte un groupe sulfonate chargé négativement à une extrémité et un groupe amino chargé positivement à l’autre, reliés par une courte chaîne carbonée. Le transporteur présente une petite niche riche en glycine qui soutient le volumineux groupe sulfonate et l’ancre via un réseau de liaisons hydrogène et un ion sodium coordonné. La chaîne carbonée s’insère dans une zone hydrophobe, tandis que l’extrémité amino atteint un résidu chargé négativement qui forme un pont salin stabilisateur. Cet agencement finement accordé explique pourquoi le transporteur préfère fortement la taurine par rapport à d’autres molécules similaires et comment de petits changements dans des résidus clés peuvent affaiblir le transport.
Molécules usurpes et modes de blocage ou de transport
La bêta‑alanine, un composé naturel avec un groupe carboxyle au lieu du sulfonate de la taurine, se lie quasiment de la même façon, utilisant la même poche, les mêmes ions sodium et les mêmes points de contact. Cependant, elle établit moins de liaisons hydrogène, ce qui correspond à son affinité légèrement plus faible pour le transporteur. Le P4S, un analogue synthétique annulé de la taurine, insère aussi son groupe sulfonate dans la même niche et occupe le site de la taurine, mais son anneau rigide n’aligne pas correctement son groupe amino avec le résidu acide clé. Cet incompatibilité perturbe l’une des interactions les plus fortes et fait du P4S un bloqueur d’affinité plus faible. Comme ces trois molécules rivalisent pour le même site, l’absorption de la taurine peut être ralentie lorsque la bêta‑alanine ou le P4S est présent à des concentrations élevées.
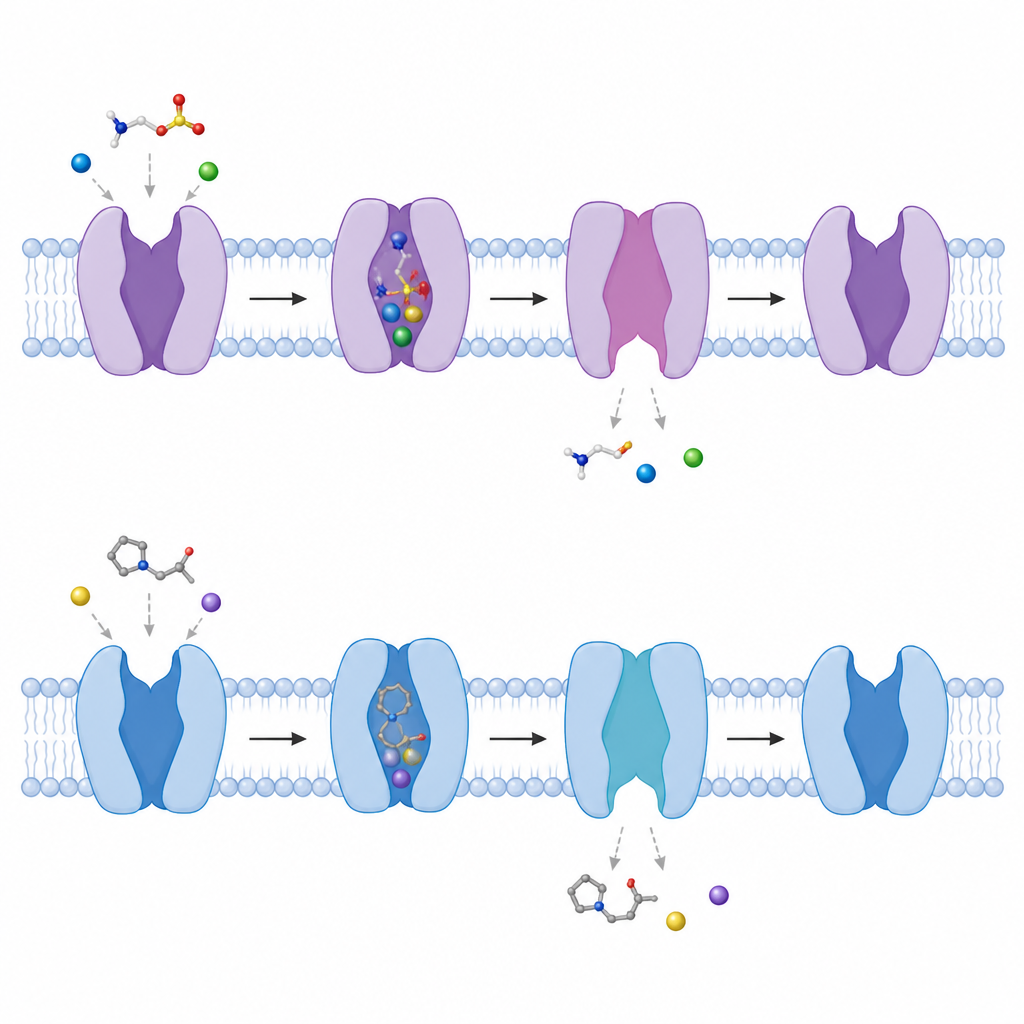
Observer la porte s’ouvrir vers l’intérieur de la cellule
En comparant les structures avec et sans molécules liées, les auteurs ont suivi comment le transporteur bascule entre conformations. Un court segment hélicoïdal près du côté interne de la membrane se courbe vers l’extérieur d’environ 50 degrés, et une autre hélice se déroule partiellement, créant un tunnel reliant la poche centrale à l’intérieur de la cellule. Au fur et à mesure, les sites de liaison au sodium soigneusement organisés se défont, facilitant la libération du sodium puis de la taurine dans le milieu intracellulaire. L’équipe a également montré qu’en l’absence de toute molécule liée, le transporteur bascule naturellement entre des formes vers l’intérieur plus fermées et plus ouvertes, suggérant un paysage conformationnel en constante évolution qui lui permet de répondre rapidement à l’arrivée de taurine.
Redéfinir un inhibiteur et perspectives pour les médicaments
De manière surprenante, des tests fonctionnels ont révélé que le P4S n’est pas seulement un simple calage qui bloque la porte. Au contraire, il peut être transporté à travers le transporteur comme la taurine elle‑même, entraîné par le même gradient de sodium, et peut même déclencher la libération de taurine préchargée des cellules. Autrement dit, le P4S se comporte comme un analogue de substrat transporté qui entre en concurrence avec la taurine. Ensemble, les instantanés structurels et les mesures de transport décrivent un cycle de fonctionnement complet pour le transporteur de la taurine et identifient les poches et mouvements spécifiques qui contrôlent chaque étape. Pour le grand public, cela signifie que les chercheurs disposent désormais d’un plan détaillé pour concevoir de nouvelles molécules qui fournissent la taurine plus efficacement ou ralentissent sélectivement son absorption dans des maladies comme le cancer, où les cellules dépendent d’un transport excessif de la taurine.
Citation: Qi, Y., Zhang, Y., Wang, D. et al. Structural mechanism of substrate binding and inhibition of human taurine transporter. Nat Commun 17, 4257 (2026). https://doi.org/10.1038/s41467-026-70772-x
Mots-clés: transporteur de la taurine, transport membranaire, cryo‑microscopie électronique, santé neurocardiaque, conception de médicaments