Clear Sky Science · it
Meccanismo strutturale del legame del substrato e dell'inibizione del trasportatore umano della taurina
Perché questa piccola pompa nutritiva è importante
La taurina è una piccola molecola presente in tutto il corpo umano, dove contribuisce al corretto funzionamento di cuore, cervello, occhi e muscoli. Le nostre cellule non possono contare sulla sola diffusione passiva per ottenere abbastanza taurina; invece usano una porta specializzata nella membrana cellulare chiamata trasportatore della taurina. Quando questo trasportatore funziona male, è associato a malattie cardiache, disturbi neurologici, perdita della vista e cancro. Questo studio rivela, a livello atomico, come il trasportatore umano della taurina afferra la taurina, la trasferisce nelle cellule e può essere bloccato o dirottato da molecole di tipo farmacologico, offrendo indizi per future terapie.
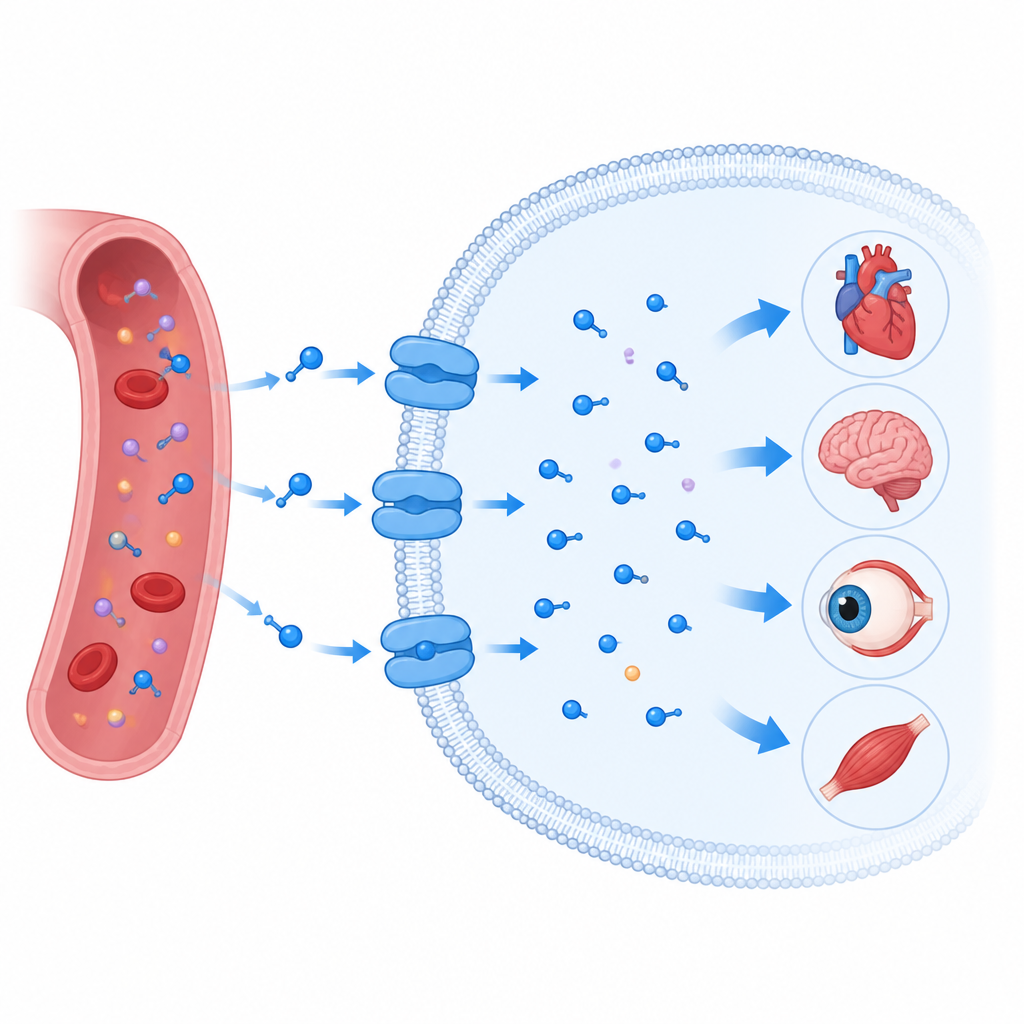
Una porta che attrae la taurina nelle cellule
Il trasportatore della taurina è inserito nella membrana lipidica che circonda ogni cellula e appartiene a una grande famiglia di proteine di trasporto che muovono anche messaggeri cerebrali come serotonina e dopamina. Come i suoi parenti, non forma semplicemente un canale aperto. Funziona piuttosto come una porta girevole: si apre da un lato della membrana, si chiude attorno al suo carico e poi si apre dall’altro lato. I ricercatori hanno utilizzato la crio-microscopia elettronica per determinare molteplici istantanee tridimensionali del trasportatore umano della taurina in azione. Lo hanno catturato vuoto, legato alla taurina, legato a una molecola correlata chiamata beta-alanina e legato a un analogo anulare della taurina noto come P4S, in forme rivolte verso l’interno parzialmente chiuse e più aperte.
Come la taurina si adatta nel suo alloggiamento su misura
Le strutture mostrano che la taurina si ancorà in una tasca centrale profonda all’interno del trasportatore, circondata da diversi eliche che attraversano la membrana. La taurina possiede un gruppo solfonato carico negativamente a un’estremità e un gruppo amminico carico positivamente all’altra, collegati da una breve catena carboniosa. Il trasportatore presenta una nicchia piccola e ricca di glicine che avvolge il voluminoso gruppo solfonato e lo ancora tramite una rete di legami a idrogeno e un ione sodio coordinato. La catena carboniosa si sistemava in una zona idrofobica, mentre l’estremità amminica raggiunge un residuo carico negativamente che forma un ponte salino stabilizzante. Questo assetto finemente sintonizzato spiega perché il trasportatore preferisce fortemente la taurina rispetto ad altre molecole simili e come piccole modifiche in residui chiave possano indebolire il trasporto.
Molecole impostrici e come bloccano o sfruttano la pompa
La beta-alanina, un composto naturale con un gruppo carbossilico al posto del solfonato della taurina, si lega quasi allo stesso modo, usando la stessa tasca, gli stessi ioni sodio e i medesimi punti di contatto. Tuttavia stabilisce meno legami a idrogeno, il che corrisponde alla sua affinità leggermente inferiore per il trasportatore. P4S, un analogo sintetico anulare della taurina, inserisce anch’esso il gruppo solfonato nella stessa nicchia e occupa il sito della taurina, ma il suo anello rigido non allinea correttamente il gruppo amminico con il residuo acido chiave. Questo inadattamento interrompe una delle interazioni più forti e rende P4S un bloccante a minore affinità. Poiché tutte e tre le molecole competono per lo stesso sito, l’assorbimento di taurina può rallentare quando beta-alanina o P4S sono presenti a livelli elevati.
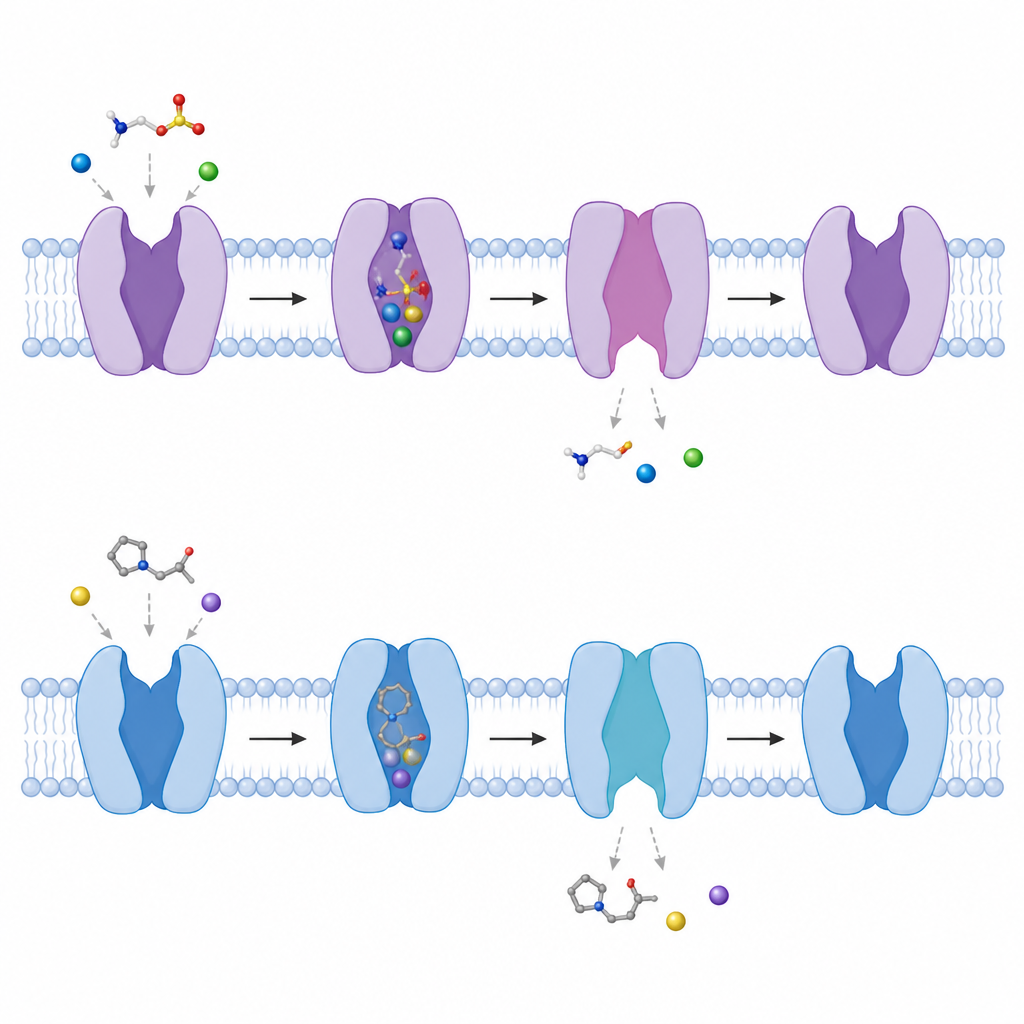
Osservare la porta aprirsi verso l’interno della cellula
Confrontando strutture con e senza molecole legate, gli autori hanno seguito come il trasportatore alterna le conformazioni. Un breve segmento elicoidale vicino al lato interno della membrana si piega verso l’esterno di circa 50 gradi, e un’altra elica si parzialmente svolge, creando un tunnel dalla tasca centrale all’interno della cellula. Man mano che questo avviene, i siti di legame del sodio accuratamente organizzati si disfano, facilitando il rilascio prima del sodio e poi della taurina nell’interno della cellula. Il gruppo ha anche mostrato che in assenza di molecole legate il trasportatore ruota naturalmente tra forme rivolte verso l’interno più chiuse e più aperte, suggerendo un paesaggio conformazionale in costante mutamento che gli permette di rispondere rapidamente quando compare la taurina.
Ridefinire un inibitore e guardare verso i farmaci
Sorprendentemente, test funzionali hanno rivelato che P4S non è semplicemente un fermo che inceppa la porta. Al contrario, può essere trasportato attraverso il trasportatore come la taurina stessa, mosso dallo stesso gradiente di sodio, e può persino indurre il rilascio di taurina precaricata dalle cellule. In altre parole, P4S si comporta come un analogo di substrato trasportato che compete con la taurina. Insieme, le istantanee strutturali e le misure di trasporto delineano un ciclo di funzionamento completo per il trasportatore della taurina e individuano le tasche specifiche e i movimenti che controllano ogni fase. Per i non specialisti, questo significa che i ricercatori dispongono ora di un progetto dettagliato per progettare nuove molecole che o forniscano taurina in modo più efficace o rallentino selettivamente il suo assorbimento in malattie come il cancro, dove le cellule dipendono da un eccessivo trasporto di taurina.
Citazione: Qi, Y., Zhang, Y., Wang, D. et al. Structural mechanism of substrate binding and inhibition of human taurine transporter. Nat Commun 17, 4257 (2026). https://doi.org/10.1038/s41467-026-70772-x
Parole chiave: trasportatore della taurina, trasporto attraverso la membrana, crio-microscopia elettronica, salute neurocardiaca, progettazione di farmaci