Clear Sky Science · ar
الآلية البنائية لالتقاط الركيزة وتثبيط ناقل التورين البشري
لماذا تهم هذه المضخة المغذية الصغيرة
التورين جزيء صغير منتشر في أنحاء الجسم البشري، حيث يساعد في الحفاظ على عمل القلب والدماغ والعينين والعضلات بشكل سليم. لا يمكن لخلاياْنا الاعتماد على الانتشار السلبي للحصول على كمية كافية من التورين؛ بل تستخدم بوابة متخصصة في غشاء الخلية تُعرف بناقلة التورين. عند خلل هذه الناقلة، يرتبط ذلك بأمراض القلب واضطرابات الأعصاب وفقدان البصر والسرطان. تكشف هذه الدراسة، بتفصيل ذري، كيف تمسك ناقلة التورين البشرية بالتورين، وتنقله إلى داخل الخلايا، وكيف يمكن أن تُحجب أو تُخترق بواسطة جزيئات شبيهة بالأدوية، مما يوفر دلائل للعلاجات المستقبلية.
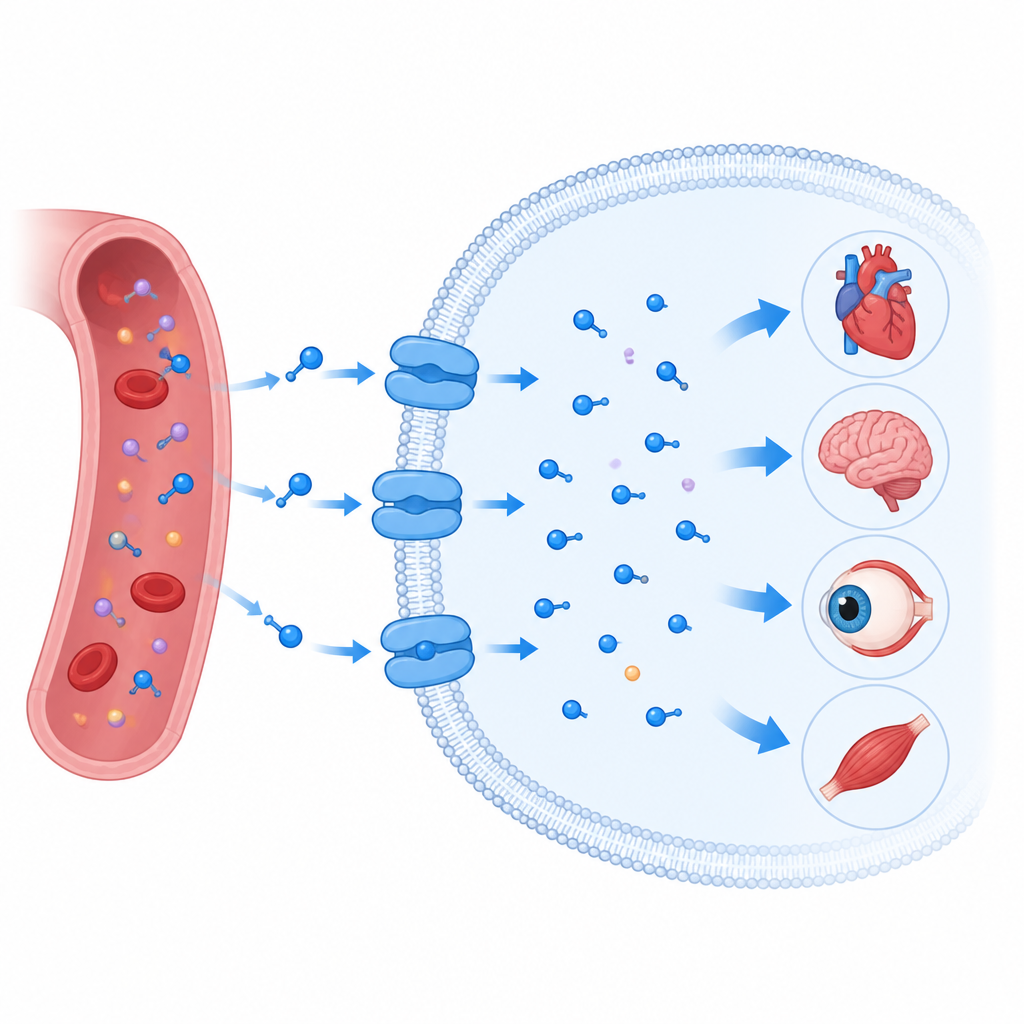
بوابة تسحب التورين إلى داخل الخلايا
تقع ناقلة التورين داخل الغشاء الدهني المحيط بكل خلية وتنتمي إلى عائلة كبيرة من بروتينات النقل التي تحرك أيضاً ناقلات عصبية مثل السيروتونين والدوبامين. مثل أقاربها، لا تُشكّل مجرد قناة مفتوحة. بل تعمل أشبه بـ"باب دوار": تفتح إلى جهة من الغشاء، تغلق حول حمولتها، ثم تفتح إلى الجهة الأخرى. استخدم الباحثون الميكروسكوب الإلكتروني بالتبريد لتحديد عدة لقطات ثلاثية الأبعاد لناقلة التورين البشرية أثناء عملها. التقطوا حالاتها فارغة، مرتبطة بالتورين، مرتبطة بجزيء ذي صلة يُدعى بيتا ألاناين، ومرتبطة بمقلد التورين الحلقي المسمى P4S، في أشكال مواجهَة للداخل جزئياً مغلقة وأكثر انفتاحاً.
كيف يتناسب التورين في جيبه المخصص
تُظهر الهياكل أن التورين يرسو في جيب مركزي عميق داخل الناقلة، محاط بعدة لفائف حلزونية عابرة للغشاء. يحمل التورين مجموعة سلفونات سالبة الشحنة في أحد الطرفين ومجموعة أمينية موجبة في الطرف الآخر، مربوطة بسلسلة كربون قصيرة. تمتلك الناقلة شقاً صغيراً غنيّاً بالجليسين يحتضن مجموعة السلفونات الضخمة ويرسخها عبر شبكة من الروابط الهيدروجينية وأيون صوديوم منسق. تستقر سلسلة الكربون في رقعة دهنية، بينما يصل الطرف الأميني إلى بقايا حمضية سالبة تشكل جسر ملحي معزِّز. يفسر هذا الترتيب الدقيق تفضيل الناقلة الواضح للتورين على جزيئات مماثلة وكيف أن تغييرات صغيرة في بقايا رئيسية يمكن أن تضعف النقل.
الجزيئات المحتالة وكيف تحجب أو تسافر مع المضخة
يرتبط بيتا ألاناين، وهو مركب طبيعي يحمل مجموعة كربوكسيل بدل سلفونات التورين، بطريقة تكاد تكون نفسها، مستخدماً نفس الجيب وأيونات الصوديوم ونقاط التماس. ومع ذلك، يُكوِّن روابط هيدروجينية أقل، مما يتوافق مع تقارب أضعف قليلاً مع الناقلة. يدفع P4S، وهو نظير اصطناعي حلقي الشكل للتورين، مجموعة السلفونات أيضاً إلى نفس الشق ويشغل موقع التورين، لكن حلقته الصلبة لا تصطف بشكل صحيح لتوضع مجموعته الأمينية مقابل البقايا الحمضية الرئيسية. هذا عدم التطابق يعرقل إحدى أقوى التفاعلات ويجعل P4S مثبطاً أقل تقارباً. وبما أن الثلاثة يتنافسون على نفس الموقع، يمكن أن يتباطأ امتصاص التورين عندما يكون تركيز بيتا ألاناين أو P4S عالياً.
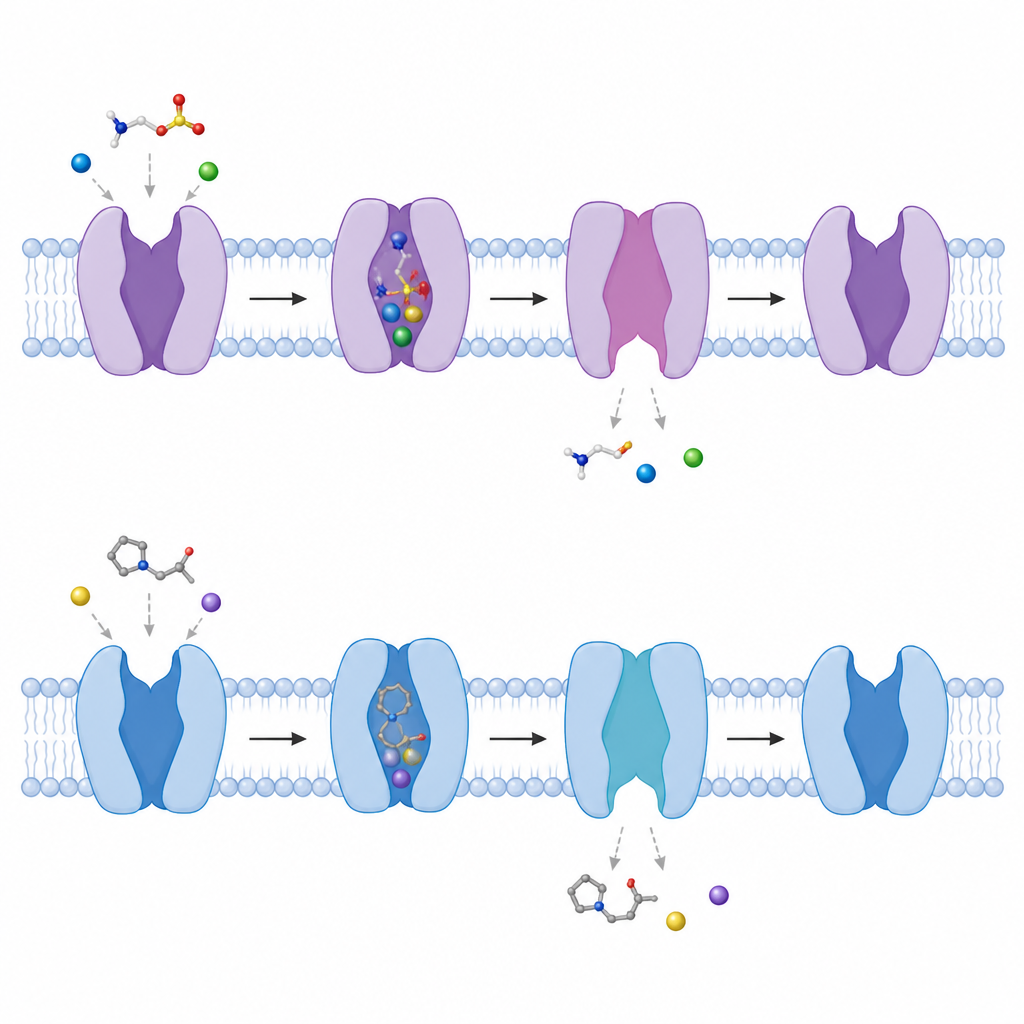
مراقبة فتح البوابة داخل الخلية
من خلال مقارنة الهياكل بوجود وبدون جزيئات مرتبطة، تتبع المؤلفون كيف تتقلب الناقلة بين التَشكُّلات. ينثني مقطع حلزوني قصير قرب الجانب الداخلي للغشاء إلى الخارج بنحو 50 درجة، وتتفكك حلزونة أخرى جزئياً، مكونة نفقاً من الجيب المركزي إلى داخل الخلية. مع حدوث ذلك، تتفكك مواقع ربط الصوديوم المجهزة بعناية، مما يسهل تحرير الصوديوم ثم التورين إلى داخل الخلية. كما أظهر الفريق أنه في غياب أي جزيئات مرتبطة، تقلب الناقلة طبيعياً بين أشكال مواجهة للداخل أكثر إغلاقاً وأكثر انفتاحاً، مما يوحي بمشهد متغير باستمرار يسمح لها بالاستجابة بسرعة عند ظهور التورين.
إعادة تعريف مثبط ونظرة نحو الأدوية
وبشكل مفاجئ، كشفت الاختبارات الوظيفية أن P4S ليس مجرد سدادة تبطيء البوابة. بل يمكن دفعه عبر الناقلة مثل التورين نفسه، بدافع نفس تدرج الصوديوم، بل ويمكن أن يحفز إطلاق التورين المحمَّل مسبقاً من الخلايا. بعبارة أخرى، يتصرف P4S كنسخة ركيزة ناقلة يحدث أن تتنافس مع التورين. ترسم اللقطات البنائية وقياسات النقل معاً دورة عمل كاملة لناقلة التورين وتحدد الجيوب والحركات المحددة التي تتحكم في كل خطوة. بالنسبة لغير المتخصصين، يعني هذا أن الباحثين لديهم الآن مخطط تفصيلي دقيق لتصميم جزيئات جديدة إما لتزويد التورين بفعالية أكبر أو لإبطاء امتصاصه انتقائياً في أمراض مثل السرطان، حيث تعتمد الخلايا على نقل مفرط للتورين.
الاستشهاد: Qi, Y., Zhang, Y., Wang, D. et al. Structural mechanism of substrate binding and inhibition of human taurine transporter. Nat Commun 17, 4257 (2026). https://doi.org/10.1038/s41467-026-70772-x
الكلمات المفتاحية: ناقلة التورين, نقل عبر الغشاء, الميكروسكوب الإلكتروني بالتبريد, الصحة العصبية القلبية, تصميم الأدوية