Clear Sky Science · nl
Structureel mechanisme van substraatbinding en remming van de menselijke taurine-transporter
Waarom deze kleine voedingspompen ertoe doen
Taurine is een kleine molecule die in het hele menselijk lichaam voorkomt en helpt het hart, de hersenen, de ogen en de spieren goed te laten functioneren. Cellen kunnen niet genoeg taurine verkrijgen door passieve diffusie; in plaats daarvan gebruiken ze een gespecialiseerd poortje in het celmembraan, de taurine-transporter. Als deze transporter niet goed werkt, wordt dat in verband gebracht met hartaandoeningen, zenuwproblemen, verlies van gezichtsvermogen en kanker. Deze studie toont op atomair niveau hoe de menselijke taurine-transporter taurine vastgrijpt, in cellen brengt en kan worden geblokkeerd of gekaapt door geneesmiddelachtige moleculen, wat aanwijzingen geeft voor toekomstige therapieën.
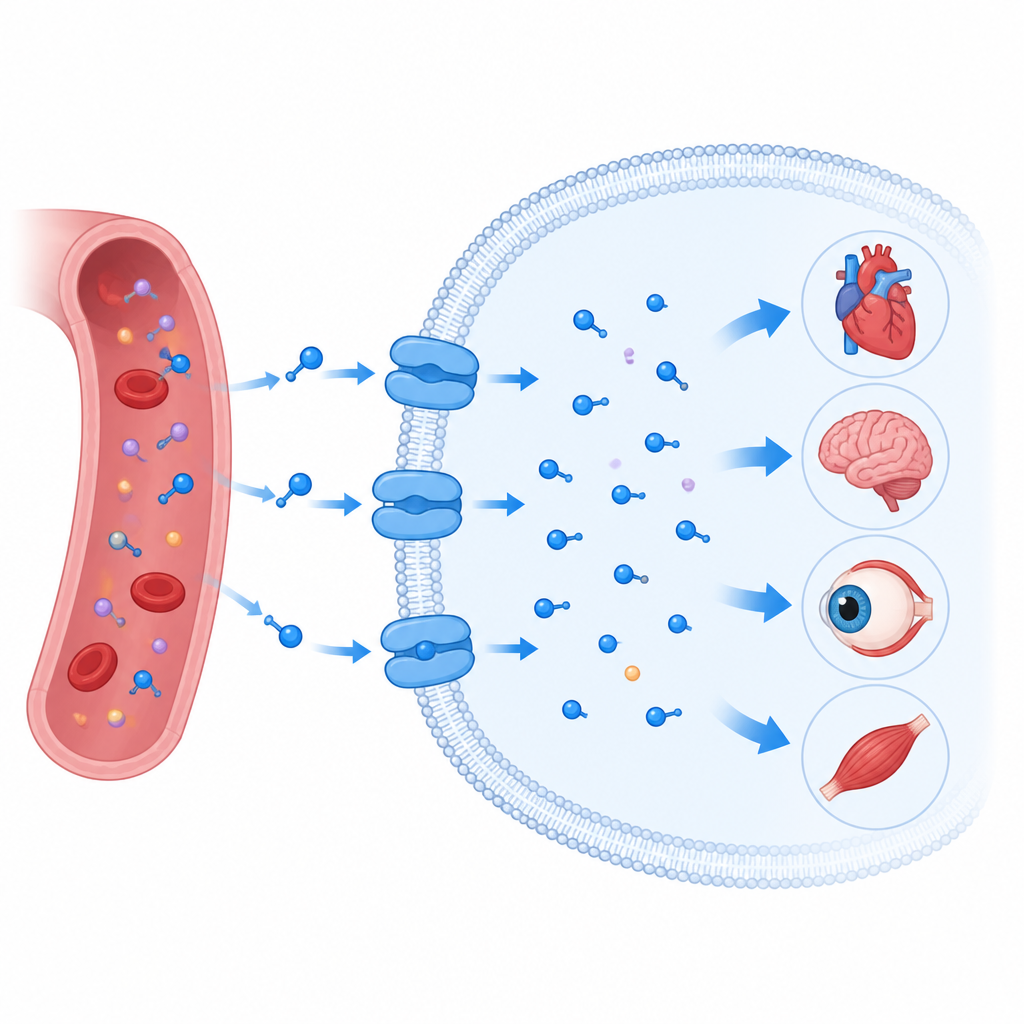
Een poort die taurine in cellen trekt
De taurine-transporter bevindt zich in het vette membraan dat elke cel omgeeft en behoort tot een grote familie van transporteiwitten die ook boodschappers in de hersenen verplaatsen, zoals serotonine en dopamine. Net als zijn verwanten vormt hij niet simpelweg een open kanaal. In plaats daarvan werkt hij meer als een draaideur: hij opent aan één kant van het membraan, sluit om zijn lading en opent dan aan de andere kant. De onderzoekers gebruikten cryo-elektronenmicroscopie om meerdere driedimensionale momentopnamen van de menselijke taurine-transporter in actie vast te leggen. Ze legden de transporter vast leeg, gebonden aan taurine, gebonden aan een verwant molecuul genaamd bèta-alanine, en gebonden aan een ringvormig taurine-mimeticum bekend als P4S, in zowel gedeeltelijk gesloten als meer open naar binnen gerichte vormen.
Hoe taurine in zijn op maat gemaakte pocket past
De structuren laten zien dat taurine in een centraal pocket diep in de transporter past, omgeven door meerdere membraanoverspannende helixen. Taurine heeft aan de ene kant een negatief geladen sulfonaatgroep en aan de andere kant een positief geladen aminogroep, verbonden door een korte koolstofketen. De transporter heeft een kleine, glycine-rijke nis die de omvangrijke sulfonaatgroep omsluit en verankert via een web van waterstofbruggen en een gecoördineerd natriumion. De koolstofketen nestelt in een vette plek, terwijl het amino-einde een negatief geladen residu bereikt dat een stabiliserende zoutbrug vormt. Deze fijn afgestemde rangschikking verklaart waarom de transporter een sterke voorkeur heeft voor taurine boven andere vergelijkbare moleculen en hoe kleine veranderingen in sleutelresiduen het transport kunnen verzwakken.
Bedriegersmoleculen en hoe ze de pomp blokkeren of meereizen
Bèta-alanine, een natuurlijk verbinding met een carboxylgroep in plaats van taurine's sulfonaat, bindt vrijwel op dezelfde manier en gebruikt dezelfde pocket, natriumionen en contactpunten. Het vormt echter minder waterstofbruggen, wat overeenkomt met zijn iets zwakkere affiniteit voor de transporter. P4S, een synthetisch, ringvormig taurine-analoog, schuift ook zijn sulfonaatgroep in dezelfde nis en bezet de taurine-plaats, maar zijn starre ring brengt de aminogroep niet goed uitgelijnd met het sleutelzure residu. Deze slechte passing verstoort een van de sterkste interacties en maakt P4S tot een remmer met lagere affiniteit. Omdat alle drie de moleculen om dezelfde plaats concurreren, kan taurine-opname worden vertraagd wanneer bèta-alanine of P4S in hoge concentraties aanwezig zijn.
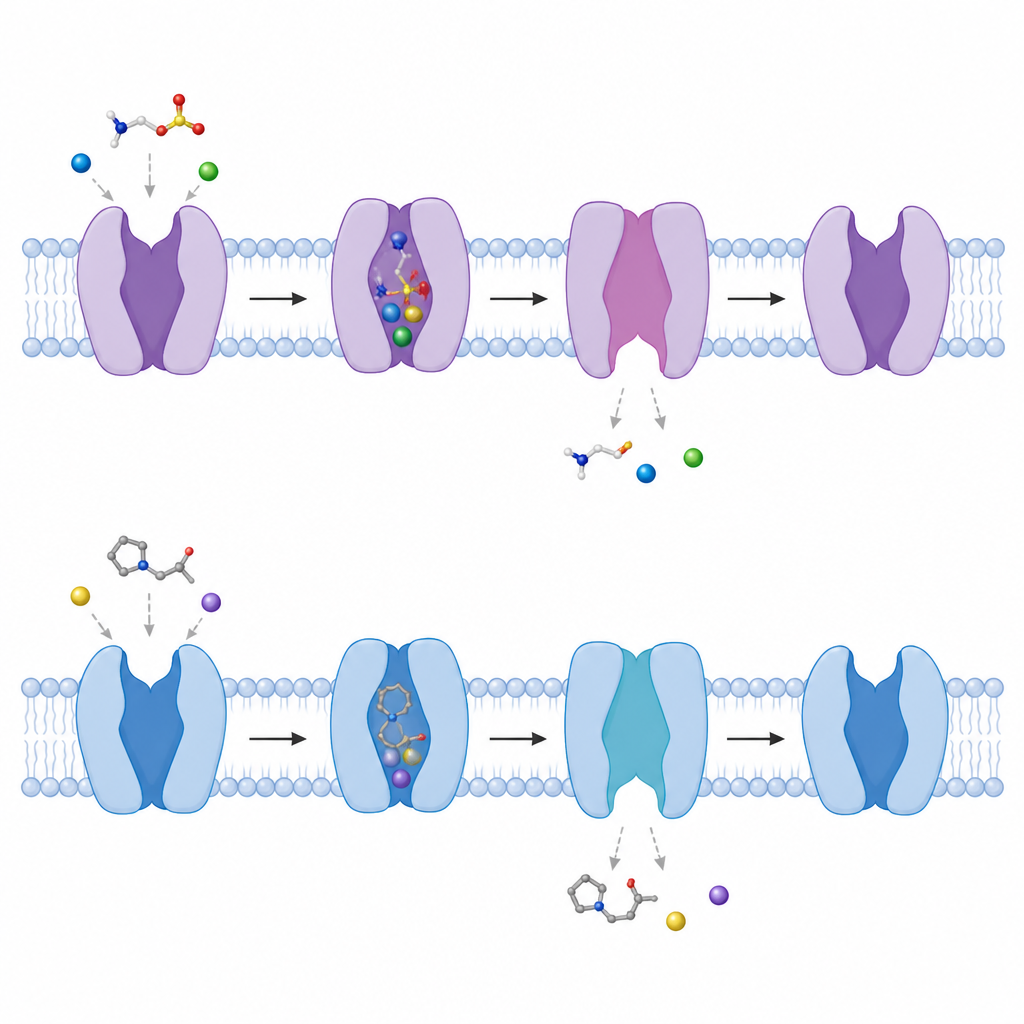
Het zien zwaaien van de poort naar binnen in de cel
Door structuren met en zonder gebonden moleculen te vergelijken, volgden de auteurs hoe de transporter schakelt tussen conformaties. Een kort helisch segment nabij de binnenzijde van het membraan buigt naar buiten met ongeveer 50 graden, en een andere helix windt deels uit, waardoor een tunnel ontstaat van het centrale pocket naar de binnenkant van de cel. Terwijl dit gebeurt, vallen de zorgvuldig gerangschikte natrium-bindingsplaatsen uit elkaar, waardoor het makkelijker wordt voor natrium en vervolgens taurine om in het celinterieur te worden vrijgegeven. Het team toonde ook aan dat, in afwezigheid van gebonden moleculen, de transporter vanzelf schakelt tussen meer gesloten en meer open naar binnen gerichte vormen, wat duidt op een voortdurend verschuivend landschap dat het in staat stelt snel te reageren wanneer taurine verschijnt.
Het herdefiniëren van een remmer en vooruitkijken naar geneesmiddelen
Verrassend genoeg onthulden functionele tests dat P4S niet slechts een eenvoudige stop is die de poort vastzet. In plaats daarvan kan het, net als taurine zelf, door de transporter worden verplaatst, aangedreven door dezelfde natriumgradiënt, en zelfs de afgifte van vooraf geladen taurine uit cellen activeren. Met andere woorden gedraagt P4S zich als een getransporteerd substraat-analoog dat toevallig concurreert met taurine. Samen schetsen de structurele momentopnamen en transportmetingen een volledige werkcyclus voor de taurine-transporter en wijzen ze de specifieke pockets en bewegingen aan die elke stap sturen. Voor niet-specialisten betekent dit dat onderzoekers nu een gedetailleerd blauwdruk hebben om nieuwe moleculen te ontwerpen die óf taurine effectiever aanleveren óf selectief de opname vertragen bij ziekten zoals kanker, waar cellen afhankelijk zijn van overmatig taurine-transport.
Bronvermelding: Qi, Y., Zhang, Y., Wang, D. et al. Structural mechanism of substrate binding and inhibition of human taurine transporter. Nat Commun 17, 4257 (2026). https://doi.org/10.1038/s41467-026-70772-x
Trefwoorden: taurine-transporter, membraantransport, cryo-elektronenmicroscopie, neurocardiale gezondheid, medicijnontwerp