Clear Sky Science · ru
Структурный механизм связывания субстрата и ингибирования человеческого тауринового транспорта
Почему этот крошечный насос питательных веществ важен
Таурин — это небольшая молекула, широко распространённая в организме человека, которая помогает поддерживать нормальную работу сердца, мозга, глаз и мышц. Клетки не могут полагаться на пассивную диффузию, чтобы получить достаточное количество таурина; вместо этого они используют специализированные ворота в клеточной мембране, называемые тауриновым транспортером. Когда этот транспортер работает неправильно, это связано с сердечными заболеваниями, неврологическими нарушениями, потерей зрения и раком. В этом исследовании показано с атомной детализацией, как человеческий тауриновый транспортер захватывает таурин, перемещает его в клетки и как на него можно повлиять или захватить лекареподобными молекулами — что даёт подсказки для будущих терапий.
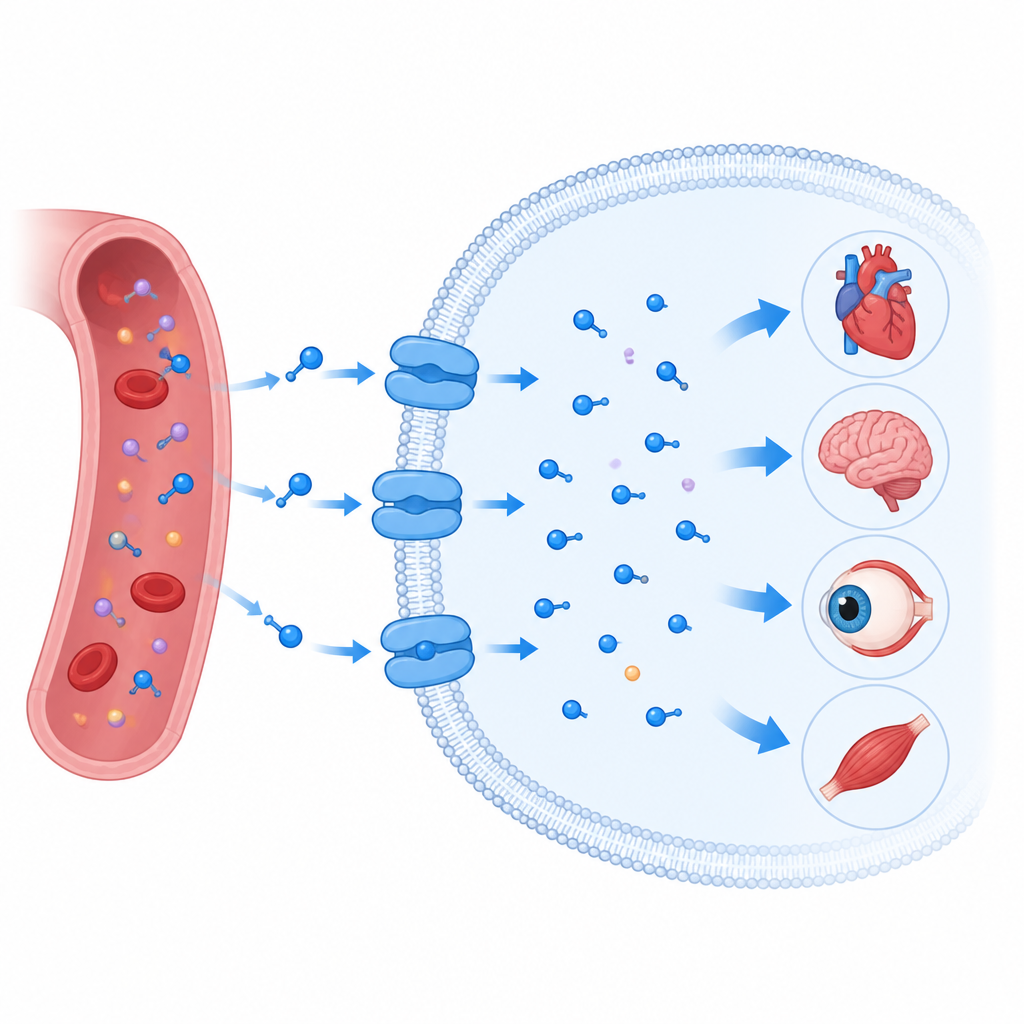
Ворота, которые втягивают таурин в клетки
Тауриновый транспортер встроен в липидную мембрану, окружающую каждую клетку, и принадлежит к большой семье транспортных белков, которые также переносят нейромедиаторы, такие как серотонин и дофамин. В отличие от простого открытого канала, он действует скорее как вращающаяся дверь: открывается в одну сторону мембраны, закрывается вокруг груза, затем открывается в другую сторону. Исследователи использовали криоэлектронную микроскопию, чтобы получить несколько трёхмерных снимков человеческого тауринового транспортера в действии. Они зафиксировали его в пустом состоянии, связанный с таурином, с родственным молекулой бета-аланином и с кольцевым тауриновым аналогом P4S, в частично закрытой и более открытой внутрь ориентированной формах.
Как таурин помещается в свою индивидуальную карман
Структуры показывают, что таурин располагается в центральном кармане глубоко внутри транспортера, окружённом несколькими спиралями, пронизывающими мембрану. Таурин имеет отрицательно заряженную сульфонатную группу на одном конце и положительно заряженную аминогруппу на другом, соединённые короткой углеродной цепочкой. Транспортер имеет небольшую нишу, богатую глицином, которая охватывает громоздкую сульфонатную группу и закрепляет её сетью водородных связей и координированным ионом натрия. Углеродная цепочка располагается в гидрофобной области, а аминогруппа тянется к отрицательно заряженному остатку, образующему стабилизирующий ионный мост. Именно такая тонкая настройка объясняет, почему транспортер явно предпочитает таурин другим похожим молекулам и как небольшие изменения в ключевых остатках могут ослабить транспорт.
Импостеры и их блокирование или проезд через насос
Бета-аланин, природное соединение с карбоксильной группой вместо сульфоната таурина, связывается почти таким же образом, используя тот же карман, ионы натрия и точки контакта. Однако он образует меньше водородных связей, что согласуется с его несколько более слабым сродством к транспортеру. P4S, синтетический кольцевой аналог таурина, также вставляет свою сульфонатную группу в ту же нишу и занимает сайт таурина, но его жёсткое кольцо не выравнивает аминогруппу должным образом с ключевым кислотным остатком. Это несоответствие нарушает одно из сильнейших взаимодействий и делает P4S блокером с более низким сродством. Поскольку все три молекулы конкурируют за один и тот же сайт, захват таурина может замедляться при высоких концентрациях бета-аланина или P4S.
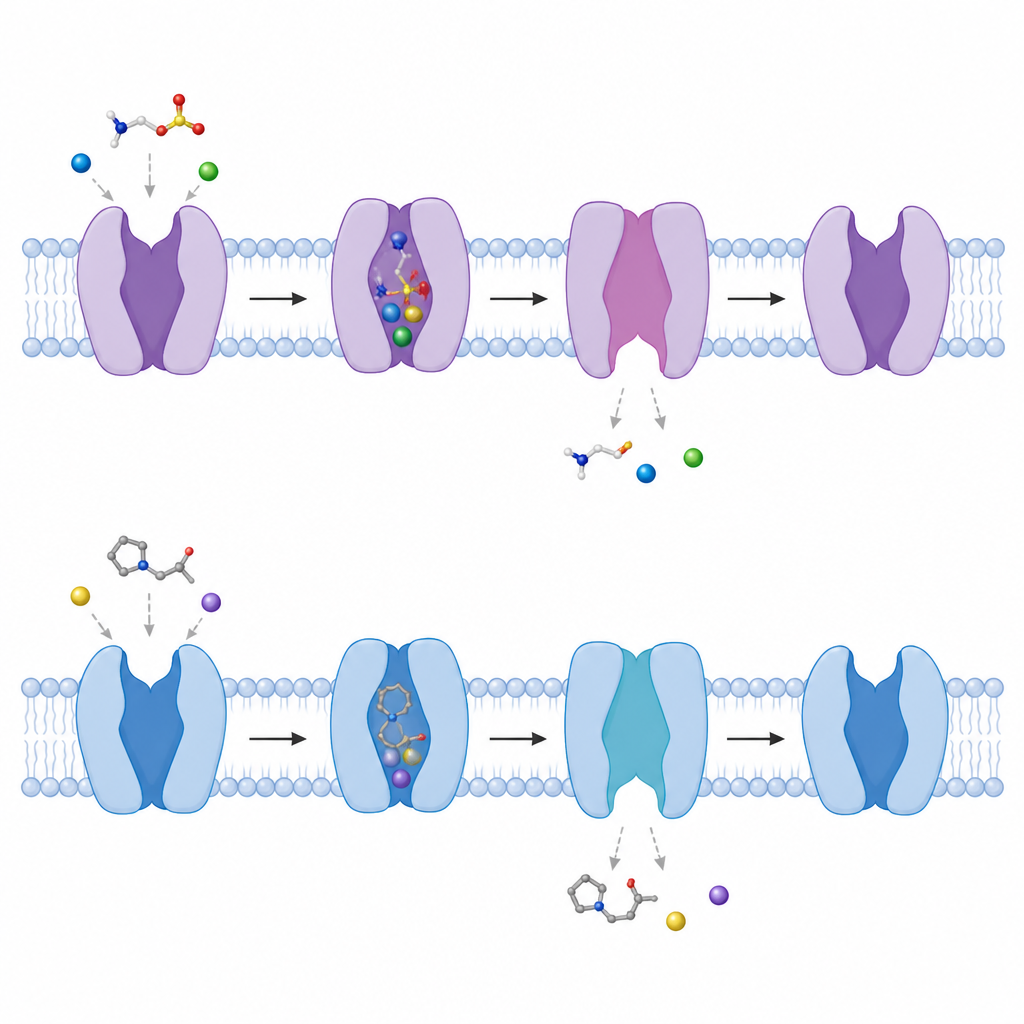
Наблюдение за раскрытием ворот внутрь клетки
Сравнивая структуры с связанными молекулами и без них, авторы проследили, как транспортер переключается между конформациями. Небольшой спиральный сегмент рядом с внутренней стороной мембраны выгибается наружу примерно на 50 градусов, а другая спираль частично разматывается, создавая туннель от центрального кармана к внутренней части клетки. По мере этого тщательно устроенные сайты связывания натрия разрушаются, что облегчает сначала выход натрия, а затем и таурина в цитозоль. Команда также показала, что в отсутствие связанных молекул транспортер естественно колеблется между более закрытыми и более открытыми внутрь формами, намекая на постоянно меняющийся ландшафт, который позволяет ему быстро реагировать на появление таурина.
Переосмысление ингибитора и перспективы для лекарств
Удивительно, но функциональные тесты показали, что P4S — это не просто заглушка, блокирующая ворота. Напротив, он может переноситься через транспортер подобно самому таурину, приводимый в движение тем же градиентом натрия, и даже вызывать высвобождение предварительно загруженного таурина из клеток. Иными словами, P4S ведёт себя как транспортируемый аналог субстрата, который конкурирует с таурином. В совокупности структурные снимки и измерения транспорта описывают полный рабочий цикл тауринового транспортера и точно определяют карманы и движения, управляющие каждым шагом. Для неспециалистов это означает, что у исследователей теперь есть детальная схема для проектирования новых молекул, которые либо более эффективно доставляют таурин, либо селективно замедляют его захват при заболеваниях, таких как рак, где клетки зависят от чрезмерного транспорта таурина.
Цитирование: Qi, Y., Zhang, Y., Wang, D. et al. Structural mechanism of substrate binding and inhibition of human taurine transporter. Nat Commun 17, 4257 (2026). https://doi.org/10.1038/s41467-026-70772-x
Ключевые слова: тауриновый транспортер, трансмембранный транспорт, криоэлектронная микроскопия, нейрокардиальное здоровье, дизайн лекарств