Clear Sky Science · de
Struktureller Mechanismus der Substratbindung und Hemmung des menschlichen Taurintransporters
Warum diese winzige Nährstoffpumpe wichtig ist
Taurin ist ein kleines Molekül, das im gesamten menschlichen Körper vorkommt und dazu beiträgt, dass Herz, Gehirn, Augen und Muskeln richtig funktionieren. Unsere Zellen können sich nicht auf passive Diffusion verlassen, um genügend Taurin zu erhalten; stattdessen nutzen sie ein spezialisiertes Tor in der Zellmembran, den Taurintransporter. Wenn dieser Transporter gestört ist, steht das im Zusammenhang mit Herzkrankheiten, Nervenschäden, Sehverlust und Krebs. Diese Studie zeigt auf atomarer Ebene, wie der menschliche Taurintransporter Taurin erfasst, in die Zelle befördert und durch wirkstoffähnliche Moleküle blockiert oder gekapert werden kann und liefert damit Hinweise für künftige Therapien.
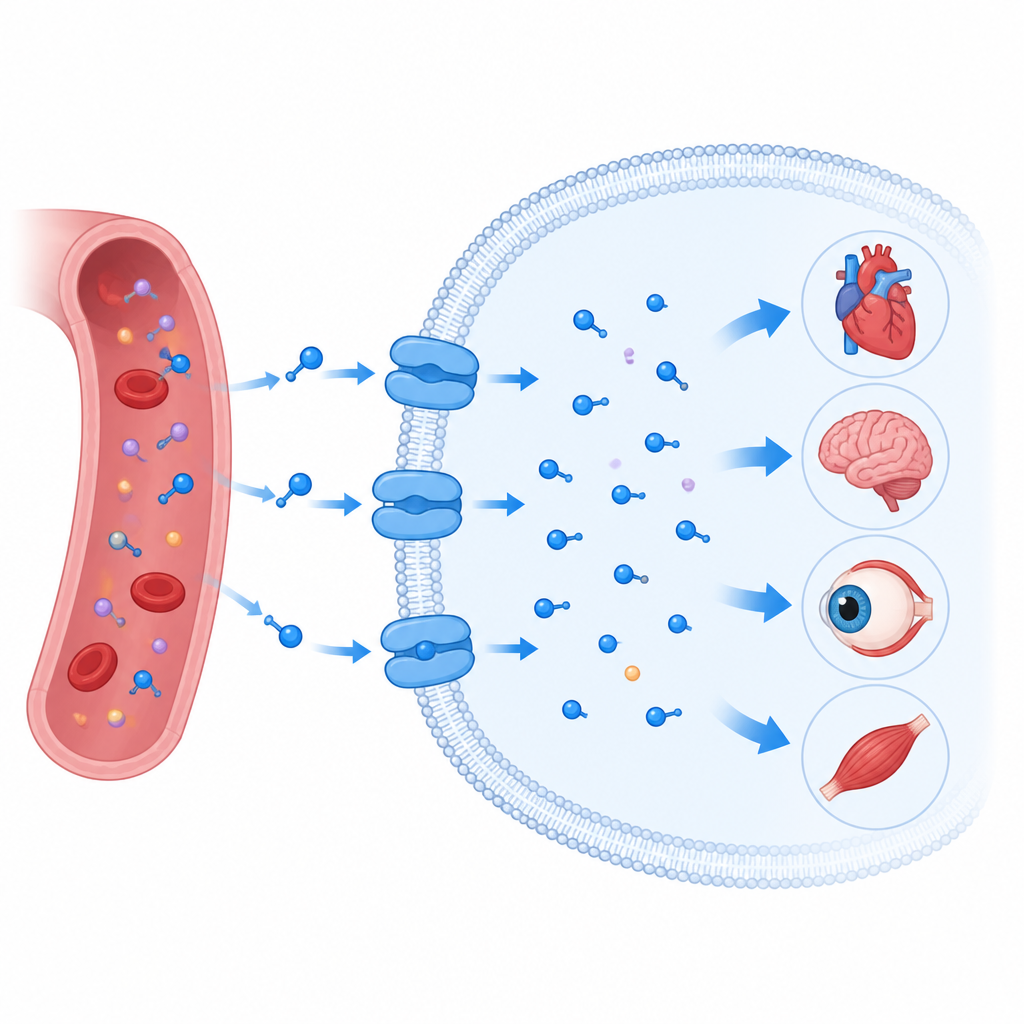
Ein Tor, das Taurin in die Zelle zieht
Der Taurintransporter sitzt in der lipophilen Membran, die jede Zelle umgibt, und gehört zu einer großen Familie von Transportproteinen, die auch Neurotransmitter wie Serotonin und Dopamin bewegen. Wie seine Verwandten bildet er keinen offenen Kanal. Stattdessen funktioniert er eher wie eine Drehschleuse: Er öffnet sich zu einer Seite der Membran, schließt sich um seine Fracht und öffnet sich dann zur anderen Seite. Die Forscher nutzten Kryo‑Elektronenmikroskopie, um mehrere dreidimensionale Momentaufnahmen des menschlichen Taurintransporters in Aktion zu bestimmen. Sie hielten ihn leer fest, gebunden an Taurin, gebunden an das verwandte Molekül Beta‑Alanine und gebunden an ein ringförmiges Taurin‑Mimikrum namens P4S, in sowohl teilweise geschlossenen als auch weiter geöffneten nach innen gerichteten Zuständen.
Wie Taurin in seine maßgeschneiderte Tasche passt
Die Strukturen zeigen, dass Taurin in eine zentrale Tasche tief im Inneren des Transporters dockt, umgeben von mehreren membranüberspannenden Helices. Taurin besitzt an einem Ende eine negativ geladene Sulfonatgruppe und am anderen Ende eine positiv geladene Aminogruppe, verbunden durch eine kurze Kohlenstoffkette. Der Transporter verfügt über eine kleine, glycinreiche Nische, die die voluminöse Sulfonatgruppe umschließt und sie durch ein Netz von Wasserstoffbrücken und ein koordiniertes Natriumion verankert. Die Kohlenstoffkette liegt in einer fettigen (hydrophoben) Zone, während das Aminoende ein negativ geladenes Rest erreicht, das eine stabilisierende Salzbrücke ausbildet. Diese fein abgestimmte Anordnung erklärt, warum der Transporter Taurin stark gegenüber anderen ähnlichen Molekülen bevorzugt und wie kleine Veränderungen in Schlüsselresten den Transport schwächen können.
Imitator‑Moleküle und wie sie die Pumpe blockieren oder mitfahren
Beta‑Alanine, eine natürliche Verbindung mit einer Carboxylgruppe statt der Sulfonatgruppe von Taurin, bindet fast auf die gleiche Weise, nutzt dieselbe Tasche, Natriumionen und Kontaktpunkte. Allerdings bildet es weniger Wasserstoffbrücken, was seiner etwas schwächeren Affinität zum Transporter entspricht. P4S, ein synthetisches, ringförmiges Taurinanalogon, drückt seine Sulfonatgruppe ebenfalls in dieselbe Nische und besetzt die Taurin‑Position, aber sein starres Ringgerüst richtet die Aminogruppe nicht richtig gegenüber dem wichtigen sauren Rest aus. Diese Fehlanpassung stört eine der stärksten Wechselwirkungen und macht P4S zu einem Bindungshemmer mit niedrigerer Affinität. Weil alle drei Moleküle um dieselbe Stelle konkurrieren, kann die Taurinaufnahme verlangsamt werden, wenn Beta‑Alanine oder P4S in hohen Konzentrationen vorhanden sind.
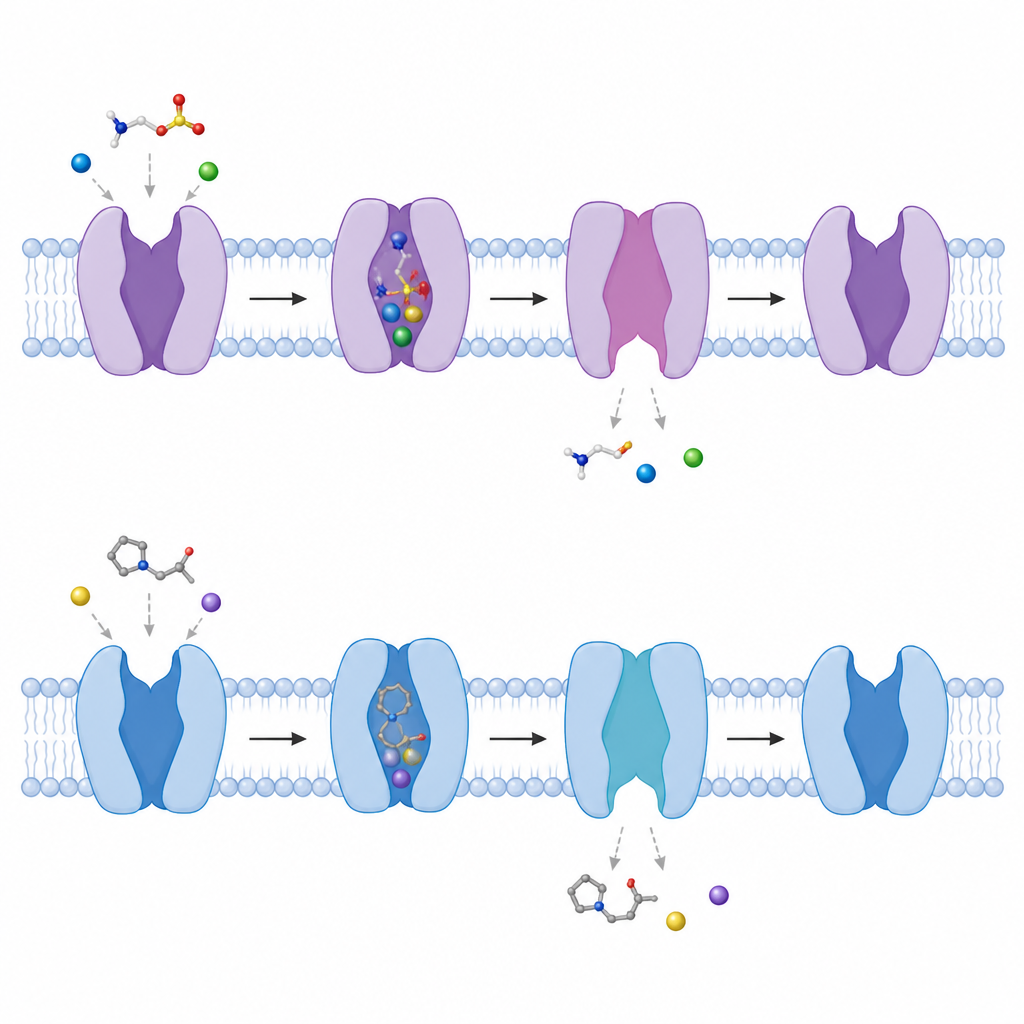
Das Aufschwingen des Tores nach innen beobachten
Durch den Vergleich der Strukturen mit und ohne gebundene Moleküle verfolgten die Autoren, wie der Transporter zwischen Konformationen umschaltet. Ein kurzes Helixsegment in der Nähe der inneren Membranseite biegt sich nach außen um etwa 50 Grad, und eine andere Helix windet sich teilweise auf, wodurch ein Tunnel von der zentralen Tasche zur Zellinnenseite entsteht. Während dieses Vorgangs lösen sich die sorgfältig angeordneten Natrium‑Bindestellen auf, was es Natrium und anschließend Taurin erleichtert, in das Zellinnere freigesetzt zu werden. Das Team zeigte außerdem, dass der Transporter in Abwesenheit gebundener Moleküle von Natur aus zwischen eher geschlosseneren und offeneren nach innen gerichteten Formen wechselt, was auf eine ständig wechselnde Landschaft hindeutet, die ihm erlaubt, schnell zu reagieren, wenn Taurin verfügbar wird.
Ein Hemmstoff neu definieren und Ausblick auf Medikamente
Überraschenderweise zeigten funktionelle Tests, dass P4S kein einfacher Pfropfen ist, der das Tor blockiert. Stattdessen kann es ähnlich wie Taurin durch den Transporter bewegt werden, angetrieben vom gleichen Natriumgradienten, und sogar die Freisetzung von vorbeladenem Taurin aus Zellen auslösen. Mit anderen Worten verhält sich P4S wie ein transportiertes Substratanalogon, das mit Taurin konkurriert. Zusammen zeichnen die strukturellen Momentaufnahmen und Transportmessungen einen vollständigen Arbeitszyklus für den Taurintransporter nach und identifizieren die spezifischen Taschen und Bewegungen, die jeden Schritt steuern. Für Nicht‑Spezialisten bedeutet das: Forschern liegt nun ein detaillierter Bauplan vor, um neue Moleküle zu entwerfen, die entweder Taurin effektiver liefern oder dessen Aufnahme in Krankheiten wie Krebs selektiv verlangsamen, wo Zellen auf übermäßigen Taurintransport angewiesen sind.
Zitation: Qi, Y., Zhang, Y., Wang, D. et al. Structural mechanism of substrate binding and inhibition of human taurine transporter. Nat Commun 17, 4257 (2026). https://doi.org/10.1038/s41467-026-70772-x
Schlüsselwörter: Taurintransporter, Membrantransport, Cryo‑Elektronenmikroskopie, Neurokardiale Gesundheit, Arzneimittelentwicklung