Clear Sky Science · he
מנגנון מבני של קשירת המצע ועיכוב של נשא הטאורין האנושי
למה המשאבה המיקרוסקופית הזו חשובה
טאורין הוא מולקולה קטנה הנמצאת בכל חלקי הגוף האנושי, ושומרת על תפקוד תקין של הלב, המוח, העיניים והשרירים. תאים אינם יכולים לסמוך על דיפוזיה פסיבית כדי לקבל כמות מספקת של טאורין; במקום זאת הם משתמשים בשער מיוחד בממברנת התא שנקרא נשא הטאורין. כשנשא זה תקול, הוא מקושר למחלות לב, בעיות עצביות, אובדן ראייה וסרטן. המחקר הזה חושף, ברזולוציה אטומית, כיצד נשא הטאורין האנושי תופס טאורין, מעביר אותו לתוך התאים, וכיצד ניתן לחסום או לחטוף אותו על ידי מולקולות דמוי‑תרופה, ומציע רמזים לטיפולים עתידיים.
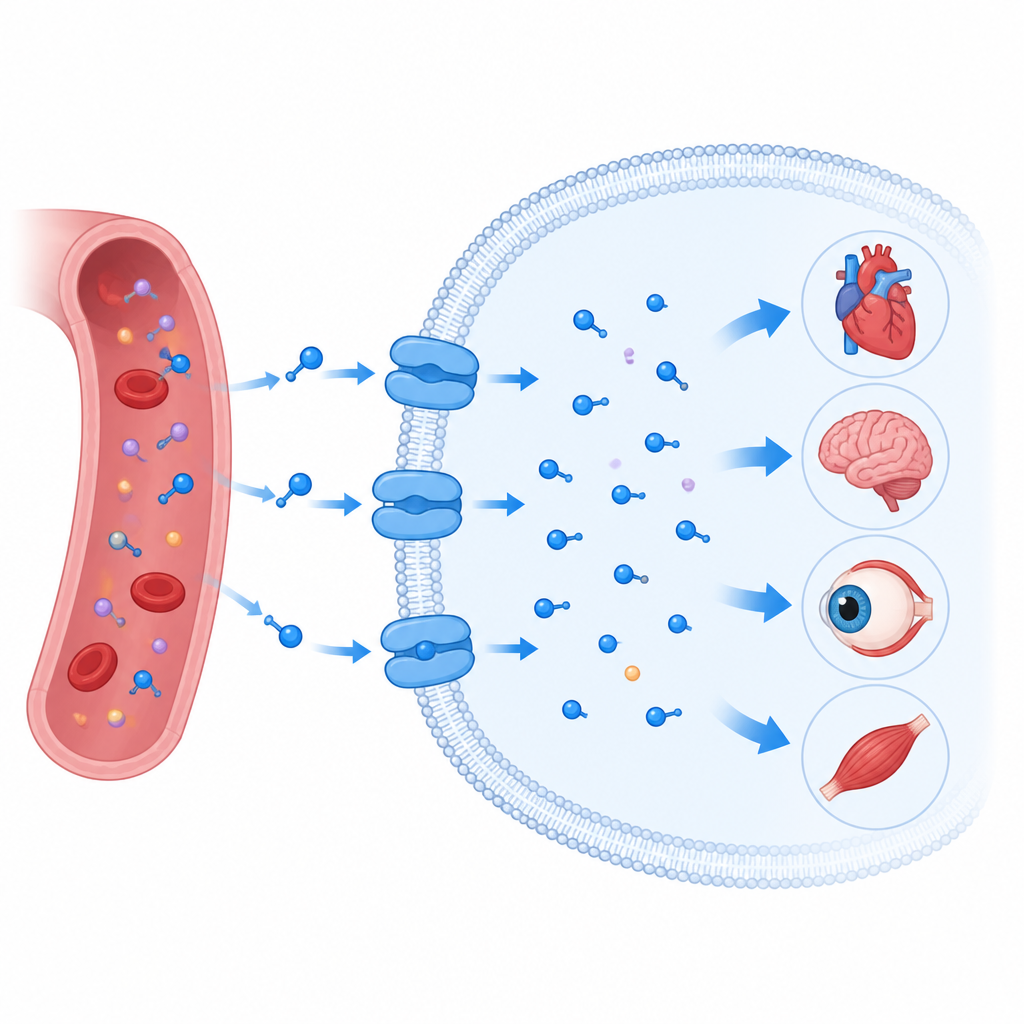
שער שמושך טאורין לתוך התאים
נשא הטאורין יושב בממברנה השומנית שמקיפה כל תא והוא שייך למשפחה רחבה של חלבוני נשא שכוללת גם נשאים שמעבירים מוליכים עצביים כגון סרוטונין ודופמין. כמו קרוביו, הוא לא יוצר פשוט תעלה פתוחה. במקום זאת הוא פועל יותר כמו דלת מסתובבת: נפתח לצד אחד של הממברנה, נסגר סביב המטען, ואז נפתח לצד השני. החוקרים השתמשו במיקרוסקופיה אלקטרונית בקירור כדי לקבוע מספר תמונות תלת־ממדיות של נשא הטאורין האנושי בפעולה. הם תפסו אותו ריק, קשור לטאורין, קשור למולקולה קרובה בשם בטא‑אלנין, וקשור למחקה טאורין בעל צורת טבעת הידוע כ‑P4S, בצורות פנימיות חלקית סגורות וביותר פתוחות.
כיצד טאורין מתיישב בכיס המותאם לו
המבנים מראים שטאורין מתחבר בכיס מרכזי עמוק בתוך הנשא, מוקף במספר סלילי ממברנה עוקפים. לטאורין יש קבוצת סולפונאט שלילית בקצה אחד וקבוצת אמינו חיובית בקצה האחר, המקושרות על ידי שרשרת פחמנית קצרה. לנשא יש שקע קטן עשיר בגליצין שמחבק את קבוצת הסולפונאט הקטנה ומעגן אותה דרך רשת של קשרי מימן ויון נתרן מתואם. שרשרת הפחמן מתמקמת בתכתש שומני, בעוד קצה האמינו מגיע שומרש לשריד חומצי מטען שמייצר גשר מלח מייצב. הסידור המכוון בקפידה הזה מסביר מדוע הנשא מעדיף מאוד טאורין על פני מולקולות דומות וכיצד שינויים קטנים ברצפים מרכזיים יכולים להחליש את ההובלה.
מולקולות מתחזות וכיצד הן חוסמות או נוסעות במשאבה
בטא‑אלנין, תרכובת טבעית שיש לה קבוצת קרבוקסיל במקום הסולפונאט של הטאורין, נקשרת כמעט באותו אופן, משתמשת באותו הכיס, באתרי נתרן ונקודות מגע זהות. עם זאת, היא יוצרת פחות קשרי מימן, מה שתואם לאפיליה החזקה פחותה שלה לנשא. P4S, אנלוג סינתטי בצורת טבעת של טאורין, גם הוא דוחף את קבוצת הסולפונאט שלו לאותו שיק וממלא את אתר הטאורין, אך הטבעת הנוקשה לא מצרפת את קבוצת האמינו שלו כהלכה למולקולה החומצית המרכזית. חוסר ההתאמה הזה משבש אחת מהאינטראקציות החזקות והופך את P4S לחוסם בעל אפיניות נמוכה יותר. מאחר ששלוש המולקולות מתחרות על אותו אתר, קליטה של טאורין יכולה להאט כאשר רמות גבוהות של בטא‑אלנין או P4S נוכחות.
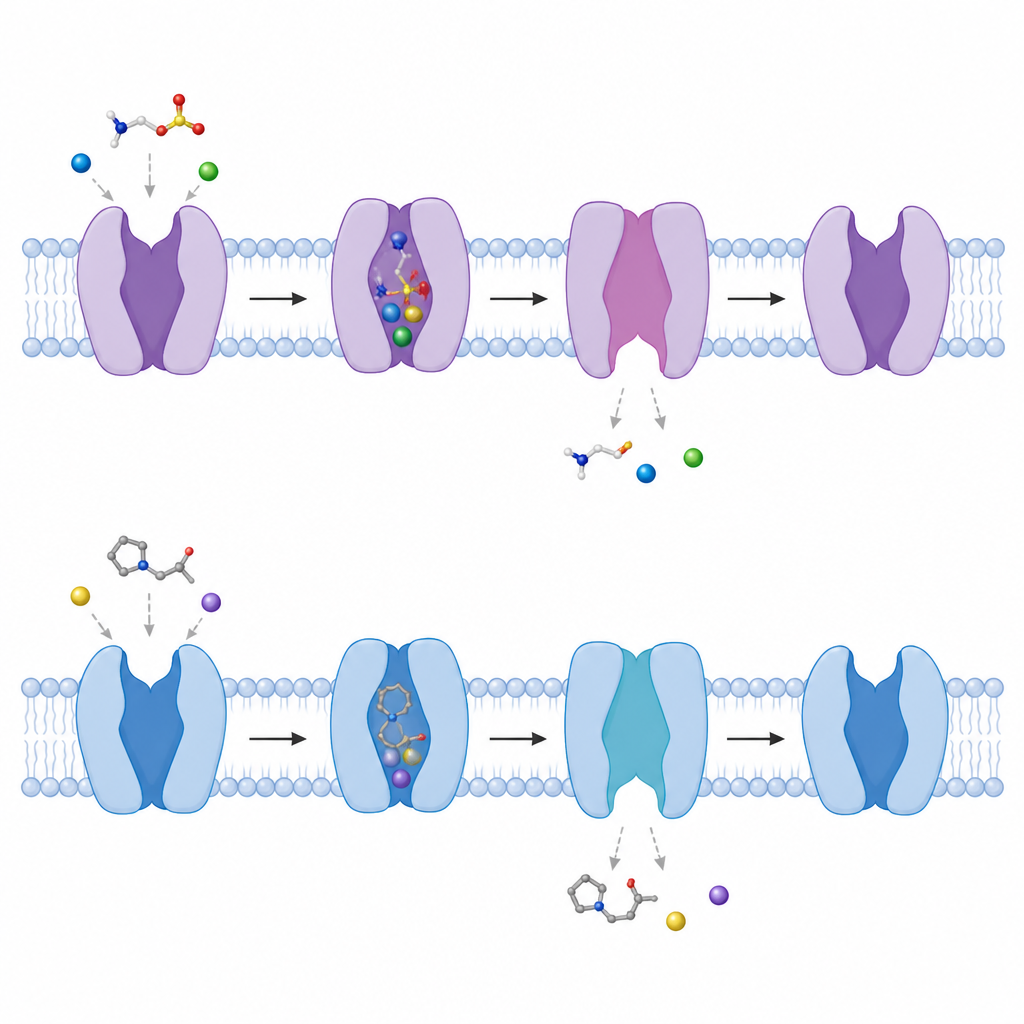
צפייה בפתיחת השער כלפי תוך התא
בהשוואת מבנים עם ובלי מולקולות קשורות, המחברים עקבו כיצד הנשא מתנדנד בין קונפורמציות. קטע אלפא‑הליקס קצר בקרבת צד פנימי של הממברנה מתכופף החוצה בכ־50 מעלות, ולעתים הליקס השני מתפרק חלקית, ויוצר תעלה מהכיס המרכזי אל תוך התא. בזמן שזה קורה, אתרי קשירת הנתרן המסודרים בקפידה מתפרקים, מה שמקל על שחרור הנתרן ורק אחריו הטאורין לתוך פנים התא. הצוות גם הראה כי בהיעדר כל מולקולה קשורה הנשא באופן טבעי מהפך בין צורות פנימיות סגורות ופתוחות יותר, מרמז על נוף קונפורמטיבי משתנה המאפשר תגובה מהירה כאשר טאורין מופיע.
הגדרת מחודש של מעכב והסתכלות לעבר תרופות
בהפתעה, בדיקות פונקציונליות הראו כי P4S אינו רק מעצור פשוט שתקע את השער. במקום זאת, הוא יכול לעבור דרך הנשא כמו הטאורין עצמו, מונע על‑ידי אותו מפל הנתרן, ואף לגרום לשחרור טאורין שהוטען מראש מתוך תאים. במילים אחרות, P4S מתנהג כאנלוג מצע שמועבר ומתחרה בטאורין. יחד, הצילומים המבניים ומדידות ההובלה מסמנות מחזור עבודה מלא לנשא הטאורין ומצביעות על הכיסים והתנועות הספציפיים ששולטים בכל שלב. עבור קהל שאינו מומחה, המשמעות היא שלחוקרים כעת יש תכנית מפורטת לעיצוב מולקולות חדשות שיספקו טאורין ביעילות רבה יותר או ירפו במדויק את קליטתו במחלות כמו סרטן, שם תאים מסתמכים על הובלה מופרזת של טאורין.
ציטוט: Qi, Y., Zhang, Y., Wang, D. et al. Structural mechanism of substrate binding and inhibition of human taurine transporter. Nat Commun 17, 4257 (2026). https://doi.org/10.1038/s41467-026-70772-x
מילות מפתח: נשא טאורין, מעבר דרך ממברנה, מיקרוסקופיה אלקטרונית בקירור, בריאות נוירוקרדיאלית, תכנון תרופות