Clear Sky Science · pl
Mechanizm strukturalny wiązania substratu i hamowania ludzkiego transportera tauryny
Dlaczego ta niewielka pompa odżywcza ma znaczenie
Tauryna to mała cząsteczka występująca w całym organizmie człowieka, która pomaga utrzymać prawidłowe funkcjonowanie serca, mózgu, oczu i mięśni. Nasze komórki nie mogą polegać wyłącznie na dyfuzji biernej, by uzyskać wystarczające ilości tauryny; zamiast tego wykorzystują wyspecjalizowaną bramkę w błonie komórkowej zwaną transporterem tauryny. Gdy ten transporter działa nieprawidłowo, wiąże się to z chorobami serca, zaburzeniami nerwowymi, utratą wzroku i nowotworami. To badanie ujawnia, w skali atomowej, jak ludzki transporter tauryny chwyta taurynę, przenosi ją do wnętrza komórek i jak może być blokowany lub wykorzystany przez molekuły przypominające leki, dając wskazówki do przyszłych terapii.
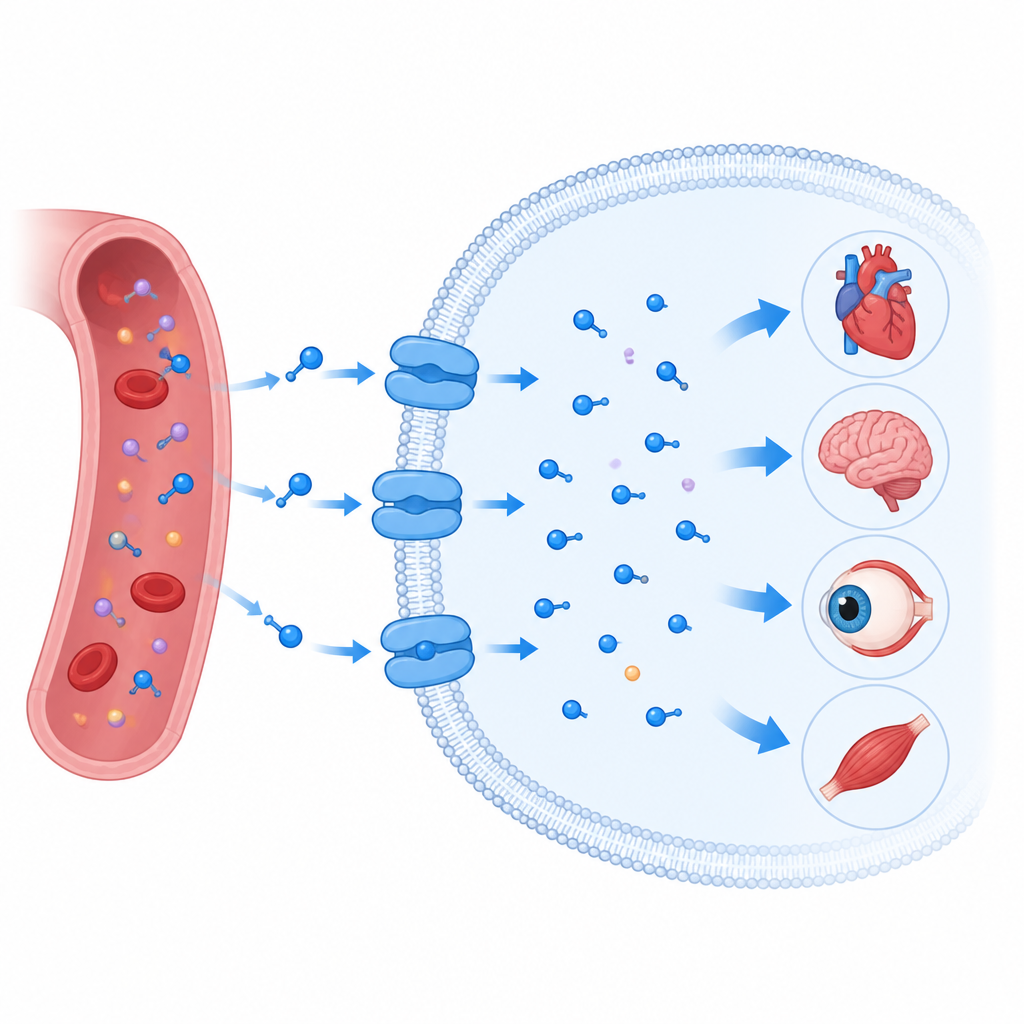
Bramka, która wciąga taurynę do komórek
Transporter tauryny osadza się w lipidowej błonie otaczającej każdą komórkę i należy do rozległej rodziny białek transportowych, które przenoszą także przekaźniki mózgowe, takie jak serotonina i dopamina. Podobnie jak jego krewni, nie tworzy po prostu otwartego kanału. Działa raczej jak obracające się drzwi: otwiera się na jedną stronę błony, zamyka wokół ładunku, a następnie otwiera na drugą stronę. Badacze wykorzystali kriomikroskopię elektronową, aby określić wiele trójwymiarowych migawkowych obrazów ludzkiego transportera tauryny w akcji. Utrwalili jego stan pusty, związany z tauryną, związany z pokrewną cząsteczką zwaną beta-alaniną oraz związany z pierścieniowym naśladowcą tauryny znanym jako P4S, zarówno w formach częściowo zamkniętych, jak i bardziej otwartych, zwróconych do wnętrza komórki.
Jak tauryna mieści się w swojej dopasowanej kieszeni
Struktury pokazują, że tauryna zakotwicza się w centralnej kieszeni głęboko wewnątrz transportera, otoczonej kilkoma helisami przecinającymi błonę. Tauryna ma na jednym końcu ujemnie naładowaną grupę sulfonianową, a na drugim dodatnio naładowaną grupę aminową, połączone krótkim łańcuchem węglowym. Transporter posiada niewielką, bogatą w glicynę niszę, która mieści masywną grupę sulfonianową i stabilizuje ją siecią wiązań wodorowych oraz skoordynowanym jonem sodu. Łańcuch węglowy układa się w tłustej kieszeni, podczas gdy koniec aminowy sięga do ujemnie naładowanego resztu, tworząc stabilizujący mostek solny. Ta precyzyjnie dobrana aranżacja tłumaczy, dlaczego transporter wyraźnie preferuje taurynę nad innymi podobnymi cząsteczkami i jak drobne zmiany w kluczowych resztach mogą osłabić transport.
Podróbki molekularne i jak blokują albo korzystają z pompy
Beta-alanina, naturalny związek z grupą karboksylową zamiast sulfonianowej jak w taurynie, wiąże się w prawie taki sam sposób, wykorzystując tę samą kieszeń, jony sodu i punkty kontaktowe. Jednak tworzy mniej wiązań wodorowych, co odpowiada jej nieco słabszemu powinowactwu do transportera. P4S, syntetyczny, pierścieniowy analog tauryny, także wciska swoją grupę sulfonianową w tę samą niszę i zajmuje miejsce tauryny, lecz jego sztywny pierścień nie ustawia właściwie grupy aminowej względem kluczowej kwaśnej reszty. To niedopasowanie zaburza jedno z najsilniejszych oddziaływań i czyni P4S inhibitorem o niższym powinowactwie. Ponieważ wszystkie trzy cząsteczki konkurują o to samo miejsce, pobieranie tauryny może być spowolnione, gdy beta-alanina lub P4S występują w wysokich stężeniach.
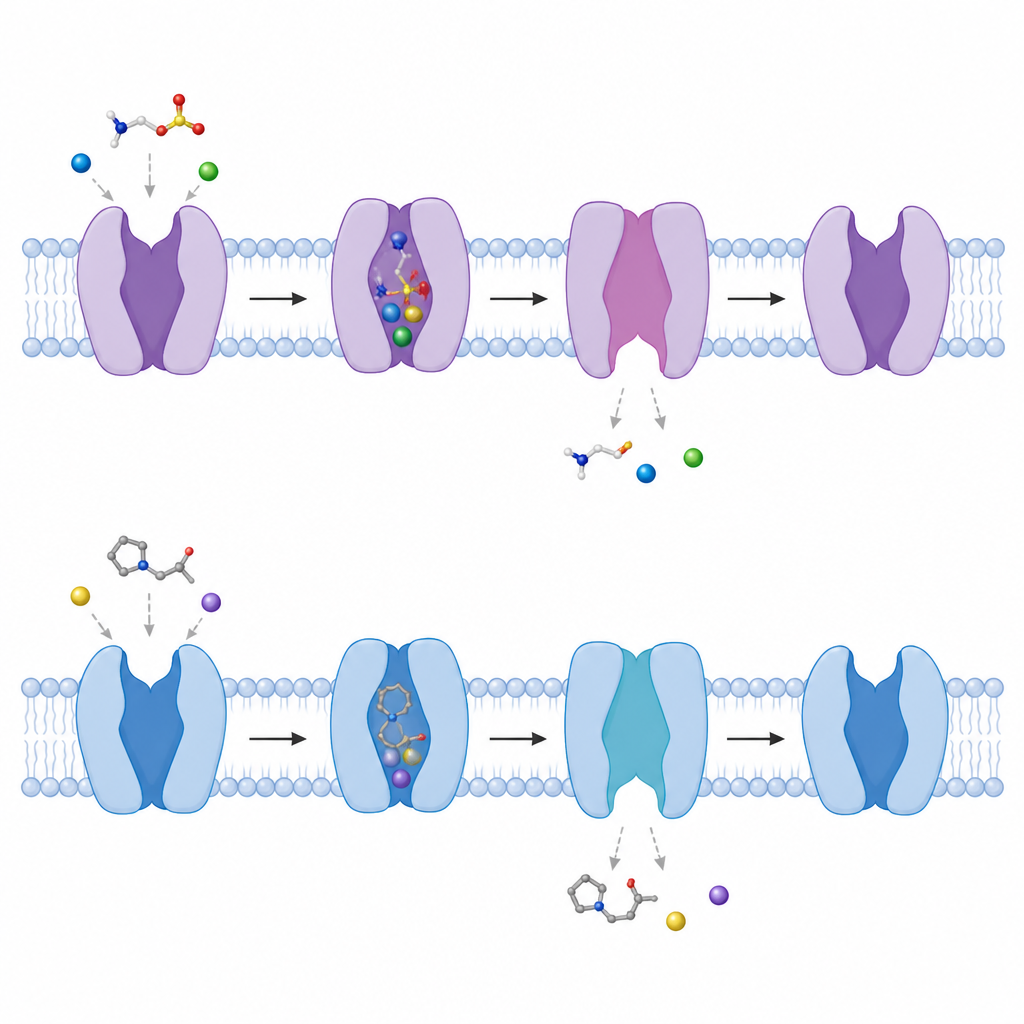
Obserwowanie, jak bramka otwiera się do wnętrza komórki
Porównując struktury związanego i niezwiązanego białka, autorzy śledzili, jak transporter przełącza się między konformacjami. Krótki segment helikalny blisko wewnętrznej strony błony zgina się na zewnątrz o około 50 stopni, a inna helisa częściowo się rozwija, tworząc tunel z centralnej kieszeni do wnętrza komórki. W miarę zachodzenia tych zmian, starannie rozmieszczone miejsca wiązania sodu rozpadają się, ułatwiając uwolnienie najpierw sodu, a następnie tauryny do wnętrza komórki. Zespół wykazał także, że w braku związanych cząsteczek transporter naturalnie przechodzi między bardziej zamkniętymi i bardziej otwartymi formami, zwróconymi do wnętrza, co sugeruje nieustannie zmieniający się krajobraz umożliwiający szybkie reagowanie, gdy pojawi się tauryna.
Przewartościowanie inhibitora i perspektywy dla leków
Zaskakująco, testy funkcjonalne wykazały, że P4S nie jest jedynie prostym korkiem zatykającym bramkę. Zamiast tego może być przemieszczany przez transporter podobnie jak sama tauryna, napędzany tym samym gradientem sodowym, a nawet może wyzwalać uwolnienie wcześniej załadowanej tauryny z komórek. Innymi słowy, P4S zachowuje się jak transportowany analog substratu, który konkuruje z tauryną. Razem, migawki strukturalne i pomiary transportu opisują pełny cykl pracy transportera tauryny i precyzyjnie wskazują kieszenie oraz ruchy kontrolujące każdy etap. Dla osób niebędących specjalistami oznacza to, że badacze dysponują teraz szczegółowym planem do projektowania nowych cząsteczek, które albo skuteczniej dostarczą taurynę, albo selektywnie spowolnią jej pobieranie w chorobach takich jak nowotwory, gdzie komórki polegają na nadmiernym transporcie tauryny.
Cytowanie: Qi, Y., Zhang, Y., Wang, D. et al. Structural mechanism of substrate binding and inhibition of human taurine transporter. Nat Commun 17, 4257 (2026). https://doi.org/10.1038/s41467-026-70772-x
Słowa kluczowe: transporter tauryny, transport przez błonę, kriomikroskopia elektronowa, zdrowie neurokardiologiczne, projektowanie leków