Clear Sky Science · sv
Strukturell mekanism för substratbindning och hämning av den humana taurintransportören
Varför denna lilla näringspump spelar roll
Taurin är en liten molekyl som finns överallt i människokroppen och som hjälper till att hålla hjärta, hjärna, ögon och muskler i gott skick. Våra celler kan inte förlita sig på passiv diffusion för att få tillräckligt med taurin; i stället använder de en specialiserad port i cellmembranet kallad taurintransportören. När denna transportör fungerar felkopplat kopplas det till hjärtsjukdom, nervproblem, synförlust och cancer. Denna studie avslöjar, i atomär detalj, hur den humana taurintransportören griper taurin, för in den i celler och kan blockeras eller kapras av läkemedelslika molekyler, vilket ger ledtrådar för framtida terapier.
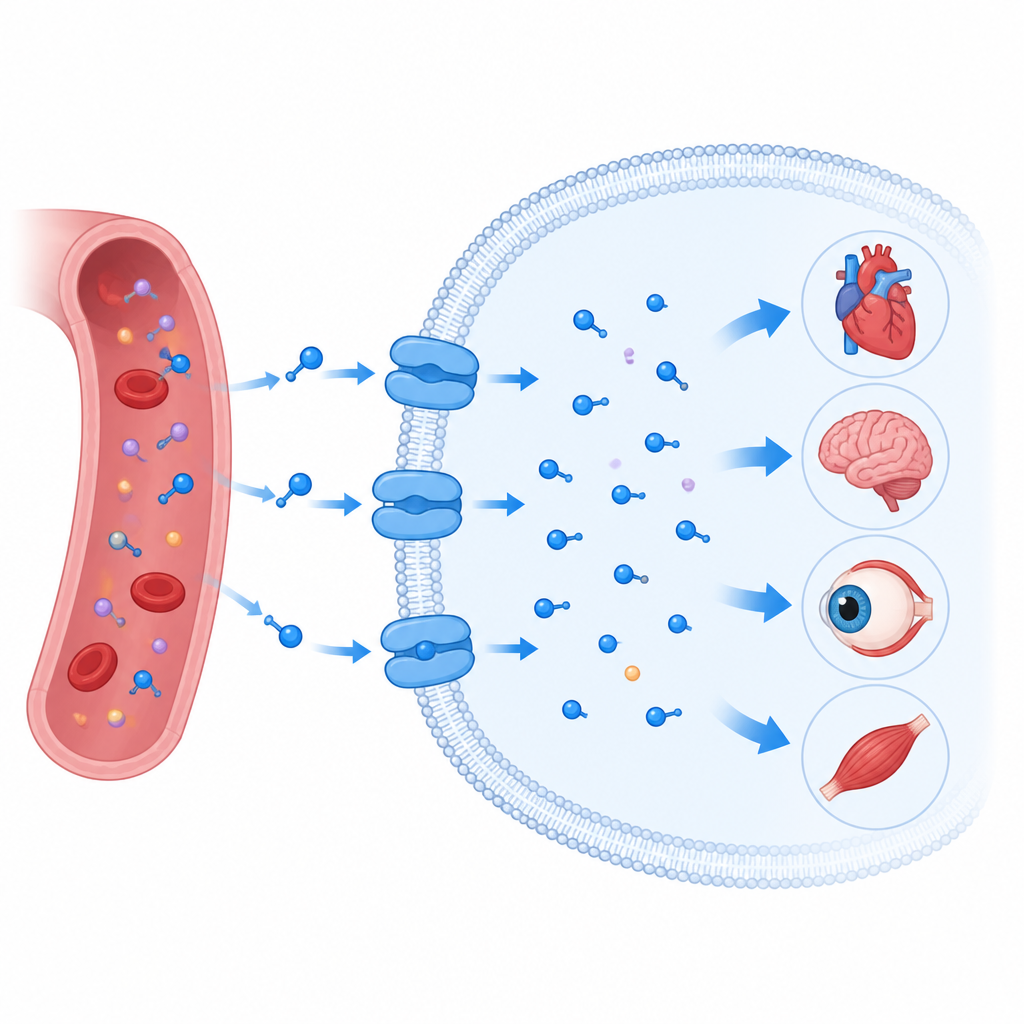
En port som drar in taurin i cellerna
Taurintransportören sitter i det oljeartade membranet som omger varje cell och tillhör en stor familj av transportproteiner som också förflyttar hjärnans budbärare som serotonin och dopamin. Likt sina släktingar bildar den inte bara en öppen kanal. Istället fungerar den mer som en snurrdörr: den öppnar åt ena sidan av membranet, sluter sig runt lasten och öppnar sedan åt andra sidan. Forskarlaget använde kryoelektronmikroskopi för att bestämma flera tredimensionella ögonblicksbilder av den humana taurintransportören i arbete. De fångade den tom, bunden till taurin, bunden till en närbesläktad molekyl kallad beta-alanin, och bunden till en ringformad taurinsimilar känd som P4S, i både delvis stängda och mer öppna inåtvända former.
Hur taurin passar i sin skräddarsydda ficka
Strukturerna visar att taurin lägger sig i en central ficka djupt inne i transportören, omgiven av flera membrangenomgående helixar. Taurin har en negativt laddad sulfonatgrupp i ena änden och en positivt laddad aminogrupp i andra, kopplade via en kort kolkedja. Transportören har en liten, glycinrik nisch som vilar den stora sulfonatgruppen och förankrar den genom ett nätverk av vätebindningar och en koordinerad natriumjon. Kolkedjan vilar i ett fettrikt parti, medan aminosidan når en negativt laddad rest som bildar en stabiliserande saltbrygga. Denna fint avvägda ordning förklarar varför transportören starkt föredrar taurin framför andra liknande molekyler och hur små förändringar i nyckelrester kan försvaga transporten.
Impostörmolekyler och hur de blockerar eller åker med pumpen
Beta-alanin, en naturlig förening med en karboxylgrupp istället för taurins sulfonat, binder på i stort sett samma sätt och utnyttjar samma ficka, natriumjoner och kontaktpunkter. Den bildar dock färre vätebindningar, vilket motsvarar dess något svagare affinitet för transportören. P4S, en syntetisk ringformad taurinanalog, trycker också sin sulfonatgrupp in i samma nisch och ockuperar taurinsite, men dess styva ring ställer inte in aminogruppen korrekt mot den viktiga sura residyn. Denna felpassning stör en av de starkaste interaktionerna och gör P4S till en lägre affinitetsblockerare. Eftersom alla tre molekyler konkurrerar om samma site kan taurinupptaget bromsas när beta-alanin eller P4S finns i höga nivåer.
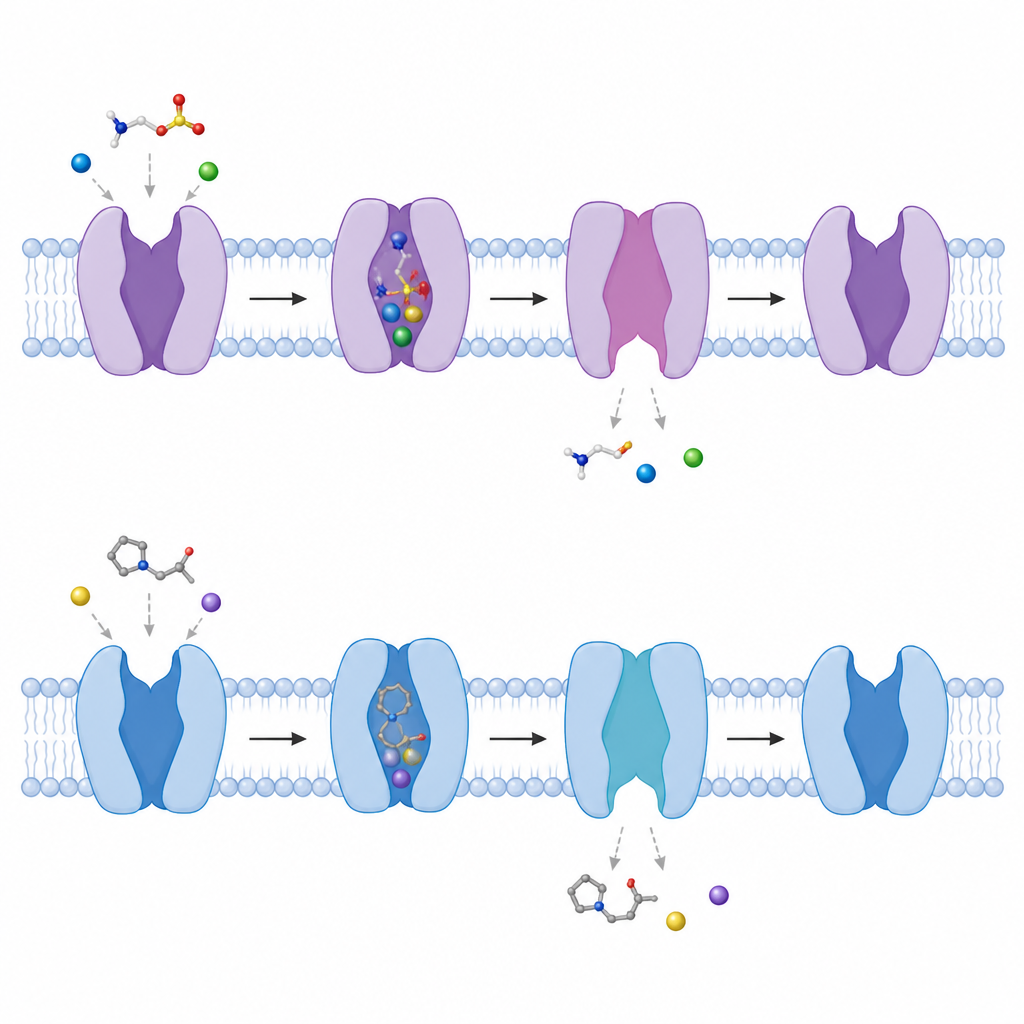
Att se porten svänga uppåt inuti cellen
Genom att jämföra strukturer med och utan bundna molekyler följde författarna hur transportören växlar mellan konformationer. Ett kort helixavsnitt nära den inre sidan av membranet böjer sig utåt med ungefär 50 grader, och en annan helix delvis vecklas upp, vilket skapar en tunnel från den centrala fickan till cellens insida. När detta sker faller de noggrant ordnade natriumbindningsställena isär, vilket gör det lättare för natrium och sedan taurin att frigöras i cellens inre. Teamet visade också att i frånvaro av bundna molekyler växlar transportören naturligt mellan mer slutna och mer öppna inåtvända former, vilket antyder ett ständigt föränderligt landskap som gör att den snabbt kan svara när taurin dyker upp.
Omdaning av en hämmare och blick mot läkemedel
Överraskande nog visade funktionella tester att P4S inte bara är en enkel stoppkloss som slår igen porten. I stället kan det förflyttas genom transportören likt taurin själv, drivet av samma natriumgradient, och till och med utlösa utsläpp av förladdad taurin från celler. Med andra ord beter sig P4S som en transporterad substratanalog som råkar konkurrera med taurin. Tillsammans skisserar de strukturella ögonblicksbilderna och transportmätningarna en fullständig arbetscykel för taurintransportören och identifierar de specifika fickorna och rörelserna som styr varje steg. För icke-specialister innebär detta att forskare nu har en detaljerad ritning för att utforma nya molekyler som antingen förser celler med taurin mer effektivt eller selektivt bromsar dess upptag i sjukdomar som cancer, där celler förlitar sig på överdriven taurintransport.
Citering: Qi, Y., Zhang, Y., Wang, D. et al. Structural mechanism of substrate binding and inhibition of human taurine transporter. Nat Commun 17, 4257 (2026). https://doi.org/10.1038/s41467-026-70772-x
Nyckelord: taurintransportör, membrantransport, kryoelektronmikroskopi, neurokardiovaskulär hälsa, läkemedelsdesign