Clear Sky Science · es
Mecanismo estructural de la unión del sustrato y la inhibición del transportador de taurina humano
Por qué importa esta diminuta bomba de nutrientes
La taurina es una molécula pequeña presente en todo el cuerpo humano, donde contribuye a que el corazón, el cerebro, los ojos y los músculos funcionen correctamente. Las células no pueden depender de la difusión pasiva para obtener suficiente taurina; en su lugar usan una puerta especializada en la membrana celular llamada transportador de taurina. Cuando este transportador falla, se asocia con enfermedades cardíacas, problemas nerviosos, pérdida de visión y cáncer. Este estudio revela, con detalle atómico, cómo el transportador humano de taurina captura la taurina, la introduce en las células y puede ser bloqueado o secuestrado por moléculas tipo fármaco, ofreciendo pistas para futuras terapias.
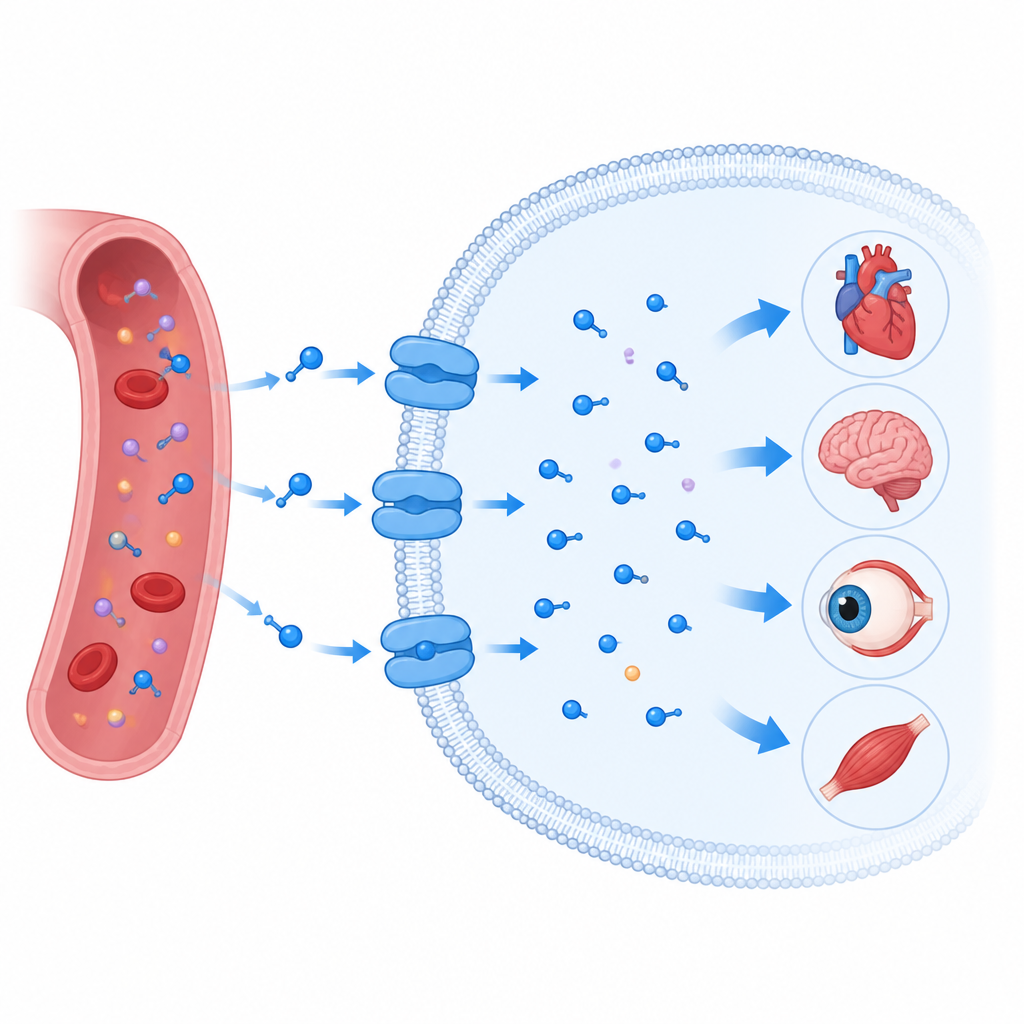
Una puerta que atrae la taurina hacia las células
El transportador de taurina se sitúa en la membrana oleosa que rodea cada célula y pertenece a una amplia familia de proteínas transportadoras que también mueven mensajeros cerebrales como la serotonina y la dopamina. Como sus parientes, no forma simplemente un canal abierto. En cambio, funciona más como una puerta giratoria: se abre hacia un lado de la membrana, se cierra alrededor de su carga y luego se abre hacia el otro lado. Los investigadores usaron criomicroscopía electrónica para determinar múltiples instantáneas tridimensionales del transportador de taurina humano en acción. Lo capturaron vacío, unido a taurina, unido a una molécula relacionada llamada beta alanina, y unido a un análogo de taurina en forma de aro conocido como P4S, en formas orientadas hacia dentro parcialmente cerradas y más abiertas.
Cómo encaja la taurina en su bolsillo a medida
Las estructuras muestran que la taurina se aloja en un bolsillo central profundo dentro del transportador, rodeado por varias hélices que atraviesan la membrana. La taurina tiene un grupo sulfonato cargado negativamente en un extremo y un grupo amino cargado positivamente en el otro, unidos por una corta cadena de carbono. El transportador dispone de un pequeño hueco rico en glicinas que acuna el voluminoso grupo sulfonato y lo ancla mediante una red de enlaces de hidrógeno y un ion sodio coordinado. La cadena de carbono se adapta a una zona hidrofóbica, mientras que el extremo amino alcanza un residuo cargado negativamente que forma un puente salino estabilizador. Este arreglo finamente ajustado explica por qué el transportador prefiere fuertemente la taurina frente a moléculas similares y cómo pequeños cambios en residuos clave pueden debilitar el transporte.
Moléculas impostoras y cómo bloquean o aprovechan la bomba
La beta alanina, un compuesto natural con un grupo carboxilo en lugar del sulfonato de la taurina, se une de forma casi idéntica, usando el mismo bolsillo, iones sodio y puntos de contacto. Sin embargo, forma menos enlaces de hidrógeno, lo que concuerda con su afinidad ligeramente menor por el transportador. P4S, un análogo sintético en forma de aro, también inserta su grupo sulfonato en el mismo hueco y ocupa el sitio de la taurina, pero su anillo rígido no alinea correctamente su grupo amino con el residuo ácido clave. Este desajuste interrumpe una de las interacciones más fuertes y convierte a P4S en un bloqueador de menor afinidad. Dado que las tres moléculas compiten por el mismo sitio, la captación de taurina puede reducirse cuando hay altos niveles de beta alanina o P4S.
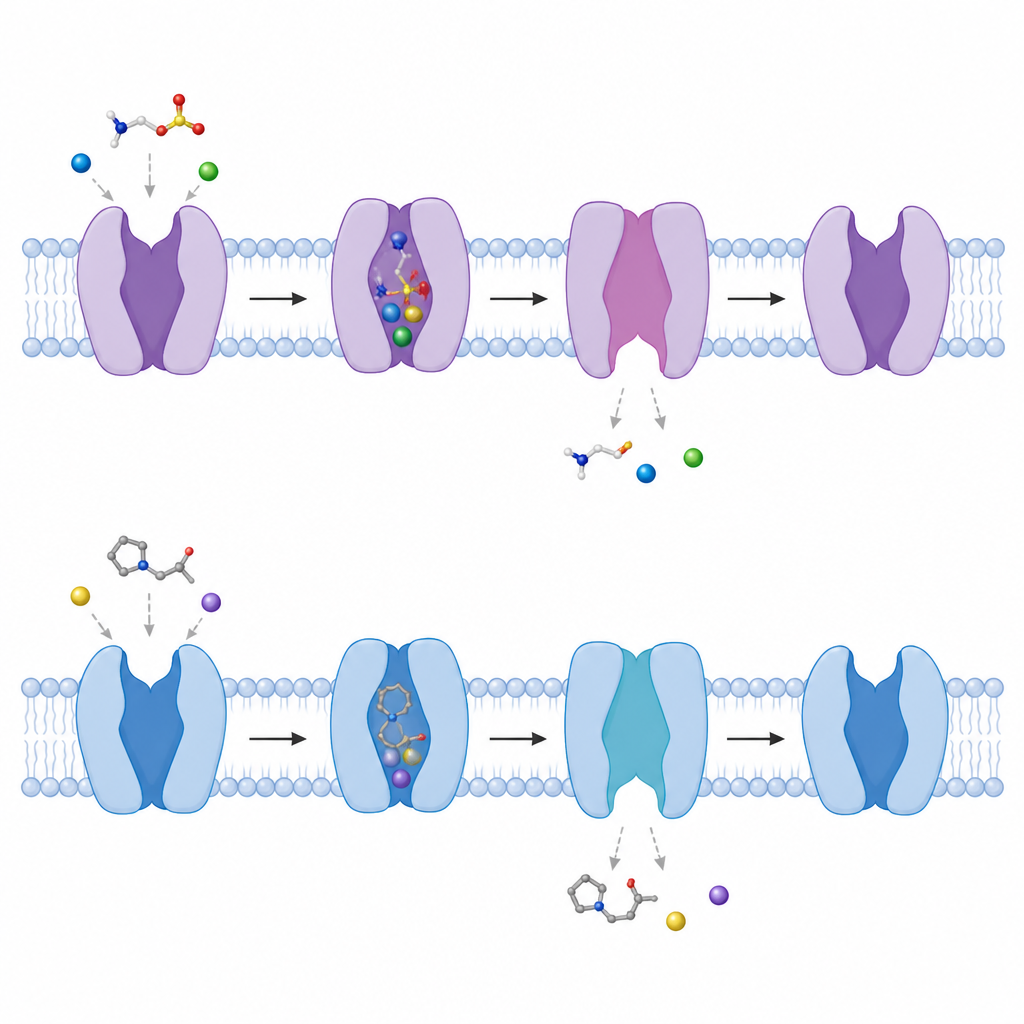
Observando la puerta abrirse hacia el interior celular
Comparando estructuras con y sin moléculas unidas, los autores rastrearon cómo el transportador alterna entre conformaciones. Un segmento helicoidal corto cerca del lado interno de la membrana se dobla hacia afuera aproximadamente 50 grados, y otra hélice se desenrolla parcialmente, creando un túnel desde el bolsillo central hasta el interior de la célula. A medida que esto sucede, los sitios de unión del sodio, cuidadosamente organizados, se deshacen, facilitando la liberación primero del sodio y luego de la taurina al interior celular. El equipo también mostró que, en ausencia de cualquier molécula unida, el transportador oscila de forma natural entre formas orientadas hacia dentro más cerradas y más abiertas, lo que sugiere un paisaje conformacional en constante cambio que le permite responder rápidamente cuando aparece taurina.
Redefiniendo un inhibidor y mirando hacia fármacos
Sorprendentemente, pruebas funcionales revelaron que P4S no es solo un simple tope que atasca la puerta. En cambio, puede ser transportado a través del transportador como la propia taurina, impulsado por el mismo gradiente de sodio, e incluso desencadenar la liberación de taurina pre-cargada desde las células. En otras palabras, P4S se comporta como un análogo de sustrato transportado que compite con la taurina. En conjunto, las instantáneas estructurales y las mediciones de transporte describen un ciclo de trabajo completo para el transportador de taurina e identifican los bolsillos y movimientos específicos que controlan cada paso. Para el público no especializado, esto significa que los investigadores disponen ahora de un plano detallado para diseñar nuevas moléculas que o bien suministren taurina de forma más eficaz o bien ralenticen selectivamente su captación en enfermedades como el cáncer, donde las células dependen de un transporte excesivo de taurina.
Cita: Qi, Y., Zhang, Y., Wang, D. et al. Structural mechanism of substrate binding and inhibition of human taurine transporter. Nat Commun 17, 4257 (2026). https://doi.org/10.1038/s41467-026-70772-x
Palabras clave: transportador de taurina, transporte de membrana, criomicroscopía electrónica, salud neurocardíaca, diseño de fármacos