Clear Sky Science · zh
内分泌治疗重编程乳腺癌通过上调P‑Rex1/Rac1信号通路促进转移逃逸
此项研究对患者的重要性
许多乳腺癌由激素雌激素驱动,术后常需多年使用阻断该信号的药物。即便如此,仍有大量此类癌症在治疗看似结束后多年悄然复发。本研究揭示,阻断激素信号的治疗可以将部分癌细胞推向一种生长缓慢但已准备好迁移的状态,并表明阻断特定的细胞运动通路可能有助于阻止这些迟发且致命的复发。 
缓慢但危险的癌细胞
临床上长期观察到,一些雌激素受体阳性乳腺癌会在初次治疗十年或更久后复发。这些迟发复发常常生长缓慢,但一旦播散便难以治愈。通过分析患者组织,研究者发现来自雌激素驱动肿瘤的转移灶中,活跃分裂的细胞明显少于原发肿瘤。这提示缓慢生长的细胞,而非仅快分裂的细胞,可能是晚期转移的关键驱动者。
构建“静默逃逸”模型
为研究这些“静默逃逸者”,团队在体外用标准阻断激素的药物处理雌激素敏感的乳腺癌细胞。随着时间推移,出现两类幸存者:一类为快速生长的耐药细胞,另一类则分裂缓慢但顽强存活。当将这类慢生长细胞植入小鼠体内时,它们形成的原发乳腺肿瘤体积较小,并表现出类似衰老或应激细胞的特征,包括大而畸形的细胞核和周围致密的胶原。尽管原位生长迟缓,这些细胞向肺和骨的转移效率与快速生长细胞相当,表明生长速度与播散能力并非同一概念。 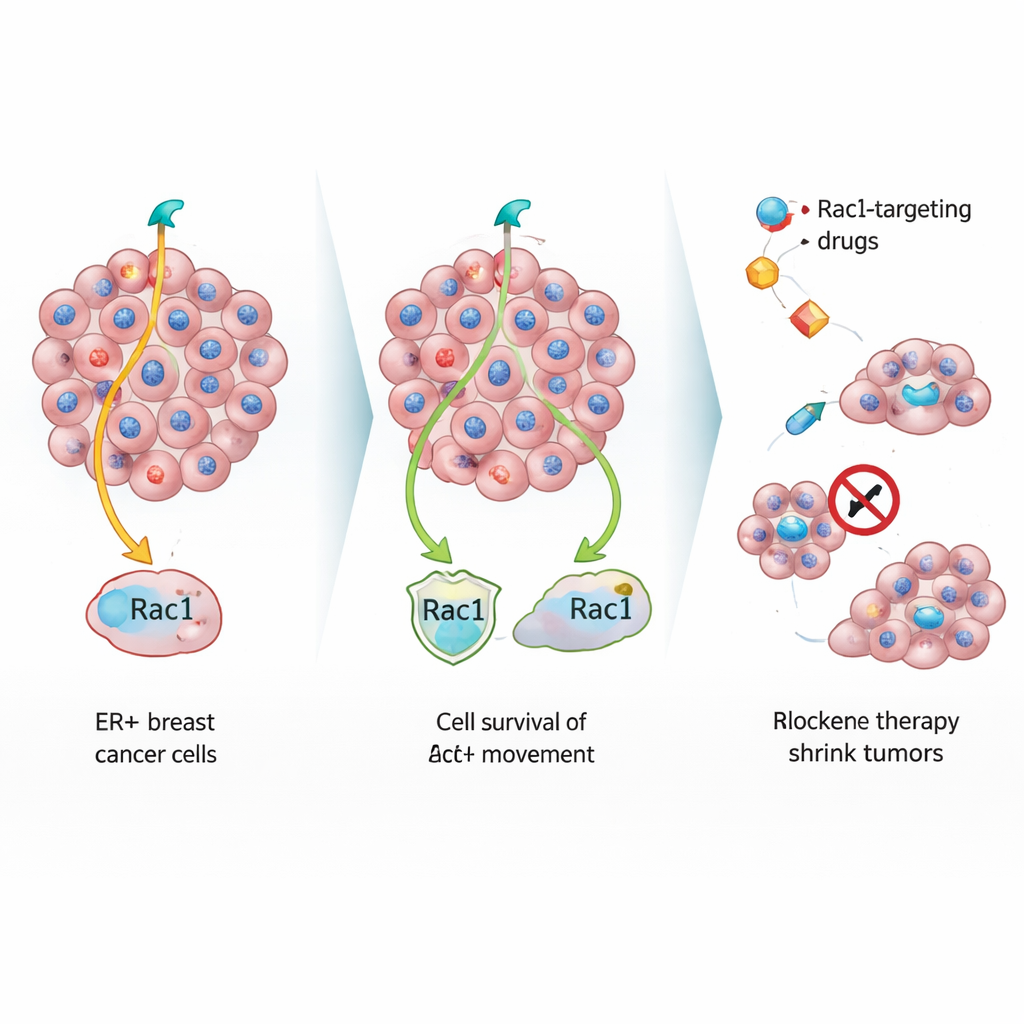
治疗触发的迁移开关
随后团队使用单细胞RNA测序——一种能读取单个细胞中数千基因活性的技术——来观察内分泌治疗如何重塑这些幸存者。他们发现内分泌治疗将一部分细胞推入一种类似衰老的状态,细胞分裂放慢但存活相关通路保持活跃。在这些细胞中,以P‑Rex1和Rac1为中心的信号通路显著上调。Rac1参与控制细胞形态与运动,而P‑Rex1是其关键激活因子之一。慢生长的耐药细胞依赖该轴来迁移,患者样本显示在雌激素受体阳性肿瘤及其转移灶中P‑Rex1水平较高,尤其在那些迟发复发的病例中更为明显。
测试新的药物组合
由于P‑Rex1/Rac1通路看起来像是这些耐受细胞的运动和存活发动机,研究者测试了可抑制Rac1活性的药物。在细胞培养中,这些抑制剂比对快速细胞更明显地减少了慢耐药细胞的克隆形成并减缓了类伤口愈合的闭合速度。在携带Rac1活性荧光传感器的小鼠模型中,两种靶向Rac1的化合物明显降低了他莫西芬处理肿瘤内的Rac1信号。在一例来自已对多种内分泌疗法产生耐药的患者衍生肿瘤模型中,单用Rac1抑制剂虽仅温和延缓肿瘤生长并延长存活期,但与他莫西芬联合使用时,肿瘤出现缩小并显著降低了终末肿瘤重量。
来自真实世界止痛药的线索
其中一种抑制Rac1的试剂R‑ketorolac,是已经用于术后止痛药物的对映体。团队对既往跟踪在手术期使用酮咯酸(ketorolac)患者乳腺癌结局的临床研究进行了荟萃分析。跨这些研究,围手术期使用酮咯酸与较低的癌症复发风险相关,而其他不具Rac1靶向活性的止痛药则未显示出此模式。尽管这不能单独作为确凿证据,但这一群体水平的提示支持了在关键治疗窗口短暂阻断Rac1可能减少耐受细胞播种未来转移的可能性这一假设。
对未来的意义
对非专业读者而言,核心信息是:激素治疗可能无意中将部分乳腺癌细胞重塑为分裂缓慢但高度擅长迁移的状态。这项工作将P‑Rex1/Rac1通路定位为调控该行为的开关,并在动物模型中证明,尤其是与常规内分泌药物联合使用时,抑制该通路可使耐药肿瘤缩小。研究结果尚不足以直接改变标准治疗,但提示将安全的Rac1靶向策略纳入治疗——甚至可能改编自现有的止痛药——未来有望帮助预防雌激素驱动乳腺癌的迟发、危及生命的复发。
引用: Fernandez, K.J., Sultani, G., Nobis, M. et al. Endocrine therapy reprogramming of breast cancer facilitates metastatic escape via upregulation of P-Rex1/Rac1 signalling. Nat Commun 17, 3042 (2026). https://doi.org/10.1038/s41467-026-70683-x
关键词: 雌激素受体阳性乳腺癌, 内分泌治疗耐药, 转移, Rac1 信号, P‑Rex1